 |
Главная |
Порядок выполнения работы. ОПРЕДЕЛЕНИЕ УНИВЕРСАЛЬНОЙ ГАЗОВОЙ ПОСТОЯННОЙ
|
из
5.00
|
ОПРЕДЕЛЕНИЕ УНИВЕРСАЛЬНОЙ ГАЗОВОЙ ПОСТОЯННОЙ
МЕТОДОМ ОТКАЧКИ
Цель работы: определить универсальную газовую постоянную.
Приборы и принадлежности
1. Установка ФПТ1-12
2. Весы
3. Колба
4. Термометр
Краткая теория
Для изучения физических свойств макроскопических систем, состоящих из большого числа частиц, используют два метода: статистический и термодинамический.
Статистический метод основан на законах теории вероятностей и математической статистики. Раздел теоретической физики, в которой изучают физические свойства макроскопических систем с помощью статистического метода, называется статистической физикой.
Термодинамический метод состоит в изучении физических свойств макроскопических систем путем анализа условий и количественных соотношений для процессов превращения энергии в рассматриваемых системах. Соответствующий раздел теоретической физики называется термодинамикой, а макроскопическая система в термодинамике - термодинамической системой.
Физические величины, служащие для характеристики состояния термодинамической системы, называюттермодинамическими параметрамисостояния системы.
К ним относятся: объём, давление, температура, концентрация и др.
Давление - физическая величина Р , численно равная силе, действующей на единицу площади поверхности телапонаправлению нормали к этой поверхности:
 ,
,
где dFn – численное значение нормальной силы, действующейнамалый участок поверхности тела площадью dS .
Более сложным и менее наглядным является параметр состояния, называемый температурой. Понятие температуры имеетсмысл только для равновесных состояний системы. Под равновесным состоянием понимают такое состояние системы, которое не изменяется с течением времени, причём это постоянство не связано с протеканием какого-либо процесса во внешней среде. С молекулярно-кинетической точки зрения температура равновесной системы характеризует интенсивность теплового движения частиц.
Абсолютная температура является мерой средней кинетической энергии поступательного движения молекул идеального газа:

гдеk  – постоянная Больцмана.
– постоянная Больцмана.
В молекулярно-кинетической теории пользуются моделью идеального газа, в котором:
- молекулы газа считаются материальными точками;
- столкновения молекул газа между собой и со стенками сосуда абсолютно упругие;
- потенциальной энергией взаимодействия между молекулами по сравнению с их кинетической энергией пренебрегают.
На основе экспериментов с достаточно разреженными газами были установлены законы, справедливые для идеального газа.
1. Закон Бойля - Мариотта (для изотермическогопроцесса).
 . (1)
. (1)
2. Закон Гей-Люссака (для изохорического процесса).
 . (2)
. (2)
3. Закон Шарля (для изобарического процесса).
 . (3)
. (3)
С помощью законов Бойля - Мариотта и Гей-Люссака легко найти связь между объёмом, давлением и температурой для произвольного равновесного состояния идеального газа:
 , (4)
, (4)
где V0 – объем одного моля газа,
R – универсальная газовая постоянная, численно равная работе, совершаемой одним молем газа при изобарном нагревании его на один градус.
Уравнение (4) называется уравнением Менделеева – Клапейрона (уравнение состояния идеального газа).
Для любой массы газа оно запишется так:
 , (5)
, (5)
где  - число молей (количество вещества).
- число молей (количество вещества).
Моль – количество вещества системы, в котором содержится столько же структурных элементов (молекул, атомов, ионов, электронов и других структурных элементов), сколько содержится атомов в 0,012 кг изотопа углерода 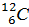 . Из определения моля следует, что 1 моль различных веществ (газообразных, жидких, твердых) содержит одинаковое число Авогадро NА = 6,022.1023 моль-1 структурных элементов.
. Из определения моля следует, что 1 моль различных веществ (газообразных, жидких, твердых) содержит одинаковое число Авогадро NА = 6,022.1023 моль-1 структурных элементов.
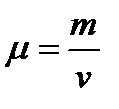 называется молярной массой газа. Масса моля, выраженная в граммах, численно равна относительной молекулярной массе.
называется молярной массой газа. Масса моля, выраженная в граммах, численно равна относительной молекулярной массе.
Теория метода и описание установки.
Установка ФПТ1-12 представляет собой конструкцию настольного типа (рис.1), состоящую из:
- блока измерительного (поз.1);
- колбы (поз.З), установленной на весах (поз. 2);
Блок измерительный представляет собой коробчатый конструктив. В нем установлен вакуумметр (поз 4.).
На лицевой панели блока БП-12 установлены органы управления и световой индикации, термометр для измерения температуры окружающей среды, внутри блока установлен компрессор.
Колба установлена на весах и соединена с вакуумметром вакуумной трубкой.
Соединение компрессора со штуцером измерительного блока осуществляется с помощью вакуумной трубки.
УСТАНОВКА ФПТ1-12 (рис. 1)

1. Блок измерительный
2. Весы
3. Колба
4. Вакуумметр
5. термометр
Порядок выполнения работы
Уравнение Менцелеева-Клапейрона (5) для объёма V при комнатной температуре Т и атмосферном давлении Р1 для массы воздуха М1 в шаре запишется:
 ,
,
где M1=m1- m0; m0 - масса пустого шара; m1 - суммарная масса шара и воздуха в нем при давлении P1.
Если откачать насосом воздух из шара, то давление в нем будет P2 (при той же температуреТ). Уравнение 5 запишется так:
 ,
,
где M2 = m2 – m0; m2 - суммарная масса шара и воздуха в
нем при давлении P2.
Из последних уравнении найдем универсальную газовую постоянную:
 . (6)
. (6)
1. Подать напряжение питания на электронные весы и включить установку тумблером «СЕТЬ». При этом загорается сигнальная лампа.
2.С помощью электронных весов определить массу колбы с воздухом m1 при давлении P1.
3. Включить компрессор кнопкой «ПУСК» и, удерживая кнопку нажатой откачать воздух из колбы до давления Р2. После чего, закрыв кран и выключив компрессор (отпустив кнопку «ПУСК»), определить массу колбы с воздухом m2 при давлении Р2.
4. Повторить измерения по п. 3 не менее 3 раз.
5. Измерить температуру воздуха в лаборатории.
6. Выключить установку тумблером «СЕТЬ».
7. По формуле (6) рассчитайте универсальную газовую постоянную R . При этом следует учесть, что  - молярная масса воздуха,
- молярная масса воздуха,
 - объем колбы.
- объем колбы.
8. Данные измерений и вычислений записать в таблицу.
9. Определите среднее значение  .
.
10. По среднему значению  определить для каждого опыта абсолютную погрешность
определить для каждого опыта абсолютную погрешность  , а затем и ее среднее значение
, а затем и ее среднее значение  .
.
11. Результат записать в виде
 .
.
Таблица измерений и вычислений.
| № опыта | 
| 
| 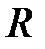
| 
| 
| 
|
| … | ||||||
Контрольные вопросы
1. В чём сущность и различие термодинамического и статистического методов исследования физических явлений?
2. Какой смысл вкладывается в понятие "термодинамическое состояние тела"? Какие параметры состояния вы знаете?
3. Какой газ называется идеальным?
4. Каков физический смысл универсальной газовой постоянной? В каких единицах она измеряется?
5. Выведите уравнение Менделеева - Клапейрона.
6. Что такое моль? Что такое число Авогадро?
7. Что такое относительная молекулярная масса?
8. Какие приборы служат для измерения давления жидкостей и газов? Чем отличается вакуумметр от манометра?
|
из
5.00
|
Обсуждение в статье: Порядок выполнения работы. ОПРЕДЕЛЕНИЕ УНИВЕРСАЛЬНОЙ ГАЗОВОЙ ПОСТОЯННОЙ |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

