 |
Главная |
Основные расчетные формулы молярных масс эквивалентов
|
из
5.00
|
ОПРЕДЕЛЕНИЕ МОЛЯРНОЙ МАССЫ ЭКВИВАЛЕНТА МЕТАЛЛА
(Mg, Al или Zn) МЕТОДОМ ВЫТЕСНЕНИЯ ВОДОРОДА
Цель работы: ознакомление с понятием эквивалента вещества и методикой расчета, связанной с законом эквивалентов.
Теоретическая часть
Эквивалент (Э) – это реальная или условная частица вещества, которая может замещать, присоединять или быть каким-либо другим образом эквивалентна (равноценна) одному иону водорода (Н+) в кислотно-основных или ионно-обменных реакциях или одному электрону (е–) в окислительно – восстановительных реакциях. Так же, как молекула, атом или ион, эквивалент безразмерен. И так же, как в случае молекул, атомов или ионов, состав эквивалента выражают с помощью химических знаков и формул.
Для того, чтобы определить состав эквивалента вещества и правильно записать его химическую формулу, надо исходить из конкретной реакции, в которой участвует данное вещество.
Рассмотрим несколько примеров определения формулы эквивалента.
 . (а)
. (а)
С одним ионом водорода реагирует один ион гидроксила, поэтому Э  .
.
 . (б)
. (б)
В реакции (б) один ион водорода эквивалентен 1/2 иона кальция, одному иону  и одному иону
и одному иону  . Следовательно Э
. Следовательно Э  ; Э
; Э  ; Э
; Э  .
.
Запишем уравнение этой реакции в молекулярной форме:
 .
.
Одному иону Н+ эквивалентна 1/2 молекулы Са(ОН)2, следовательно, Э  . В реакции
. В реакции
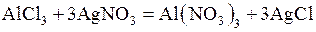 (в)
(в)
эквиваленты AlCl3 и AlNO3 можно определить косвенным путем, введя вспомогательные реакции:

Одному иону водорода (Н+) эквивалентна 1/3 молекулы AlCl3 и молекула AgNO3, следовательно Э  ; и Э
; и Э  .
.
 . (г)
. (г)
В этой окислительно-восстановительной реакции с одним ионом цинка взаимодействуют два электрона. Поэтому эквивалент 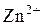 Э
Э 
 . (д)
. (д)
В этом случае один ион 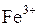 реагирует с тремя электронами и, следовательно, Э
реагирует с тремя электронами и, следовательно, Э 
 (е)
(е)
В данной окислительно-восстановительной реакции атом марганца  в молекуле KMnO4 принимает пять электронов и превращается в марганец со ст. ок. +2
в молекуле KMnO4 принимает пять электронов и превращается в марганец со ст. ок. +2 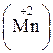
 .
.
В молекуле FeSO4 атом железа 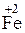 отдает один электрон и превращается в железо со ст. ок. +3
отдает один электрон и превращается в железо со ст. ок. +3
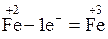 .
.
Поэтому Э  ;
;
Э  .
.
Величина, показывающая какая доля реальной частицы соответствует эквиваленту, получила название фактора эквивалентности 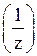 , z – всегда целое положительное число и называется эквивалентное число.
, z – всегда целое положительное число и называется эквивалентное число.
В обменных реакциях величина z равна суммарному заряду обменивающихся ионов, т.е. z = число ионов ´ заряд иона. В реакции
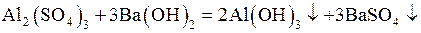 (ж)
(ж)
 .
.
В реакции (б)  ; в реакции (д)
; в реакции (д)  .
.
Количество вещества измеряют в молях. Один моль эквивалентов содержит столько же эквивалентов, сколько атомов углерода содержится в 0,012 кг углерода – 12, т.е. 6,02 ∙ 1023 атомов. Количество вещества эквивалентов определяется формулой 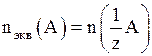 . Масса моля эквивалентов называется молярной массой эквивалента Мэ.
. Масса моля эквивалентов называется молярной массой эквивалента Мэ.
Например, молярные массы эквивалентов в рассматриваемых ранее реакциях равны:
 г/моль;
г/моль;
 г/моль и т.д.
г/моль и т.д.
Молярная масса эквивалентов вещества определяется формулой:

(для водорода – 1 г/моль; для кислорода – 8 г/моль).
Состав эквивалента вещества зависит от реакции, поэтому молярная масса эквивалента одного и того же вещества может быть разной. Например, молярная масса эквивалента FeSO4 в реакции
FeSO4 + 2HCl = FeCl2 + H2SO4
равна 75,925 г/моль, т.к. Э  , т.е.
, т.е.
 г/моль = 75,925 г/моль,
г/моль = 75,925 г/моль,
а в реакции
 ;
;

Э(FeSO4) = FeSO4; МЭ(FeSO4) = М(FeSO4) = 151,85 г/моль.
Основные расчетные формулы молярных масс эквивалентов
Сложных веществ
Молярная масса эквивалентов элемента в соединении АаВв:
 ,
,
где в – эквивалентное число.
Молярная масса эквивалентов оксида А2Ов:
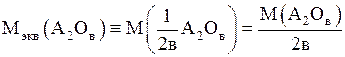 .
.
Молярная масса эквивалентов кислоты НаВ:
 ,
,
где а – основность кислоты.
Молярная масса эквивалентов основания А(ОН)в:
 ,
,
где в – кислотность основания.
Молярная масса эквивалентов соли АаВв:
 .
.
Моль любого газа при нормальных условиях занимает объем Vm = 22,4 л. Соответственно, для вычисления объема моля эквивалентов газа необходимо знать число молей эквивалентов в одном моле газа. Например, в реакции окисления водорода

Э 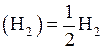 , поэтому
, поэтому  , значит один моль эквивалентов водорода занимает при нормальных условиях объем
, значит один моль эквивалентов водорода занимает при нормальных условиях объем
 л.
л.
Объем одного моля эквивалентов кислорода в реакции восстановления

равен 22,4 : 4 = 5,6 л, т.к. Э  ,
,  . Объем эквивалентов вещества определяется формулой:
. Объем эквивалентов вещества определяется формулой:

(для водорода – 11,2 л/моль, для кислорода – 5,6 л/моль).
| Закон эквивалентов: вещества реагируют друг с другом в эквивалентных соотношениях, т.е. моль эквивалентов одного вещества реагирует с молем эквивалентов другого вещества. |
Например, в реакции:

 ;
; 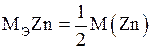
 ;
;  ,
,
т.е. один моль эквивалентов цинка (  моль Zn) реагирует с одним молем эквивалентов кислоты (1 моль HCl) с образованием одного моля эквивалентов хлорида цинка (
моль Zn) реагирует с одним молем эквивалентов кислоты (1 моль HCl) с образованием одного моля эквивалентов хлорида цинка (  моль ZnCl2). В соответствии с законом эквивалентов количество веществ эквивалентов реагирующих соединений равны:
моль ZnCl2). В соответствии с законом эквивалентов количество веществ эквивалентов реагирующих соединений равны:
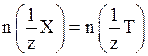 ,
,
где Т – вещество, вступающее в реакцию с анализируемым соединением.
Раствор, содержащий один моль эквивалентов вещества в литре, называется «нормальным». Нормальная концентрация раствора выражается в кмоль/м3 или моль/л и обозначается «Н» или «N». Закон эквивалентов для реакции:
mA + nB = AmBn,
протекающей в растворе, можно записать следующим образом:
 ,
,
где VA и VB – объемы реагирующих растворов; NА и NВ – их нормальные концентрации.
Закон эквивалентных отношений можно выразить формулой:
 .
.
Определение количества вещества эквивалентов А
 .
.
Для удобства расчетов в аналитике используют вспомогательный способ выражения состава раствора – молярную концентрацию эквивалента  :
:
 .
.
|
из
5.00
|
Обсуждение в статье: Основные расчетные формулы молярных масс эквивалентов |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

