 |
Главная |
Организация дыхательной цепи. Переносчики в дыхательной цепи (ЦПЭ)
|
из
5.00
|
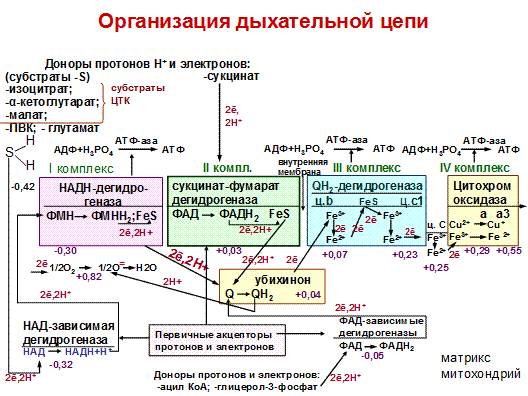
Основные переносчики электронов встроены во внутреннюю мембрану митохондрий и организованы в 4 комплекса. Компоненты комплексов расположены в строго определенной последовательности, в порядке возрастания их окислительно-восстановительных потенциалов (редокс-потенциалов). Величина редокс-потенциала связана с изменением свободной энергии. Её выражают в вольтах; чем она меньше (отрицательнее), тем меньше сродство вещества к электронам. Чем больше сродство, тем больше восстановительный потенциал.
I комплекс – НАДН-дегидрогеназа– состоит из нескольких полипептидных цепей.
В I комплекс входят две простетические группы: ФМН и FeS (железо-серные белки). Атомы железа в этих белках (негемовое железо) собраны в несколько групп, так называемых железо-серных центров. Известны 3 типа FeS-центров (FeS, Fe2S2, Fe4S4), в котором атом железа связан с атомом серы остатками цистеина или неорганической серы.
На I комплекс протоны и электроны от субстратов (изоцитрат, малат и др.) транспортирует главный первичный акцептор водорода – НАД-зависимая дегидрогеназа (восстановленная форма НАДН+Н+). НАДН+Н+ - два электрона и один протон переносятся на ФМН простетическую группу I комплекса с образованием ФМНН2. Второй протон поглощается из матрикса. С ФМНН2 электроны и протоны транспортируются на FeS. От железо-серных центров электроны и протоны переносятся на кофермент Q (убихинон).
II комплекс– сукцинат-фумарат-дегидрогеназа.Состоит из 2 простетических групп: ФАД и FeS. На ФАД электроны и протоны отщепляются от субстрата – сукцинат, при этом ФАД восстанавливается в ФАДН2. Затем протоны и электроны передаются на FeS, с FeS они транспортируется на убихинон.
Убихинон- (вездесущий хинон) или кофермент Q. Это небелковый переносчик. Он является жирорастворимым соединением. Структура КоQ сходна с витаминами К, Е.
Молекулы убихинона различаются длиной углеводородной цепи, которая у млекопитающих содержит 10 изопреноидных звеньев и обозначается как Q10.
Убихинон выполняет коллекторную функцию, присоединяя ē и протоны от НАДН-дегидрогеназы (I комплекс), сукцинат-фумаратдегидрогеназы (II комплекс) и ФАД- зависимых дегидрогеназ, он обратимо восстанавливается в гидрохинон (QН2).
Содержание убихинона значительно превосходит количество других компонентов ЦПЭ. Например, на 1 молекулу НАД+ приходится 50молекул КоQ.
От убихинона происходит транспорт только электронов на цитохромы.
Цитохромы.
Обнаружены в 1886г. Мак-Мунном, исследованы в 1925г. Девидом Кейлином.
Цитохромы – это сложные белки-гемопротеины, которые в качестве простетической группы содержат гем.
Известно около 30 различных цитохромов.
Их многообразие обусловлено:
- различием боковых цепей в структуре гема;
- различием в структуре полипептидных цепей;
- различием в способе связи полипептидных цепей с гемом.
В зависимости от способности поглощать свет в различной части спектра все цитохромы делятся на группы а, в, с. Внутри каждой группы отдельные виды с уникальными спектральными свойствами обозначают цифровыми индексами (в, в1, в2 и т.д.)
Цитохромы имеют ряд особенностей:
1. Цитохромы в ЦПЭ располагаются в порядке возрастания окислительно-восстановительного потенциала (редокс-потенциала);
2. Железо в цитохромах способно изменять свою степень окисления, поэтому цитохромы в ЦПЭ транспортируют только электроны.
В транспорте двух электронов принимают участие две молекулы каждого вида цитохромов, так как одна молекула цитохрома может переносить только один электрон.
В ЦПЭ участвуют 5 типов цитохромов- а, а3, в, с, с1. За исключением цитохрома с, все цитохромы находятся во внутренней мембране митохондрий в виде сложных белковых комплексов.
III комплекс –QН2-дегидрогеназа состоит из 2 типов цитохромов (в1 и в2), цитохрома с1 и FeS. Внутри комплекса электроны передаются от цитохромов в на FeS-центры, затем на цитохром с1. С цитохрома с1 электроны транспортируются на цитохром С.Это периферический водорастворимый мембранный белок с молекулярной массой 12500Д, имеющий одну полипептидную цепь из 100 аминокислотных остатков и молекулу гема, ковалентно связанную с полипептидом. От цитохрома С электроны переносятся на IV комплекс.
IV комплекс –цитохромоксидазавходят два цитохрома типа аа3, каждый из которых имеет центр связывания с кислородом. Цитохромы а и а3 имеют в своей структуре гем А, отличающийся от гема цитохромов с и с1. Он содержит формильную группу вместо одной из метильных групп и углеводородную цепь вместо одной из винильных групп.
Другая особенность комплекса аа3 – наличие в нем ионов меди, связанных с белковой частью в так называемых CuA- центрах. Перенос электронов комплексом а-а3 включает реакции:
 Cu+ Cu2+ + ē
Cu+ Cu2+ + ē
 Fe2+ Fe3+ + ē
Fe2+ Fe3+ + ē
Комплекс цитохромов а-а3 транспортирует электроны непосредственно на молекулярный кислород, активируя его:
аа3 2ē ½ О2 О=
 |  |
У активированного кислорода появляются две свободные валентности, к которым присоединяются 2 протона Н+ от первичных акцепторов водорода: НАД-зависимых дегидрогеназ, ФАД-зависимых дегидрогеназ; сукцинат-фумарат-дегидрогеназы (II комплекс) через убихинон (QН2).
|
|
из
5.00
|
Обсуждение в статье: Организация дыхательной цепи. Переносчики в дыхательной цепи (ЦПЭ) |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

