 |
Главная |
Факторы, влияющие на основность
|
из
5.00
|
1. Природа гетероатома в основном центре
Н3С - NH2 > Н3С - OH Н3С - OH > Н3С – SH
Сила оснований зависит от электроотрицательности гетероатома в основном центре. Чем больше ЭО атома, тем слабее основные свойства, поэтому спирты и простые эфиры являются более слабыми основаниями по сравнению с аминами.
2. Строение радикала, связанного с основным центром.
 анилин Н3С → СН2 → NH2 этиламин
анилин Н3С → СН2 → NH2 этиламин
Алифатические амины проявляют более сильные основные свойства, чем ароматические. Объясняется это тем, что алкильные радикалы являются электронодонорами (электронная плотность на атоме азота повышается, что облегчает присоединение протона), а бензольное кольцо электроноакцептором (электронная плотность на атоме азота понижается, что затрудняет присоединение протона).
Электронодонорые заместители усиливают основные свойства, а электроноакцепторные – уменьшают, например:
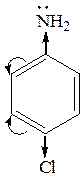 4-хлоранилин
4-хлоранилин  анилин
анилин 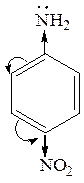 4-нитроанилин
4-нитроанилин
РКВН+ 5,1 4,6 1,0

уменьшение основности
3. Влияние растворителя
В водной среде важную роль играет уменьшение пространственных препятствий для гидратации, поэтому вторичные амины лучше гидратируются, чем третичные, которые пространственно труднодоступны.
 H3C - NH – CH3 > H3C – NH2 > H3C - N – CH3
H3C - NH – CH3 > H3C – NH2 > H3C - N – CH3
CH3
 |
основность уменьшается
В газовой среде основность возрастает с увеличением углеводородных радикалов, так как усиливается их стабилизирующее действие за счет +I-эффекта на катион сопряженной кислоты, поэтому третичные амины проявляют более сильные основные свойства по сравнению с другими аминами.
 H3C - N – CH3 > H3C - NH – CH3 > H3C – NH2
H3C - N – CH3 > H3C - NH – CH3 > H3C – NH2
CH3
 основность уменьшается
основность уменьшается
Вопросы для самоконтроля
1. Теория Бренстеда - Лоури. Сопряженные кислоты и основания.
2. Кислотные свойства органических соединений с водородосодержащими функциональными группами (спирты, фенолы, тиолы, карбоновые кислоты, амины).
3. Основные свойства органических соединений.
4. Факторы, влияющие на реакционную способность кислот и оснований.
Упражнения
1. Объясните, какое из соединений проявляет более сильные кислотные свойства и почему?
а) CH3 -SH, б) CH3-NH2, в) CH3-OH.
2. Какая кислота является более сильной и почему?
а) СH3COOH, б) Сl-CH2COOH, в) Cl2- CH – COOH.
3. Объясните, почему анилин проявляет более слабые основные свойства, по сравнению с этиламином.
4. Напишите реакцию, которая доказывает более сильные кислотные свойства фенола по сравнению со спиртами.
5. В качестве антидота при отравлении солями мышьяка был предложен 2,3-димеркаптопропанол. Объясните, чем определяется его большая кислотность в сравнении с пропантриолом.
|
из
5.00
|
Обсуждение в статье: Факторы, влияющие на основность |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

