 |
Главная |
Строение атома. Модель Томсона
|
из
5.00
|
Дискретность электрического заряда
Начиная изучение электродинамики, перед тем как приступать к рассмотрению основных понятий заряда, сохранения зарядов, электризации и т. д., необходимо обратиться к первым экспериментальным фактам, полученным человеком по этому вопросу. Впервые электрические опыты были задокументированно произведены в пятом веке до нашей эры в Греции. А именно, было замечено явление притягивания янтарной расчёской, которой недавно расчёсывали волосы, небольших частиц любого вещества: волосков, пылинок, кусочков ткани, бумаги и т. д. (рис. 1).

Рис. 1. Действие потёртой о волосы или мех янтарной расчёски (Источник)
Собственно говоря, мы сейчас и пришли к этимологии слова «электричество, ведь «электрон» в переводе с греческого и означает «янтарь».
Следующие опыты по электризации тел были проведены лишь в 1729 году французским исследователем Шарлем Дюфе (рис. 2). Он проводил натирание стеклянных и смоляных палочек шёлком и шерстью соответственно. В результате получился эффект в точности такой же, какой и был описан древними греками. И палочки, и тряпочки начали притягивать мелкие кусочки материалов. Дюфе понял эти явления так, что, конечно же, при натирании палочки меняют свои свойства. И вот новые свойства стеклянной палочки он назвал «стеклянными», или же что палочка приобретает «стеклянный» заряд. Соответственно, на смоляную палочку перетекает «смоляной» заряд в терминологии Дюфе.

Рис. 2. Шарль Дюфе (Источник)
Строение атома
Теперь рассмотрим непосредственно, откуда берутся указанные электрические заряды. Для этого следует обратиться к структуре атома. Как известно из курса химии, все вещества состоят из молекул, которые в свою очередь состоят из атомов. Атом же состоит из трёх различных частиц: электронов, протонов и нейтронов.

Рис. 5. Строение атома гелия
Подробнее разберём строение атома на примере атома гелия – второго химического элемента в таблице Менделеева (рис. 5). Химическая формула атома гелия:
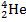
Индекс 2 говорит нам о том, что в ядре атома гелия находятся две положительно заряженные частицы – протоны (р). Таким же количеством частиц – электронами (е), и скомпенсирован положительный заряд ядра. Электроны непрерывно вращаются вокруг ядра на значительно большем расстоянии, нежели размеры самого ядра. Индекс же 4 означает, что всего в ядре находится 4 частицы. Две дополнительные частицы – это нейтроны (n), которые не имеют электрического заряда.
Электризация
Рассмотрим теперь собственно сам механизм электризации (то есть перераспределение заряда). Для начала, скажем, что проводить её можно несколькими способами:
Способы электризации:
*Трением (прикосновением);
*Влиянием;
*Освещением;
*Химическим способом
А теперь примем во внимание, что элементарным носителем зарядов является электрон. Так как практически невозможно вырвать протон из ядра (очень сильные ядерные связи можно разорвать только вследствие ядерной реакции), то поменять заряд какого-либо тела, а значит, поменять заряд какого-то количества атомов можно, либо забирая из атомов электроны, либо передавая новые. В результате этих процессов атом превращается в ион.
Определение. Ион – атом, потерявший или приобревший один или несколько электронов, вследствие чего получивший положительный или отрицательный заряд соответственно.
Замкнутая система – совокупность тел, взаимодействующих между собой, на которые не действуют внешние силы.
Примером выполнения закона служит следующий случай. Если два одинаковых шара зарядить зарядами Кл и Кл, а потом соединить, то после совмещения заряд разделится таким образом, что на каждом из шаров остаётся по 1 Кл. Так как суммарный заряд что до соединения, что после должен оставаться постоянным, а именно Кл. А так как тела одинаковые, заряды всегда разделятся поровну.
Строение атома. Модель Томсона
После того, как стало ясно, что атом тоже имеет сложную структуру, как-то по-особенному устроен, необходимо было исследовать само строение атома, объяснить, как он устроен, из чего состоит. И вот ученые приступили к этому изучению.
Первые идеи о сложном строении были высказаны Томсоном, который в 1897 году открыл электрон. В 1903 году Томсон впервые предложил модель атома. По теории Томсона, атом представлял собой шар, по всему объему которого «размазан» положительный заряд. А внутри, как плавающие элементы, находились электроны. В целом, по Томсону, атом был электронейтрален, т. е. заряд такого атома был равен 0. Отрицательные заряды электронов компенсировали положительный заряд самого атома. Размер атома составлял приблизительно 10-10м. Модель Томсона получила название «пудинг с изюмом»: сам «пудинг» – это положительно заряженное «тело» атома, а «изюм» – это электроны (рис. 1).
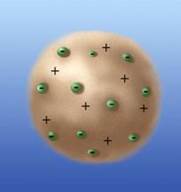
Рис. 1. Модель атома Томсона («пудинг с изюмом»)
Модель Резерфорда
Первый достоверный опыт по определению строения атома удалось провести Э. Резерфорду. На сегодняшний день мы твердо знаем, что атом представляет собой структуру, напоминающую планетную солнечную систему. В центре находится массивное тело, вокруг которого вращаются планеты. Такая модель атома получила название планетарной модели.
Опыт Резерфорда
Давайте обратимся к схеме опыта Резерфорда (рис. 2) и обсудим результаты, которые привели к созданию планетарной модели.

Рис. 2. Схема опыта Резерфорда
Внутрь свинцового цилиндра с узким отверстием был заложен радий. При помощи диафрагмы создавался узкий пучок a-частиц, которые, пролетая через отверстие диафрагмы, попадали на экран, покрытый специальным составом, при попадании возникала микро-вспышка. Такое свечение при попадании частиц на экран называется «сцинтиляционная вспышка». Такие вспышки наблюдались на поверхности экрана при помощи микроскопа. В дальнейшем до тех пор, пока в схеме не было золотой пластины, все частицы, которые вылетали из цилиндра, попадали в одну точку. Когда же внутрь экрана на пути летящих a-частиц была поставлена очень тонкая пластинка из золота, стали наблюдаться совершенно непонятные вещи. Как только была поставлена золотая пластина, начались отклонения a-частиц. Были замечены частицы, которые отклонялись от своего первоначального прямолинейного движения и уже попадали в совершенно другие точки этого экрана.
Более того, когда экран сделали почти замкнутым, выяснилось, что есть частицы, которые каким-то образом летят в обратную сторону. Они отклоняются под углом 90° и больше. Эти наблюдения были проанализированы Резерфордом, и выяснилась следующая довольно любопытная вещь.
|
из
5.00
|
Обсуждение в статье: Строение атома. Модель Томсона |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

