 |
Главная |
Ферментативное осахаривание крахмала
|
из
5.00
|
ПРОИЗВОДСТВО ЭТАНОЛА
Мировой рынок этанола составляет около 4 млрд. дал (декалитров абсолютного алкоголя) в год. Лидерами в производстве этанола являются США, Бразилия, Китай. В США функционирует 97 заводов по производству этанола из кукурузы (строится еще 35 заводов) общей мощностью 1,5 млрд. дал в год.
Основные направления использования этанола в мировой практике:
− 60% − добавка к моторному топливу;
− 25% − химическая промышленность;
− 15% − пищевая промышленность (доля ее сокращается).
Автомобильное топливо на основе этанола содержит 10% этанола (топливо Е-10) или 85% этанола (Е 85). При стоимости нефти 60-70 $ за баррель биоэтанол становится конкурентоспособным топливом. Введение этанола в бензин позволяет отказаться от добавки в топливо тетраэтилсвинца, в результате чего снижается токсичность выхлопных газов и расход горючего.
В США проводятся масштабные исследования по производству биоэтанола из возобновляемого растительного сырья (из стеблей кукурузы, тростника и др.)
В промышленных условиях этанол получают гидратацией этилена в присутствии катализатора (H3PO4 на силикагеле), из гидролизатов растительного сырья (древесины, стеблей кукурузы, тростника), а также из крахмалсодержащего сырья (пшеница, рожь, тритикале, картофель), мелассы, молочной сыворотки, топинамбура. Средний выход 95,5%-ного этилового спирта из 1 т различных видов сырья представлен в таблице 2.1.
Таблица 2.1
Выход этанола из различных видов сырья
| Сырье | Выход спирта, л |
| Пшеница | 321,7 |
| Кукуруза | 317,9 |
| Гречиха | 315,6 |
| Рис | 300,9 |
| Ячмень | 299,7 |
| Рожь | 298,2 |
| Меласса | 266,4 |
| Овес | 240,7 |
| Картофель | 86,3 |
| Сахарная свекла | 83,6 |
Окончание таблицы 2.1
| Сырье | Выход спирта, л |
| Яблоки | 54,5 |
| Сливы | 42,1 |
| Морковь | 37,0 |
| Молочная сыворотка с 4% лактозы | 25,4 |
На спиртовых заводах Республики Беларусь (функционирует около 70 спиртовых заводов общей мощностью более 9 млн. дал в год) для производства этанола используют крахмалсодержащее сырье, главным образом зерно злаков. Содержание крахмала в различных видах зерна составляет (в %): пшеница – 48–57; рожь – 46–53; ячмень – 43–55; овес – 34–40; просо – 42–60; кукуруза – 61–70. В зерне содержатся также (в среднем) сахара ~ 3%; клетчатка ~ 6%; пентозаны и пектиновые вещества ~ 9%; азотистые (белковые) вещества ~ 11%, жир ~ 3%.
Продуценты этанола
При микробиологическом синтезе классическими продуцентами этанола являются дрожжи - сахаромицеты и шизосахаромицеты. Чаще других используют дрожжи Saccharomyces cerevisiae, Saccharomyces vini, Schizosaccharomyces pombe.
Сахаромицеты имеют клетки округлой формы размером 10-15 мкм, размножаются почкованием. Шизосахаромицеты имеют крупные палочковидные клетки диаметром 4-5 мкм и длиной 18-20 мкм, размножаются делением. И те, и другие дрожжи хорошо сбраживают глюкозу, маннозу, фруктозу, сахарозу, мальтозу, труднее сбраживают галактозу и не сбраживают пентозные сахара (ксилозу, арабинозу).
Теоретический выход этанола из 100 кг сброженной глюкозы составляет 51,14 кг или 64,80 л (при этом образуется 48,86 кг СО2). На практике выход спирта составляет 82-92% от теоретического в связи с расходом части субстрата на размножение и рост дрожжей и образование побочных продуктов.
 Синтез этанола в дрожжевой клетке осуществляется по следующей схеме:
Синтез этанола в дрожжевой клетке осуществляется по следующей схеме:
Побочными продуктами спиртового брожения являются глицерин, высшие (сивушные) спирты, органические кислоты (уксусная, пировиноградная, молочная, янтарная), альдегиды. При спиртовом брожении сахар (глюкоза) расходуется на образование различных веществ в следующем количестве: этанола - 46-47%, диоксида углерода - 44-46%, биомассы дрожжей - 1,8-4,0%, глицерина - 3-4%, высших спиртов - 0,3-0,7%, органических кислот - 0,2-1,0%, альдегидов - 0,1-0,2%. При многократном возврате дрожжей на брожение расход сахара на образование биомассы сокращается, а интенсивность брожения даже несколько возрастает.
Образование глицерина при спиртовом брожении объясняется тем, что в индукционный период (до образования уксусного альдегида) между двумя молекулами фосфоглицеринового альдегида под действием фермента альдегидмутазы при участии молекулы воды происходит реакция дисмутации. При этом одна молекула фосфоглицеринового альдегида восстанавливается, образуя фосфоглицерин, а другая окисляется в 3-фосфоглицериновую кислоту. Фосфоглицерин в дальнейших реакциях не участвует и после отщепления фосфорной кислоты является побочным продуктом спиртового брожения. 3-фосфогли-цериновая кислота претерпевает превращения по ЭМП-пути с образованием уксусного альдегида. После появления уксусного альдегида наступает стационарный период брожения, при котором окисление фосфоглицеринового альдегида в фосфоглицериновую кислоту протекает более сложным путем, с присоединением неорганического фосфата (ЭМП-путь). В связи с этим наряду с этанолом при брожении всегда образуется некоторое количество глицерина.
При связывании уксусного альдегида бисульфитом процесс брожения направляется в сторону образования глицерина:
С6Н12О6 ® СН3СНО + СО2 + СН2ОН-СНОН-СН2ОН.
В щелочной среде молекула уксусного альдегида вступает в окислительно-восстановительную реакцию со второй молекулой, образуя этанол и уксусную кислоту. Одновременно идет накопление глицерина. Суммарно процесс выражается следующим уравнением:
2С6Н12О6 + Н2О ® ® 2СН2ОН-СНОН-СН2ОН + С2Н5ОН + СН3СООН + 2СО2.
Эти приемы используются для промышленного получения глицерина.
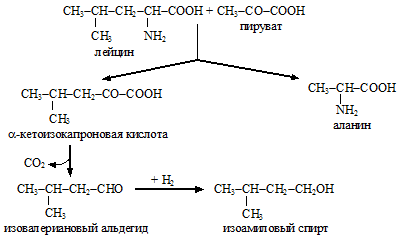
Высшие спирты образуются из аминокислот (в меньшей степени из кетокислот), содержащихся в ферментационной среде, в результате последовательно протекающих реакций дезаминирования аминокислот, декарбоксилирования образовавшихся кетокислот и восстановления альдегидов.
Из высших спиртов в бражке присутствуют: пропиловый (образуется из треонина), изобутиловый (из валина), амиловый (из изолейцина) и изоамиловый (из лейцина).
 |
В настоящее время ведется интенсивный поиск нетрадиционных микроорганизмов-продуцентов этанола, способных сбраживать широкий круг субстратов, имеющих высокую продуктивность по этанолу, обладающих повышенной устойчивостью к этанолу и высокой температуре. Представляют интерес этанолсинтезирующие бактерии. Например, бактерии Zymomonas mobilis отличаются от дрожжей интенсивным метаболизмом: имеют высокую удельную скорость конверсии глюкозы в этанол, обеспечивают более высокий выход этанола (до 95% от теоретически возможного), более толерантны к спирту. Но эти бактерии чувствительны к присутствию в питательных средах ингибиторов (фурфурола, фенолов) и требуют осуществления процесса брожения в условиях асептики.
Термофильные бактерии Clostridium thermocellum (оптимальная температура роста 68°С) способны непосредственно трансформировать целлюлозу растительного сырья в этанол, но при этом сырье должно быть освобождено от лигнина. Достичь высокого выхода спирта при прямой конверсии растительного сырья пока не удается.
Получены штаммы дрожжей, способные сбраживать пентозные сахара (Pachysolen tannophilus, Pichia stipitis, Candida shehata). Выход этанола при сбраживании 100 кг ксилозы достигает 35-47 л.
В отечественной практике производства этанола из крахмалсодержащего сырья используют дрожжи Saccharomyces cerevisiae, имеющие оптимальную температуру брожения 29–30°С.
Ферментативное осахаривание крахмала
Традиционные продуценты этанола не способны к расщеплению полисахаридов, поэтому при получении сусла крахмалсодержащее сырье подлежит развариванию и осахариванию. Крахмал большинства растений содержит 20-25% амилозы и 80-75% амилопектина. В растительных клетках крахмал находится в виде зерен (гранул), размер которых колеблется от 1 до 120 мкм (картофельный крахмал имеет гранулы размером 40-50 мкм, гранулы крахмала зерна − 10-15 мкм). Крахмал, амилоза и амилопектин нерастворимы в холодной воде, спирте, эфире. Амилоза легко растворяется в теплой воде, амилопектин - при нагревании под давлением. Сетчатая структура молекул амилопектина обусловливает набухание крахмальных гранул без их растворения (вторичные связи ослабляются гидратацией). При определенной температуре гранулы разрыхляются, разрываются связи между отдельными структурными элементами, нарушается целостность гранул. При этом резко возрастает вязкость раствора - происходит клейстеризация крахмала. Для клейстера характерны беспорядочное расположение молекул, потеря кристаллической структуры. При температуре 120–130°С клейстер становится легкоподвижным. Наиболее полное растворение амилопектина происходит у пшеничного крахмала при 136–141°С, у картофельного - при 132°С.
Растворенный при разваривании зерна или картофеля крахмал гидролизуют (осахаривают) амилолитическими ферментами зернового солода или культур микроорганизмов, преимущественно мицелиальных грибов и бактерий. Из растительных материалов наиболее богато амилолитическими ферментами пророщенное зерно злаков, называемое солодом. В настоящее время в спиртовой промышленности широко применяют ферментные препараты на основе культур мицелиальных грибов (или бактерий рода Bacillus), которые имеют ряд преимуществ по сравнению с солодом. Культуры мицелиальных грибов выращивают на пшеничных отрубях или кукурузной муке, тогда как для получения солода требуется кондиционное зерно. С солодом в сусло вносятся в большом количестве посторонние микроорганизмы, что отрицательно сказывается на выходе этанола. Глубинные культуры грибов выращивают в стерильных условиях, они не загрязняют сусло посторонними микроорганизмами. Выращивание поверхностной культуры грибов осуществляется намного быстрее (1,5-2,0 сут), чем протекает проращивание зерна (9-10 сут). Грибы образуют комплекс ферментов, которые глубже гидролизуют крахмал, а также расщепляют гемицеллюлозы до моносахаридов, что повышает выход этанола из сырья.
В процессе осахаривания крахмалсодержащего сырья участвуют различные ферменты. Наибольшее производственное значение имеют амилазы. α- и β-амилазы катализируют разрыв только α-1,4-глюкозидных связей. Под действием α-амилаз связи разрываются беспорядочно, но преимущественно внутри цепей. В результате образуются главным образом декстрины, небольшое количество мальтозы и олигосахаридов. Исходя из характера действия, α-амилазу называют эндогенной или декстриногенной амилазой.
Дейстивие β-амилазы направлено на концевые (внешние) связи в крахмале, при этом последовательно, начиная с нередуцирующих концов цепей, отщепляется по два остатка глюкозы (мальтоза). β-амилаза не может обойти места ветвления в макромолекуле крахмала, поэтому гидролиз прекращается на предпоследней α-1,4-глюкозидной связи и остаются высокомолекулярные декстрины при гидролизе амилопектина. Амилоза практически полностью превращается β-амилазой в мальтозу, амилопектин – только на 50–55%.
В результате совместного действия α- и β-амилаз образуется смесь сахаридов, состоящая из мальтозы, небольшого количества глюкозы и низкомолекулярных декстринов, в которых сосредоточены все α-1,6-глюкозидные связи крахмала.
В бактериях и микроскопических грибах отсутствует β-амилаза, но содержится активная α-амилаза, отличающаяся композицией аминокислот в белке и специфичностью действия. В частности, при катализе α-амилазой микроскопических грибов образуется большое количество глюкозы и мальтозы. Среди бактериальных амилаз имеются как сахарогенные, так и декстриногенные. Первые гидролизуют крахмал на 60% и более, вторые – на 30–40%. α-Амилазы микробного происхождения, как и α- и β-амилазы солода, не атакуют α-1,6-глю-козидные связи.
В микроскопических грибах содержится глюкоамилаза, которая катализирует разрыв α-1,4- и α-1,6-глюкозидных связей в крахмале. При катализе этим ферментом от нередуцирующих концов амилозы и амилопектина последовательно отщепляются остатки глюкозы. По месту разрыва связей присоединяется молекула воды, поэтому теоретический выход глюкозы в процессе гидролиза составляет 111,11% к массе крахмала.
Известны три вероятных способа взаимодействия фермента с субстратом (содержащим большое количество цепей): многоцепочный, одноцепочный и комбинированный.
По многоцепочному способу молекула фермента в случайном порядке атакует одну из полисахаридных цепей, отщепляя от нее звено, а затем также в случайном порядке атакует следующие цепи, в том числе, возможно, и атакованную ранее. Таким образом, за время существования фермент-субстратного комплекса происходит только один каталитический акт.
При одноцепочном способе молекула фермента, атаковав в случайном порядке одну из полисахаридных цепей, последовательно отщепляет от нее звенья до полного расщепления цепи. За время существования фермент-субстратного комплекса гидролизуются все доступные для фермента связи.
Комбинированный способ, или способ множественной атаки, заключается в том, что за время существования фермент-субстратного комплекса гидролизуется несколько связей. При этом после отщепления одного звена фермент не отталкивается, а задерживается. Атака происходит с чередованием одно- и многоцепочного способов.
Исследования показали, что α- и β-амилазы осуществляют гидролиз по способу множественной атаки (многоцепочный способ характерен для α-амилазы бактерий).
На отечественных спиртовых заводах для осахаривания крахмала сырья применяют сырцовый (несушенный) солод в виде солодового молока, ферментные препараты (глюкаваморин, амилоризин, амилосубтилин) различного уровня активности или смесь солодового молока и ферментного препарата.
Технология получения солода включает следующие основные процессы: замачивание сырья с достижением влажности 38–40%; проращивание зерна в течение 10 сут в пневматической солодовне в слое толщиной 0,5–0,8 м; измельчение солода в дисковых или молотковых дробилках; дезинфекция солода формалином или раствором хлорной извести и приготовление солодового молока. Солодовое молоко получают смешиванием измельченного солода с водой (4–5 л воды на 1 кг солода).
В солоде, приготовленном из зерна различных злаков, содержится неодинаковое количество каждого из амилолитических ферментов. Например, солод из ячменя имеет высокую α- и β-амилолитическую активность, а солод из проса отличается сильной декстринолитической активностью. Чаще всего готовят смесь из трех видов солода: ячменного (50%), просяного (25%) и овсяного (25%). Запрещается использовать солод из одной культуры при производстве спирта из той же культуры.
|
из
5.00
|
Обсуждение в статье: Ферментативное осахаривание крахмала |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

