 |
Главная |
Влияние ПАВ на поверхностное натяжение воды
|
из
5.00
|
РЕФЕРАТ
По дисциплине: «Химия в строительстве»
на тему: « Поверхностно-активные вещества, используемые в строительстве в строительстве»
Работу выполнил:
студент группы 41-СУ, Сидорова Е.С.
Проверил: к.т.н., доцент Цымай Д. В.
Орел ,2014
Поверхностно-активные вещества (ПАВ) — химические соединения, которые, концентрируясь на поверхности раздела фаз, вызывают снижение поверхностного натяжения.
Применяющиеся в настоящее время синтетические поверхностно-активные вещества (ПАВ) делятся на 4 класса:
· анионные ПАВ – соединения, которые в водных растворах диссоциируют с образованием анионов, обусловливающих поверхностную активность. Среди них наибольшее значение имеют линейный алкилбензосульфонат, сульфаты и сульфоэфиры жирных кислот;
· амфотерные (амфолитные) ПАВ – соединения, которые в водных растворах ионизируются и ведут себя в зависимости от условий (главным образом от рН – среды), т. е. в кислом растворе проявляют свойства катионных ПАВ, а в щелочном растворе – анионных ПАВ. Среди основных амфотерных ПАВ следует отметить алкилбетаины, алкиламинокарбоновые кислоты, производные алкил имидазолинов, алкиламиноалкансульфонаты.
· неионогенные ПАВ – соединения, которые растворяются в воде, не ионизируясь. Растворимость неионогенных ПАВ в воде обуславливается наличием в них функциональных групп. Как правило, они образуют нитраты в водном растворе вследствие возникновения водородных связей между молекулами воды и атомами кислорода полиэтиленгликолевой части молекулы ПАВ. К ним относятся: полигликолевые эфиры жирных спиртов и кислот, полигликолевые эфиры амидов жирных кислот, ацилированные или алкилированные поли гликолевые эфиры алкиламидов.
· катионные ПАВ – соединения, которые в водном растворе диссоциируют с образованием катионов, определяющих поверхностную активность. Среди катионных ПАВ наибольшее значение имеют четвертичные аммониевые соединения, имидазалины, жирные амины.
Влияние ПАВ на поверхностное натяжение воды
При растворении какого-либо вещества в воде поверхностное натяжение её, как правило, изменяется. К примеру, неорганические соли при их растворении в воде несколько повышают величину ее поверхностного натяжения. Вещества, повышающие поверхностное натяжение воды, называют поверхностно-инактивными. На рис. 1 приведены изотермы поверхностного натяжения при повышении концентрации вещества.

Рис. 1. Зависимость поверхностного натяжения(  на границе раствор-газ от равномерной концентрации( С) поверхностно-активного 1 и поверхностно-инактивного 2 вещества (
на границе раствор-газ от равномерной концентрации( С) поверхностно-активного 1 и поверхностно-инактивного 2 вещества (  - поверхностное натяжение воды)
- поверхностное натяжение воды)
Органические вещества( такие как жирные кислоты, соли жирных кислот достаточно большим углеводородным радикалом( содержащим 10-18 углеродных атомов, чаще линейного строения) значительно понижают поверхностное натяжение воды( Рис.1, кривая 1).
Характерной особенностью строения молекул большинства поверхностно- активных веществ является их дифильность, т. е. молекула содержит как гидрофобную часть молекулы( неполярный углеводородный радикал), так и гидрофильную группу( поярную), например, группы- OH;- COOH; -N  ;-SH; -CN; - N
;-SH; -CN; - N  ;- S
;- S  и др.
и др.
Полярные группы (обладающие большим количеством дипольным моментом) обуславливают средство поверхностно- активного вещества к полярным молекулам воды. Радикал, придающий гидрофобные свойства (обычно алифатический или ароматический), является причиной пониженной растворимости ПАВ в воде. Длина углеводородного радикала оказывает значительное влияние на поверхностную активность молекулы (т. е. на способность уменьшать поверхностное натяжение). Так для гомологического ряда предельных жирных кислот поверхностная активность ( на границе раствор - воздух) увеличивается в 3, 2 раза на каждую группу C  / Это можно объяснить тем, что с увеличением длины углеводородной цепи уменьшается растворимость жирной кислоты, и, следовательно, повышается способность ее молекул переходить из объёма в поверхностный слой.
/ Это можно объяснить тем, что с увеличением длины углеводородной цепи уменьшается растворимость жирной кислоты, и, следовательно, повышается способность ее молекул переходить из объёма в поверхностный слой.
 Дифильность молекулы поверхностно-активного вещества принято изображать так :
Дифильность молекулы поверхностно-активного вещества принято изображать так :
 |
где кружок обозначает полярную ( гидрофильную) часть, а черточка- неполярную( гидрофобную) часть молекулы ПАВ. На рис. 2 представлено расположение молекулы ПАВ. На рис. 2 представлено расположение молекул ПАВ в поверхностном слое (водный раствор ПАВ в контакте с воздухом). Если концентрация ПАВ мала, то немного его молекул и в поверхностном слое (рис. 2, а). При увеличении концентрации ПАВ молекулы располагаются перпендикулярно поверхности воды, образуя мономолекулярный, а иногда и полимолекулярный слой, включая и коллоидную систему, также возможен перевод водного раствора в эмульсию, пену, суспензию.
Рис. 2. Расположение молекул ПАВ в поверхностном слое: а) концентрация молекул ПАВ мала; б) молекулы ПАВ образовали мономолекулярный слой - концентрация молекул ПАВ достаточно велика
Если рассматривать адсорбцию ПАВ на твердой поверхности , то наблюдается картина, аналогичная представленной на рис.2. Например, к неполярной поверхности угля на границе с водой обращен неполярный углеводородный радикал молекулы ПАВ ,а полярная группа ориентирована к воде ( рис. 3, а).
К полярной поверхности, например, силикагеля, на границе с бензолом молекулы ПАВ ориентированы своей полярной группой, неполярный радикал обращен к неполярному растворителю - бензолу (рис. 3, б).

Рис. 3. Расположение молекул ПАВ на границе раздела фаз разной природы
Связь между концентрацией ПАВ в растворе ( с), избытком адсорбированного вещества в поверхностном слое (Г) и поверхностным натяжением (  ) на границе водный раствор - воздух описывается уравнением адсорбции Гиббса:
) на границе водный раствор - воздух описывается уравнением адсорбции Гиббса:
 ,
,
в предположении, что раствор близок к идеальному, и коэффициент активности может быть принят равным единице.
Количественной мерой адсорбции i-го компонента служит, по Гиббсу, величина  . Также называемая адсорбцией и определяемая как избыток (обычно в моль) рассматриваемого компонента, приходящийся на единицу площади поверхности раздела фаз:
. Также называемая адсорбцией и определяемая как избыток (обычно в моль) рассматриваемого компонента, приходящийся на единицу площади поверхности раздела фаз:
 ,
,
Где,
 - общее число моль i-го компонента в системе ;
- общее число моль i-го компонента в системе ;
 и
и  - число моль того же компонента в каждой из двух соприкасающихся фаз в предположении, что его концентрация в фазах остаются постоянными вплоть до геометрической разделяющей поверхности площадью S.
- число моль того же компонента в каждой из двух соприкасающихся фаз в предположении, что его концентрация в фазах остаются постоянными вплоть до геометрической разделяющей поверхности площадью S.
Если поверхностное натяжение  уменьшается с увеличением концентрации с, т. е.
уменьшается с увеличением концентрации с, т. е.  0, то величина Г
0, то величина Г  0 и концентрация растворенного вещества в поверхностном слое больше объемной концентрации. Если же
0 и концентрация растворенного вещества в поверхностном слое больше объемной концентрации. Если же 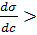 0, т.е. поверхностное натяжение увеличивается с увеличением концентрации с, то величина Г
0, т.е. поверхностное натяжение увеличивается с увеличением концентрации с, то величина Г  0, т.е. концентрация растворенного вещества в поверхностном слое меньше, чем в объеме (рис. 1, кривая 2).
0, т.е. концентрация растворенного вещества в поверхностном слое меньше, чем в объеме (рис. 1, кривая 2).
Зависимость поверхностного натяжения растворов поверхностно-активных веществ от температуры изучалась П. А. Ребиндером. При повышении температуры поверхностное натяжение индивидуальных жидкостей уменьшается. Поверхностное натяжение растворов некоторых поверхностно-активных веществ с повышением температуры может изменяться по кривой с максимумом (рис. 4).Максимум объясняется десорбцией поверхностно-активного вещества в определенном интервале температур.

Рис. 4. Зависимость поверхностного натяжения  от температуры t;1- индивидуальная жидкость (вода); 2- раствор поверхностно-активного вещества
от температуры t;1- индивидуальная жидкость (вода); 2- раствор поверхностно-активного вещества
|
из
5.00
|
Обсуждение в статье: Влияние ПАВ на поверхностное натяжение воды |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

