 |
Главная |
Поверхностные явления
|
из
5.00
|
Все высокодисперсные системы имеют очень большую площадь поверхности раздела фаз. Согласно уравнению G = σ ∙ S, они обладают большим избытком поверхностной энергии Гиббса. По второму началу термодинамики, такие системы термодинамически неустойчивы. Они стремятся самопроизвольно уменьшить эту энергию и перейти в устойчивое равновесное состояние с минимальным значением энергии Гиббса.
Самопроизвольные процессы в дисперсных системах, идущие с уменьшением избыточной поверхностной энергии, называются поверхностными явлениями.
Согласно уравнению (1.1), энергия Гиббса может быть уменьшена либо за счет уменьшения σ, либо за счет уменьшения S. Поэтому существует два вида поверхностных явлений:
а) идущих за счет уменьшения площади поверхности, ΔS<0, σ = const: коагуляция, коалесценция, спекание порошков, конденсация мелких капель в крупные.
б) идущих за счет уменьшения поверхностного натяжения Δσ < 0, а S=const – это все виды сорбции: адсорбция, абсорбция, смачивание.
Сорбция. Адсорбция.
Сорбцией называют процесс поглощения одного вещества другим веществом. Из многих явлений сорбции наибольшее медико-биологическое значение имеет адсорбция.
Адсорбция(“ад”- на) – самопроизвольный процесс накопления какого-либо вещества на поверхности раздела фаз, ведущий к уменьшению поверхностного натяжения, а значит и уменьшению избыточной поверхностной энергии.
Обратный процесс удаления с поверхности адсорбированного вещества называют десорбцией. Вещество, на поверхности которого идет адсорбция, называется адсорбентом (уголь в противогазе), а адсорбированное вещество – адсорбатом (поглощенный из воздуха углем хлор или аммиак). Проникновение адсорбированного вещества в глубь адсорбента называют абсорбцией («аб» - в). Абсорбцией является растворение газов в жидкости. Терминология адсорбции видна из рисунка 1.3. Адсорбция всегда ведет к уменьшению поверхностного натяжения, а значит и уменьшению избыточной поверхностной энергии. Система становится более устойчивой.

|
Физическая и химическая адсорбция.
В зависимости от природы химических связей, которыми адсорбат удерживается на поверхности адсорбента, различают два вида сорбции: физическую и химическую.
При невысоких температурах обычно имеют место оба вида адсорбции, а при высоких – преобладает хемосорбция.
| |||
| |||
Изотерма адсорбции
Адсорбцию количественно обозначают буквой Г (гамма). Это количество вещества адсорбата, накопленного на единице площади поверхности адсорбента, Г, моль/м2. Для твердых адсорбентов из-за трудности определения площади поверхности адсорбцию измеряют в моль/г.
Адсорбция зависит от многих факторов: от природы адсорбата и адсорбента, температуры, концентрации адсорбата. Зависимость адсорбции от концентрации адсорбата при постоянной температуре называют изотермой адсорбции. Эта зависимость может быть выражена математически или графически. Наиболее типичной изотермой адсорбции является изотерма Лэнгмюра. (рис 1.4)
|
 .
.
1.8. Адсорбция из раствора на поверхности раздела «газ-жидкость» 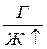 .
.
Для дисперсной системы газ – чистый растворитель единственной возможностью самопроизвольного уменьшения избыточной поверхностной энергии является уменьшение площади поверхности. Например, конденсация мелких капелек тумана в более крупные капли дождя.
Для растворов есть еще одна возможность уменьшения G – это уменьшение поверхностного натяжения за счет адсорбции из раствора на поверхности раздела фаз растворенного вещества. Растворенные вещества по-разному влияют на поверхностное натяжение жидкости (рис.1.5.). Существуют вещества, которые не изменяют поверхностное натяжение жидкости (например, сахароза в воде); их называют поверхностно-неактивными, ПНВ.
Вещества, увеличивающие поверхностное натяжение, называют поверхностно инактивными, ПИВ. Это сильные электролиты. Силы взаимодействия между их ионами выше, чем между молекулами растворителя.
|
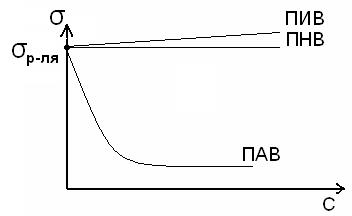
Особое значение имеют вещества, уменьшающие поверхностное натяжение жидкости.
Вещества, самопроизвольно адсорбирующиеся из раствора на поверхности раздела фаз и уменьшающие поверхностное натяжение (а значит и избыточную поверхностную энергию), называются поверхностно-активными веществами, ПАВ.
Молекулы ПАВ имеют особое «дифильное» строение. Их принято изображать в виде «головастиков». Они имеют неполярный гидрофобный
хвост и полярную гидрофильную головку, R-X. Неполярный хвост – это чаще всего углеводородный радикал.


|
из
5.00
|
Обсуждение в статье: Поверхностные явления |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

