 |
Главная |
Термодинамика реакций восстановления бора
|
из
5.00
|
ГЛАВА 17. ЭЛЕКТРОМЕТАЛЛУРГИЯ
ФЕРРОБОРА И КАРБИДА БОРА
Свойства бора и его соединений
Бор элемент ІІІ группы элементов Периодической системы Д.И.Менделеева. Порядковый номер бора 3, атомная масса 10, 811, температура плавления 2074°С, температура кипения 3658оС, конфигурация внешней электронной оболочки 2s22p, степень окисления 3. Известно более 10 аллотропных модификаций бора. Природный бор состоит из двух стабильных изотопов  В (19,57%) и
В (19,57%) и  В (80,43%). Поперечное сечение захвата тепловых нейтронов
В (80,43%). Поперечное сечение захвата тепловых нейтронов  В 3×10-25 м2,
В 3×10-25 м2,  В 4×10-32 м2. Стандартная энтропия бора S
В 4×10-32 м2. Стандартная энтропия бора S  = 5,85 Дж/(моль×K).
= 5,85 Дж/(моль×K).
Система В–Fe (рис. 17.1). Бор с железом образует соединения – бориды Fe2B, FeB и FeB2. Некоторые свойства боридов железа приведены в табл. 17.1.
Рис. 17.1. Диаграмма равновесного состояния системы Fe–B
Таблица 17.1. Некоторые свойства боридов железа
| Борид железа | В, % | Тпл,. K | r, г/см3 | –∆Н  , Дж/моль , Дж/моль
|
| Fe2B | 8,79 | 6,98 | ||
| FeB | 16,17 | 6,47 | ||
| FeB2 | 27,83 | 5,00 | – |
Борид Fe2B плавится инконгруэнтно при 1389°С, а борид FeB2 – конгруэнтно при ~ 1550°С. Бориды железа – термодинамически прочные химические соединения. Энтальпия образования ∆Н  = –71,06 кДж/моль, энтропия S
= –71,06 кДж/моль, энтропия S  = 56,59 Дж/(моль×K). Растворение бора в жидком железе сопровождается выделением большого количества тепла (см. табл. 17.1).
= 56,59 Дж/(моль×K). Растворение бора в жидком железе сопровождается выделением большого количества тепла (см. табл. 17.1).
Парциальные и интегральные энтальпии образования жидких сплавов бора с железом приведены ниже (при 1680°С, в кДж/моль):
| XВ | –∆ 
| –∆ 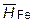
| –∆Н |
| 73,23 | |||
| 0,1 | 74,12 | 0,01 | 7,42 |
| 0,3 | 58,03 | 4,99 | 20,90 |
| 0,5 | 7,93 | 39,29 | 23,60 |
Система В–С (рис. 17.2). В этой системе образуются карбид В4С, имеющий широкую концентрационную область гомогенности. Теплота образования карбида В4С из элементов ∆Н  = –71,48 кДж/моль, стандартная энтропия S
= –71,48 кДж/моль, стандартная энтропия S  = 27,08 Дж/(моль×K), что свидетельствует о его термодинамической прочности. Температура плавления карбида бора ~2450°С.
= 27,08 Дж/(моль×K), что свидетельствует о его термодинамической прочности. Температура плавления карбида бора ~2450°С.
Система В–Si (рис. 17.3). Бор с кремнием образует термодинамически прочные соединения – силициды бора SiB3, SiB6 и SiBn. Силицид SiB6 плавится инконгруэнтно при 1850°С.
Система В–Al (рис.17.4). Известны алюминиды бора AlB2, AlB10 и AlB12. Алюминид AlB2 плавится инконгруэнтно при 960°С, а AlB12 – конгруэнтно при 2150°С. Cоединение AlB10 существует в узком температурном интервале 1660–1850оС.
Рис. 17.2. Диаграмма равновесного состояния системы В–С
Рис. 17.3. Диаграмма равновесного состояния системы В–Si
Система В–О. В системе В–О известен ряд оксидов с различным отношением В:О, от 7 : 1 до 4 : 5. Термически наиболее устойчивым является В2О3. Температура плавления В2О3 равна 450°С. Взаимодействие бора с молекулярным кислородом, описывается реакцией:
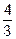 В + О2 =
В + О2 = 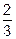 В2О3; ∆G
В2О3; ∆G 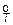 = –847146 + 144,3Т, Дж/моль.
= –847146 + 144,3Т, Дж/моль.
Рис. 17.4.Диаграмма равновесного состояния системы В–Al
Давление пара В2О3 зависит от температуры, и эта связь описывается уравнением:
lgPобщ (Па) = -19000/Т + 12,771.
Теплота сублимации В2О3; ∆Н  = 375,14 кДж/моль.
= 375,14 кДж/моль.
Минералы и руды бора
Основные минералы бора: борацит – (Mg,Fe,Mn)3[ClB2O3], ссайбелиит (ашарит) - Mg2[B2O5]×H2O, колеманит – Ca[B3O4(OH)3], кернит – Na2[B4O6(OH)2]∙3H2O, бура – Na2[B4O7(OH)4]∙8H2O.
Руды Индерского месторождения имеют следующий состав, %: 8–30 В2О3; 1,5–13 SiO2; 15–25 CaO; 10–30 MgO; 2–5 FeO; 2–6 Na2O; 2–3 C; 5–10 S; ≤0,01 Р. Из этой руды получают концентраты, борную кислоту (Н3ВО3), борный ангидрит (В2О3), диборат кальция (СаО∙В2О3∙2Н2О), октаборат натрия (Na2B8O13) и выплавляют ферроборал и ферросиликоборал. В табл. 17.2 приведен химический состав рудных концентратов, применяемых для выплавки сплавов бора. При получении богатых лигатур используют чистый (>98 % В2О3) и технический ангидрид.
Таблица 17.2. Химический состав, %, концентратов борсодержащих материалов
| Наименование | В2О3, не менее | СаО | MgO | SiO2 | Fe2O3 | Na2O | H2O |
| не более | |||||||
| Борный ангидрид | 95,0 | – | – | – | 0,0065 | – | 3–5 |
| Диборат кальция (СаО∙В2О3∙2Н2О) | 38,0 | 35,6 | 2,0 | 0,04 | 0,1 | ||
| Борная кислота (Н3ВО3) | 99,5 | – | – | 0,8 | 0,0065 | – | – |
| Октаборат натрия (Na2B8O13) | 74,0 | – | – | 1,0 | – | 23,0 | – |
Термодинамика реакций восстановления бора
Восстановление бора углеродом. Реакция взаимодействия В2О3 с углеродом с получением чистого бора имеет вид:
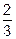 В2О3 + 2С =
В2О3 + 2С = 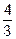 В + 2СО;
В + 2СО;
∆G 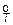 = 661890 – 346,3Т, Дж/моль.
= 661890 – 346,3Т, Дж/моль.
Теоретическая температура начала реакции (т.е. условие ∆G 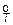 = 0 и РСО = 101 кПа) равна 1926 K. Термодинамически вероятна реакция взаимодействия В2О3 с углеродом с образованием карбида В4С
= 0 и РСО = 101 кПа) равна 1926 K. Термодинамически вероятна реакция взаимодействия В2О3 с углеродом с образованием карбида В4С
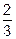 В2О3 +
В2О3 +  С =
С = 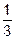 В4С + 2СО;
В4С + 2СО;
∆G 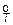 = 579350 – 314,3Т, Дж/моль.
= 579350 – 314,3Т, Дж/моль.
Теоретическая температура начала реакции равна 1843 K. Таким образом, реакция восстановления В2О3 до карбида В4С термодинамически более предпочтительна.
Восстановление бора кремнием. Силикотермическое восстановление бора по реакции
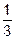 В2О3 + Si =
В2О3 + Si = 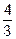 B + SiO2;
B + SiO2;
∆G 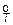 = –10376 + 32,93Т Дж/моль
= –10376 + 32,93Т Дж/моль
характеризуется получением бора с большим содержанием кремния и поэтому не может рассматриваться как основа для выплавки чистого бора.
Восстановление бора алюминием. Реакция восстановления бора из В2О3 алюминием
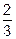 В2О3 +
В2О3 + 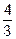 Al =
Al = 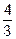 B +
B + 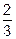 Al2O3
Al2O3
∆G 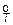 = –216370 + 32,93Т, Дж/моль
= –216370 + 32,93Т, Дж/моль
имеет наибольшую из рассмотренных термодинамическую предпочтительность.
|
из
5.00
|
Обсуждение в статье: Термодинамика реакций восстановления бора |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

