 |
Главная |
Практическая работа №1. Основные законы химии Название закона Формулировка закона Автор
|
из
5.00
|
Основные законы химии
| Название закона | Формулировка закона | Автор, год открытия | Примечание |
| Закон сохранения массы | Масса веществ, вступивших в реакцию, равна массе веществ, образовавшихся в результате реакции | М.В.Ломоносов, 1748р. (русский учёный) А.Л.Лавуазье, 1789р. (французский учёный) | При реакции остаётся постоянной не только общая масса вещества, но и масса каждого из взаимодействующих элементов. |
| Закон эквивалентности массы и энергии | Изменению массы на величину ∆m соответствует в целом определённое изменение энергии | А. Эйнштейн (немецкий физик) | Е = m·c2, де с – скорость света. |
| Закон кратных отношений | Если два элемента образуют друг с другом несколько соединений молекулярного строения, то одинаковому количеству одного из них соответствуют такие количества другого, соотносящиеся между собой как небольшие целые числа. | Дж. Дальтон, 1803р. (английский учёный) | В СО і СО2 одной массовой части углерода С соответствуют разные массовые части кислорода О, которые соотносятся между собой как 1 : 2 |
| Закон простых объемных отношений | При одинаковых условиях вступающие в реакцию газы относятся другу к другу, а также к объёмам газообразных продуктов реакции как небольшие целые числа. | Гей-Люссак, 1808р. (французский учёный) | При взаимодействии 2 объёмов водорода и одного объёма кислорода образуется 2 объёма водяного пара. 2Н2 + О2 → 2Н2О |
| Закон Авогадро | В одинаковых объёмах разных газов, находящихся при одинаковых условиях (температуре и давлении), содержится одинаковое число молекул. | А.Авогадро, 1811р. (итальянский физик) | 

|
| Закон постоянства состава вещества | Любое химически чистое вещество имеет одинаковый качественный и количественный состав независимо от способа получения. | Ж.Л.Пруст, 1789р. (французский учёный) | Малахит, добытый в Сибири и в Испании, имеет одинаковый состав |
| Закон эквивалентов | Химические элементы соединяются друг с другом, а вещества реагируют между собой в количествах, пропорциональных их эквивалентам. | И. Рихтер, 1792-1794р.р. (немецкий учёный) | 

|
Закон постоянства состава способствовал введению в химию понятий «эквивалент», «молярная масса эквивалента».
Эквивалентом элемента называют такое его количество, которое соединяется с 1 молем атомов Водорода, или замещает такое же самое количество атомов Водорода в химических реакциях.
Масса одного эквивалента элемента называется эквивалентной массой.
Например, в соединениях НF, Н2О, NH3 эквиваленты Фтора, Кислорода и Азота равны 1, 1/2, 1/3 моль, а молярные массы эквивалентов соответственно 18,99; 8; 4,67.
Стехиометрическая валентность: В =  ,
,
де М – молярная масса вещества;
Мекв – молярная масса эквивалента
Эквивалент элемента можно рассчитать двумя способами:
- Прямой метод (по составу соединения этого элемента с любым другим элементом с известным эквивалентом).
ЕА ‑ q
ЕВ ‑ (m ‑ q) отсюда, 
- Метод вытеснения. Расчет проводят по водороду. Учитывают массу металла, вытесняющего водород с воды, кислоты или щёлочи и массу вытесненного водорода.
Эквивалент химического элемента рассчитывают по формуле:  ,
,
де m – масса вытесненного водорода, г; q – масса взятого металла, г.
Если в реакции принимают участие газообразные вещества, то используют понятие эквивалентный объём (объём, который занимает при данных условиях 1 эквивалент газообразного вещества).
При нормальных условиях эквивалентный объём водорода равен 11,2л, эквивалентный объём кислорода – 5,6л.
Задачи для решения:
- Определить эквивалентную массу Азота в кислородсодержащих соединениях следующего состава: а) N2O; б)NO; в) N2O3; г) NO2; д) N2O5. (Ответ: а)14 г/моль; б) 7 г/моль; в) 4,67г/моль; г) 3,5г/моль; д) 2,8 г/моль)
- Соединение элемента Х с кислородом содержит 60% данного элемента. Вычислить его эквивалентную массу. (Ответ: 12 г/моль)
- Вычислить эквивалентную массу металла, 1 г которого вытесняет из кислоты 700мл водорода, измеренного при н.у. (Ответ: 16 г/моль)
- Вычислить эквивалентную массу металла, 1 г оксиду которого образует 1,81 г сульфата этого металла. (Ответ: 100,6 г/моль)
- Вычислить эквивалентную массу Нg, если из 1г её оксида при нагревании выделяется 51,7мл кислорода. (Ответ: 100,3 г/моль)
- Хлорид металла содержит 31% металла с атомной массой 47,9. Вычислить валентность металла. (Ответ: 3)
- Оксид шестивалентного элемента содержит 48% Кислорода. Вычислить атомную массу элемента. (Ответ: 52 а.о.м.)
- При пропускании сероводорода через раствор, содержащий 1,35г хлорида металла, образуется 0,96г его сульфида. Вычислить эквивалентную массу металла. (Ответ: 32 г/моль)
- Вычислить эквивалентную массу металла, если из 1,85г гидроксида образуется 2,5г карбоната. (Ответ: 20 г/моль).
þ Эквивалентом сложного вещества называется условная частичка этого вещества, которая в данной реакции соединяется с одним атомом или ионом Водорода, или замещает его.
Реакция: 2НСІ + Са(ОН)2 → СаСІ2 + 2Н2О
Двум атомам Водорода в НСІ соответствует одна часть Са(ОН)2 (одному атому Н эквивалентна условная частица, равная ½ Са(ОН)2).
Эквивалент вещества кислоты или основания изменяется и зависит от реакции, в которой это вещество принимает участие.
þ Число, показывающее какая часть реальной частички вещества Х эквивалентна одному иону водорода в данной кислотно-основной реакции, называется фактором эквивалентности вещества Х.Обозначается fекв (Х), величина безразмерной.
fекв (Са (ОН)2) = ½, а fекв (НСІ) = 1
Фактор эквивалентности отдельных веществ можно рассчитать по формулам:
Для кислоты фактор эквивалентности равен обратной величине основности (число ионов Н+ в молекуле кислоты, которые замещаются в реакции на метал):
fекв (кислоты) = 1/N (H+)
fекв (НNO3) = 1; fекв (Н2СО3) = ½; fекв (Н3РО4) = 1/3.
Для основания фактор эквивалентности равен обратной величине кислотности (число ионов ОН- в молекуле основания, которые замещаются в реакции на метал):
fекв (основания) = 1/N (ОH-)
fекв (Zn (ОН)2) = ½; fекв (КОН) = 1; fекв (АІ (ОН)3) = 1/3; fекв (Pb(ОН)4) = ¼.
Фактор эквивалентности в реакциях обмена определяют в зависимости от стехиометрии реакции (от образованного продукта):
H2SO4 + NaOH → NaHSO4 + H2O,
fекв(H2SO4) =1 (в реакции – замещение 1 катиона водорода на катион натрия.
H2SO4 + 2NaOH → Na2SO4 + 2H2O,
fекв(H2SO4)= 1/2 (в реакции – замещение 2-х катионов водорода на катионы натрия).
þ Величина fекв(Х)Х называется эквивалентом вещества Х,или эквивалентной формой Х и является общей формой обозначения всех частичек, реагирующих в кислотно-основных реакциях.
Форма записи эквивалента серной кислоты:
fекв(H2SO4)H2SO4) = H2SO4
для реакции: H2SO4 + NaOH → NaHSO4 + H2O;
fекв(H2SO4)H2SO4) = ½ H2SO4
для реакции: H2SO4 + 2NaOH → Na2SO4 + 2H2O.
Фактор эквивалентности вещества в кислотно-основных реакциях может равняться 1 или быть меньше 1: fекв(Х)<1.
Для эквивалентов как условных частиц можно вычислить молярную массу и количество вещества.
þ Молярная масса эквивалентаfекв(Х)Х – это масса одного моля вещества эквивалента fекв(Х)Х.
Молярная масса вещества эквивалента равна произведению фактора эквивалентності fекв(Х) на молярную массу вещества Х.
Форма записи молярной массы вещества эквивалента fекв(Х)Х:М(fекв(Х)Х)и рассчитывается по формуле:
М(fекв (Х)Х) = fекв (Х) ∙ М(Х);
М(fекв (H2SO4)H2SO4) = fекв (H2SO4) ∙M(H2SO4).
· Для реакции (1): М(fекв(H2SO4)H2SO4) = 1∙ 98 = 98г/моль;
· Для реакции (2): М(fекв(H2SO4)H2SO4) = ½ ∙98 = 49г/моль;
М(1/2 H2SO4) = ½ ∙ 98 = 49 г/моль.
Фактор эквивалентности показывает во сколько раз молярная масса эквивалента данного вещества меньше, чем её молярная масса.
М(fекв (НСІ)НСІ) = М(НСІ)·1 = 36,46·1 = 36,46г/моль → М(fекв (НСІ)НСІ) = М(НСІ)
М(fекв(H3PO4)H3PO4) = 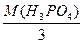 =
= 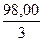 = 32,66г/моль → М(1/3 H3PO4)
= 32,66г/моль → М(1/3 H3PO4)
М(fекв(MgO)MgO) =  =
= 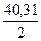 = 20,16г/моль → М(1/2 MgO)
= 20,16г/моль → М(1/2 MgO)
М(fекв(Ca(OH)2)Ca(OH)2) =  =
=  = 37,05г/моль → М(1/2 Ca(OH)2)
= 37,05г/моль → М(1/2 Ca(OH)2)
М(1/6 Fe2(SO4)3) =  =
=  = 66,65г/моль
= 66,65г/моль
Вывод: молярная масса вещества эквивалента меньше молярной массы данного вещества в то количество раз, что соответствует фактору эквивалентности.
þ Количество вещества эквивалента –это количество вещества (в молях), которое состоит из эквивалентов (fекв(Х)Х). Единицей количества вещества эквивалента есть моль.
Форма записи количества вещества эквивалента: n ( fекв (Х)Х).
Вычислить количество вещества эквивалента можно по формуле:
n( fекв (Х)Х )= 
Связь молярной массы вещества эквивалента, количества вещества эквивалента с массой вещества m (Х) выражается:
m (Х) = 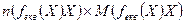 ,
,
Отсюда, количество вещества эквивалента равно:
 ;
;
Согласно закону эквивалентов: все вещества взаимодействуют в одинаковых количествах вещества эквивалента.
Задачи для решения:
- Вычислить количество вещества эквивалента гидроксида кальция, если масса Са(ОН)2 равна 2,3 г. (Ответ: 0,06 моль)
- Фактор эквивалентности серной кислоты в реакции с гідроксидом натрия равен ½. Какая масса гидроксида необходима для реакции с кислотой массой 19,6г ? (Ответ: 16 г)
- Серная кислота массой 4,9 г прореагировала с гідроксидом калия массой 2,8 г. Вычислить молярную массу вещества эквивалента серной кислоты и написать уравнение реакции. (Ответ: 98 г/моль, fекв(H2SO4) =1, образуется кислая соль)
Эквивалент вещества, фактор эквивалентности, молярная масса эквивалента в окислительно-восстановительных реакциях отличаются от их значений в реакциях обмена.
þ Эквивалент окислителя или восстановителя – условна часть вещества, которая в данной окислительно-восстановительной реакции эквивалентна одному полученному или отданному электрону одной молекулой вещества.
Число, показывающее количество отданных иди принятых электронов одним атомом, ионом или молекулой, называется фактором эквивалентности (fекв).
Для вычисления фактора эквивалентности и молярной массы эквивалента нужно:
ü написать уравнение окислительно-восстановительной реакции;
ü составить электронный баланс;
ü по количеству электронов, отданных или присоединённых одной молекулой (ионом), определить фактор эквивалентности fекв;
ü вычислить молярную массу эквивалента окислителя и восстановителя:

Практическая работа №1
Тема:Вычисление молярных масс эквивалентов веществ
Вариант № 1
- Рассчитайте молярную массу эквивалента для следующих веществ: НNO3, NaOH, Ca(OH)2, AICI3, CuSO4, Fe2(SO4)3.
- Чему равна молярная масса эквивалента сернистой кислоты в реакциях: а) полной нейтрализации; б) неполной нейтрализации.
- Вычислить молярную массу эквивалента окислителя и восстановителя в реакции:
H2S + KMnO4 + H2SO4 ® S + MnSO4 + K2SO4 + H2O
- Вычислить эквивалентную массу металла, если из 1,85г гидроксида образуется 2,5г карбоната.
|
из
5.00
|
Обсуждение в статье: Практическая работа №1. Основные законы химии Название закона Формулировка закона Автор |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

