|
Главная |
Ковалентная связь. Полярная и неполярная ковалентные связи
|
из
5.00
|
КОВАЛЕНТНАЯ СВЯЗЬ -это связь, возникающая между атомами за счет образования общих электронных пар (Например, H2, HCl, H2O, O2).
По степени смещенности общих электронных пар к одному из связанных ими атомов ковалентная связь может быть полярной и неполярной.
А) КОВАЛЕНТНАЯ НЕПОЛЯРНАЯ СВЯЗЬ (КНС) -образуют атомы одного и того же химического элемента - неметалла (Например, H2, O2, О3).
Механизм образования связи.
Каждый атом неметалла отдает в общее пользование другому атому наружные не спаренные электроны. Образуются общие электронные пары. Электронная пара принадлежит в равной мере обоим атомам.
Рассмотрим механизм образования молекулы хлора:
Cl2 – кнс.
Электронная схема образования молекулы Cl2:
 Структурная формула молекулы Cl2:
σ
Cl – Cl , σ (p – p) - одинарная связь
Структурная формула молекулы Cl2:
σ
Cl – Cl , σ (p – p) - одинарная связь
 Демонстрация образования молекулы водорода
Рассмотрим механизм образования молекулы кислорода:
О2 – кнс.
Электронная схема образования молекулы О2:
Демонстрация образования молекулы водорода
Рассмотрим механизм образования молекулы кислорода:
О2 – кнс.
Электронная схема образования молекулы О2:
 Структурная формула молекулы О2:
σ
О = О
π
В молекуле кратная, двойная связь:
Одна σ (p – p)
Структурная формула молекулы О2:
σ
О = О
π
В молекуле кратная, двойная связь:
Одна σ (p – p)
 и одна π (р – р)
и одна π (р – р)
 Демонстрация образования молекул кислорода и азота
Б) КОВАЛЕНТНАЯ ПОЛЯРНАЯ СВЯЗЬ (КПС) -образуют атомы разных неметаллов, отличающихся по значениям электроотрицательности (Например, HCl, H2O).
Встречаются исключения, когда ковалентную связь образуют атом неметалла и металла!
Например, AlCl3, разница в электроотрицательности ∆ Э.О.<1.7, т.е. ∆ Э.О.= 3,16 (Cl) – 1,61(Al) = 1,55
Электроотрицательность (ЭО) - это свойство атомов одного элемента притягивать к себе электроны от атомов других элементов.
Самый электроотрицательный элемент – фтор F
Электроотрицательность можно выразить количественно и выстроить элементы в ряд по ее возрастанию. Наиболее часто используют ряд электроотрицательности элементов, предложенный американским химиком Л. Полингом.
Таблица. Электроотрицательности (ЭО) некоторых элементов (приведены в порядке возрастания ЭО).
Демонстрация образования молекул кислорода и азота
Б) КОВАЛЕНТНАЯ ПОЛЯРНАЯ СВЯЗЬ (КПС) -образуют атомы разных неметаллов, отличающихся по значениям электроотрицательности (Например, HCl, H2O).
Встречаются исключения, когда ковалентную связь образуют атом неметалла и металла!
Например, AlCl3, разница в электроотрицательности ∆ Э.О.<1.7, т.е. ∆ Э.О.= 3,16 (Cl) – 1,61(Al) = 1,55
Электроотрицательность (ЭО) - это свойство атомов одного элемента притягивать к себе электроны от атомов других элементов.
Самый электроотрицательный элемент – фтор F
Электроотрицательность можно выразить количественно и выстроить элементы в ряд по ее возрастанию. Наиболее часто используют ряд электроотрицательности элементов, предложенный американским химиком Л. Полингом.
Таблица. Электроотрицательности (ЭО) некоторых элементов (приведены в порядке возрастания ЭО).
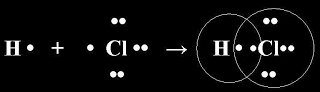
Механизм образования связи. Каждый атом неметалла отдает в общее пользование другому атому свои наружные не спаренные электроны. Образуются общие электронные пары. Общая электронная пара смещена к более электроотрицательному элементу. Рассмотрим механизм образования молекулы хлороводорода: НCl – кпс. Электронная схема образования молекулы НCl: Структурная формула молекулы НCl: σ Н → Cl , σ (s – p) - одинарная связь σ, смещение электронной плотности в сторону более электроотрицательного атома хлора (→) |
Ионная связь
ИОННАЯ СВЯЗЬ (ИС) – образуется между атомами металлов и неметаллов, т.е. между атомами, резко отличающимися друг от друга по значениям электроотрицательности. (Например, NaCl, K2O, LiF)
Механизм образования связи.
Атом неметалла забирает наружные электроны у атома металла и превращается в анион (отрицательно заряженный ион). Атом металла теряет электроны и превращается в катион (положительно заряженный ион). Ионы связаны электростатическими силами. Происходит полная отдача (принятие) валентных электронов, перекрывание облаков отсутствует, обобществления электронов не наблюдается.
Ионы
Рассмотрим механизм образования молекулы фторида натрия:
NaF – ис.
Электронная схема образования молекулы NaF:
В результате образования связи электронная пара полностью сместилась к атому фтора, разноименно заряженные иона натрия и фтора притягиваются за счёт электростатического взаимодействия. Пример, механизм образования хлорида натрия |
|
из
5.00
|
Обсуждение в статье: Ковалентная связь. Полярная и неполярная ковалентные связи |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы