 |
Главная |
Изменение электролизом веществ
|
из
5.00
|
| Катодные процессы (К-) | |||
| Катионы активных металлов | Катионы менее активных металлов | Катионы неактивных металлов | |
| Li+, Cs+, Rb+, K+, Ba2+, Sr2+, Ca2+, Na+, Mg2+, Be2+, Al3+ | Mn2+, Cr3+, Zn2+, Ga3+, Fe2+, Cd2+, In3+, Tl+, Co2+, Ni2+, Mo4+, Sn2+, Pb2+ | Bi3+, Cu2+, Ag+, Hg2+, Pd3+, Pt2+, Au3+ | |
| Тяжело разряжаются (только из расплавов), в водном растворе электролизу подвергается вода с выделением водорода расплав Na+ + 1e = Na0 раствор 2H2O + 2e = H2 + 2OH− | В водном растворе восстанавливается металл (при малой концентрации катионов в растворе — металл и водород) Zn2+ + 2e = Zn0 2H2O + 2e = H2 + 2OH− | Легко разряжаются и восстанавливается только металл Cu2+ + 2e = Cu0 | |
| Анодные процессы (А+) | |||
| Анионы кислородсодержащих кислот и фторид-ион | Гидроксид-ионы; анионы бескислородных кислот (кроме F−) | ||
| PO43−, CO32−, SO42−, NO3−, NO2−, ClO4−, F− | OH−, Cl−, Br−, I−, S2− | ||
| Тяжело разряжаются (только из расплавов), в водном растворе электролизу подвергается вода с выделением кислорода расплав 2SO42− −4e =2SO3+O2 раствор 2H2O — 4e = O2 + 4H+ | Легко разряжаются Cl− — 1e = Cl0; Cl0+Cl0=Cl2 4OH− −4e =2H2O + O2 | ||
| Расплавы | Растворы |
| 1) Активные металлы 1.Соль активного металла и бескислородной кислоты NaCl ↔ Na+ + Cl− K"катод"(-): Na+ + 1e = Na0 A"анод"(+): Cl− — 1e = Cl0; Cl0+Cl0=Cl2 Вывод: 2NaCl → (электролиз) 2Na + Cl2 2.Соль активного металла и кислородосодержащей кислоты Na2SO4↔2Na++SO42− K(-): 2Na+ +2e =2Na0 A(+): 2SO42− −4e =2SO3+O2 Вывод: 2Na2SO4 → (электролиз) 4Na + 2SO3 + O2 3. Гидроксид: активный металл и гидроксид-ион NaOH ↔ Na+ + OH− K(-): Na+ +1e =Na0 A(+): 4OH− −4e =2H2O + O2 Вывод: 4NaOH → (электролиз) 4Na + 2H2O + O2 2) Менее активные металлы Точно так же 3) Неактивные металлы Точно так же | 1) Активные металлы 1.Соль активного металла и бескислородной кислоты NaCl ↔ Na+ + Cl− K"катод"(-): 2H2O + 2e = H2 + 2OH− A"анод"(+): Cl− — 1e = Cl0; Cl0+Cl0=Cl2 Вывод: 2NaCl + 2H2O(электролиз) → H2 + Cl2 +2NaOH 2.Соль активного металла и кислородсодержащей кислоты Na2SO4↔2Na++SO42− K(-): 2H2O + 2e = H2 + 2OH− A(+): 2H2O — 4e = O2 + 4H+ Вывод: 2H2O (электролиз) → 2H2 + O2 3. Гидроксид: активный металл и гидроксид-ион NaOH ↔ Na+ + OH− K(-): 2H2O + 2e = H2 + 2OH− A(+): 2H2O — 4e = O2 + 4Н+ Вывод: 2H2O (электролиз) → 2H2 + O2 2) Менее активные металлы 1.Соль менее активного металла и бескислородной кислоты ZnCl2 ↔ Zn2+ + 2Cl− K"катод"(-): Zn2+ + 2e = Zn0 2H2O+2e-=H2+2OH- A"анод"(+): 2Cl− — 2e = 2Cl0 Вывод: ZnCl2 (электролиз) → Zn + Cl2 2.Соль менее активного металла и кислородсодержащей кислоты ZnSO4 ↔ Zn2++SO42− K(-): Zn2+ + 2e = Zn0 A(+): 2H2O — 4e = O2 + 4Н+ Вывод: 2ZnSO4 + 2H2O(электролиз) → 2Zn + 2H2SO4 + O2 3. Гидроксид: невозможно (нерастворим) 3) Неактивные металлы Точно так же |
Дополнительно о реакциях электролиза
В том случае, когда металл расположен в средней части ряда напряжения (от цинка до водорода) на катоде одновременно протекают два процесса: восстановление катиона металла и восстановление молекул воды. Рассмотрим электролиз водного раствора сульфата никеля с инертными электродами.
В растворе: NiSO4 = Ni2+ + SO42–;
На катоде:
K(-) Ni2+ + 2ē = Ni
2H2O + 2ē = H2 + 2OH–
Эти реакции никак не связаны между собой и суммировать их нельзя! Никакого простого соотношения между количеством никеля и водорода нет, оно зависит от концентрации, температуры, материала катода и прочих факторов.
На аноде:
А(+) (SO42– – не окисляются )
2H2O – 4ē = O2 + 4H+
Общих уравнений (катод + анод) в этом случае тоже будет два. Чтобы получить общее уравнение основной реакции, мы должны сложить уравнение основного процесса на катоде и уравнение анодного процесса, с учетом коэффициентов электронного баланса:
K(-) Ni2+ + 2ē = Ni |2
А(+) 2H2O – 4ē = O2 + 4H+|1
--------------------------------------------------------
2Ni2+ + 2H2O = 2Ni + O2 + 4H+ – ионное,
2NiSO4 + 2H2O = 2Ni + O2 + 2H2SO4 – молекулярное уравнение основной реакции.
Аналогично получаем общее уравнение побочной реакции:
K(-) 2H2O + 2ē = H2 + 2OH–|2
А(+) 2H2O – 4ē = O2 + 4H+|1
--------------------------------------------------------
6H2O = 2H2 + 4OH– + O2 + 4H+
2H2O = 2H2 + O2
Реакции
основание + кислота = соль + вода
основный оксид + кислота = соль + вода
основание + кислотный оксид = соль + вода
основный оксид + кислотный оксид = соль
амфотерный оксид (гидроксид) + кислота (основание) = соль + вода
металл + кислота = соль + Н2
металл + неметалл = соль бескислородной кислоты
pH = - lg [H+]
[H+] = [OH-] = 10-7 - среда нейтральная, рН=7
[H+] > 10-7 - среда кислая, рН < 7
[H+] < 10-7 - среда щелочная, рН > 7
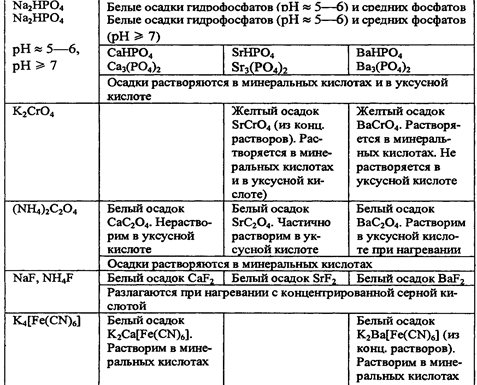
Гидролиз солей
| Состав соли | Примеры | Способность к гидролизу | Уравнение реакции гидролиза | Реакция среды | |
| катион | анион | ||||
| Сильного основания | Сильной кислоты | BaCl2, NaBr, K2SO4 | Не гидролизуется | - | Нейтральная рН=7 |
| слабого основания | Слабой кислоты | CH3COONH4, (NH4)2CO3 | Гидролизуется в наибольшей степени | CH3COONH4 + H2O <=> CH3COOH + NH3*H2O | Зависит от степени диссоциации (a) образующихся продуктов |
| Сильного основания | Слабой кислоты | Na2CO3, K2SO3, CH3COONa | гидролизуется | CO32- + H2O <=> HCO3- +OH- | Щелочная рН < 7 |
| слабого основания | Сильной кислоты | ZnCl2, Fe(NO3)2, CuSO4 | гидролизуется | Zn2+ +H2O <=> ZnOH+ + H+ | Кислая рН > 7 |

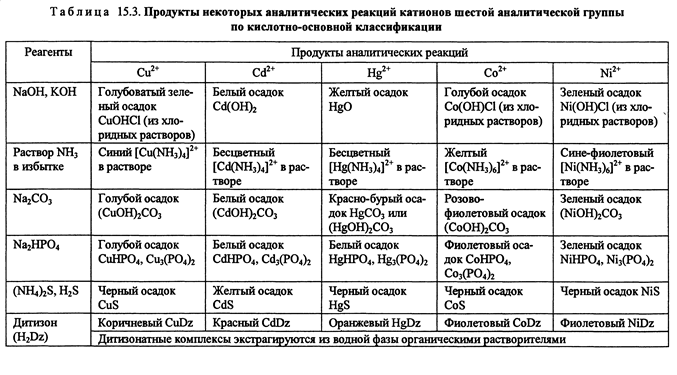
Индикаторы
| индикатор | Интервал перехода рН | Изменение окраски | ||
| Кислая среда | нейтральная | щелочная | ||
| фенолфталеин | 8,2-10,0 | Бесцветный | Бесцветный | красный |
| Лакмус | 5,0-8,0 | красная | желтая | синяя |
| метиловый оранжевый | 3,0-4,0 | красная | желтая | желтая |


 |  | ||
 |  | ||
 |
 |
|
из
5.00
|
Обсуждение в статье: Изменение электролизом веществ |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

