 |
Главная |
Силы притяжения, действующие между атомами и молекулами на больших расстояниях
|
из
5.00
|
Выше мы показали (см. (3.7)), что благодаря высокой симметрии атома водорода его электростатическое поле экспоненциально мало на больших расстояниях от атомного ядра. При этом мы не учитывали флуктуаций электромагнитного поля, которые связаны с обусловленными движением атомного электрона флуктуациями электронной плотности внутри атома. Подобного рода флуктуации приводят к тому, что на больших расстояниях между атомами и молекулами возникает дополнительное взаимодействие, которое имеет характер притяжения и называется дисперсионным.
Дисперсионное взаимодействие – это квантовый эффект, и его последовательное описание возможно только в рамках квантовой механики. Тем не менее, оно допускает простое качественное объяснение.
Рассмотрим простейший пример дисперсионного взаимодействия двух атомов водорода (рис.3.1, а).
В каждый момент времени электрон атома водорода располагается вблизи атомного ядра в определенной точке пространства, создавая мгновенный (быстро меняющийся) электрический диполь с дипольным моментом  . Мгновенное электрическое поле этого диполя будет оказывать влияние на движение электрона соседнего атома, благодаря чему движение обоих атомных электронов становится коррелированным (согласованным). Возникновение корреляции в движении электронов соседних атомов эквивалентно тому, что под действием мгновенного электрического поля
. Мгновенное электрическое поле этого диполя будет оказывать влияние на движение электрона соседнего атома, благодаря чему движение обоих атомных электронов становится коррелированным (согласованным). Возникновение корреляции в движении электронов соседних атомов эквивалентно тому, что под действием мгновенного электрического поля  одного атома возникает дипольный момент
одного атома возникает дипольный момент  у второго атома, причем
у второго атома, причем  ~
~  , или, иначе,
, или, иначе,  , где a – коэффициент пропорциональности, называемый поляризуемостью частицы.
, где a – коэффициент пропорциональности, называемый поляризуемостью частицы.
Как известно (приложение 3), напряженность электрического поля диполя  . Поэтому
. Поэтому  , где R – расстояние между соседними атомами.
, где R – расстояние между соседними атомами.
Энергия взаимодействия двух диполей  , поэтому для энергии дисперсионного взаимодействия двух атомов водорода получаем:
, поэтому для энергии дисперсионного взаимодействия двух атомов водорода получаем:
 . .
| (3.17) |
Аналогичные рассуждения можно провести и для более сложных атомов, и даже для молекул. При этом более строгий квантовомеханический расчет приводит к той же зависимости энергии дисперсионного взаимодействия этих частиц от расстояния, что и в формуле (3.17). В частности, Лондон показал, что энергия дисперсионного взаимодействия двух атомных частиц разного сорта (1 и 2)
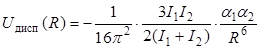 , ,
| (3.18) |
где I – энергия ионизации частицы (см. табл. 2.1).
Следует отметить, что энергия дисперсионного взаимодействия отрицательна. Это говорит о том, что дисперсионное взаимодействие действительно имеет характер притяжения. Благодаря тому, что энергия дисперсионного взаимодействия пропорциональна квадрату мгновенного дипольного момента, она оказывается отличной от нуля даже тогда, когда среднее по времени значение самого дипольного момента равно нулю (как известно,  ). В то же время известно, что при определенных условиях атомы, а тем более молекулы, в которых центры положительного и отрицательного зарядов часто не совпадают, могут обладать еще и постоянным дипольным моментом. В этом случае частицы, находясь на большом расстоянии друг от друга, могут взаимодействовать еще и посредством постоянного электрического поля.
). В то же время известно, что при определенных условиях атомы, а тем более молекулы, в которых центры положительного и отрицательного зарядов часто не совпадают, могут обладать еще и постоянным дипольным моментом. В этом случае частицы, находясь на большом расстоянии друг от друга, могут взаимодействовать еще и посредством постоянного электрического поля.
Электростатическое взаимодействие двух частиц, одна из которых имеет постоянный дипольный момент  , а другая не обладает собственным дипольным моментом, называется индукционным.
, а другая не обладает собственным дипольным моментом, называется индукционным.
Индукционное взаимодействие возникает благодаря тому, что электрическое поле диполя  индуцирует дипольный момент
индуцирует дипольный момент  у второй частицы:
у второй частицы:  . Энергия индукционного взаимодействия будет определяться энергией взаимного притяжения постоянного диполя
. Энергия индукционного взаимодействия будет определяться энергией взаимного притяжения постоянного диполя  и индуцированного диполя
и индуцированного диполя  . Как показал Дебай, эта энергия
. Как показал Дебай, эта энергия
 . .
| (3.19) |
Молекулы, обладающие собственным дипольным моментом, называются полярными. Полярными являются все двухатомные молекулы с полярной ковалентной (а значит, и с ионной) связью.
Молекулы, не имеющие постоянного дипольного момента, называются неполярными.
В международной системе единиц СИ дипольный момент измеряется в кулон-метрах (Кл×м). Однако значения дипольных моментов реальных молекул оказываются при этом очень маленькими, поэтому достаточно часто их выражают в дебаях (D): 1 D = 3,336×10–30 Кл×м.
Дипольный момент двухатомной молекулы AB, выраженный в дебаях, можно оценить, зная электроотрицательности (по Полингу)  и
и 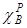 атомов, из которых она состоит (см. табл.2.1):
атомов, из которых она состоит (см. табл.2.1):
 , D. , D.
| (3.20) |
В многоатомных молекулах связь между атомами может быть полярной, а сами молекулы в зависимости от пространственного строения могут быть как полярными, так и неполярными. Дипольные моменты и поляризуемости некоторых молекул приведены в таблице 3.1.
Электростатическое взаимодействие двух частиц, каждая из которых обладает постоянным дипольным моментом, называется ориентационным.
Ориентационное взаимодействие стремится расположить диполи  и
и  так, чтобы их энергия оказалась минимальной (рис.3.2):
так, чтобы их энергия оказалась минимальной (рис.3.2):
 . .
| (3.21) |
Однако правильная ориентация диполей нарушается тепловым движением. Поэтому энергия системы, определяемая ориентацией частиц, сильно зависит от температуры: при низких температурах, когда достигается полная ориентация диполей, энергия ориентационного взаимодействия определяется соотношением (3.21), а при высоких температурах, как показал Кеезом,
Таблица 3.1.[1] Дипольные моменты и поляризуемость некоторых молекул
| d, D | a, 10–24 см3 | |
| H2 | 9.93 | |
| N2 | 22.1 | |
| CO2 | 33.3 | |
| CO | 0.10 | 24.5 |
| HF | 1.91 | 6.4 |
| HCl | 1.08 | 33.1 |
| HBr | 0.80 | 45.4 |
| HI | 0.42 | 68.5 |
| H2O | 1.85 | 18.6 |
| NH3 | 1.47 | 27.8 |
| CCl4 | ||
| CHCl3 | 1.01 | |
| CH2Cl2 | 1.57 | 81.4 |
| CH3Cl | 1.87 | 103.4 |
| CH4 | 32.7 | |
| CH3OH | 1.71 | 40.6 |
| CH3CH2OH | 1.68 | |
| C6H6 | 129.7 | |
| C6H5CH3 | 0.36 | |
| He | 2.5 | |
| Ar | 20.1 |

| Рис. 3.2.За счет электростатического взаимодействия разноименных зарядов диполи ориентируются в пространстве так, чтобы их дипольные моменты  и и  оказались направлены в одну сторону, вдоль прямой, соединяющей центры диполей. При этом энергия взаимодействия диполей принимает минимальное значение. оказались направлены в одну сторону, вдоль прямой, соединяющей центры диполей. При этом энергия взаимодействия диполей принимает минимальное значение.
|
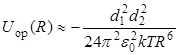 , ,
| (3.22) |
где k – постоянная Больцмана.
Следует отметить, что частицы, обладающие собственным дипольным моментом, под действием поля соседних частиц могут приобрести дополнительный (индуцированный) дипольный момент. Поэтому в общем случае при сближении двух частиц энергия их притяжения будет складываться из энергии дисперсионного, ориентационного и индукционного взаимодействия:
 . .
| (3.23) |
Эта энергия будет наибольшей для полярных частиц, для которых одновременно проявляются все три вида сил. Неполярные же частицы притягиваются друг к другу только за счет дисперсионного взаимодействия.
Силы притяжения, которые отвечают энергии взаимодействия частиц (3.23), получили обобщенное название сил Ван-дер-Ваальса.
В заключение этого раздела отметим, что электростатическое взаимодействие – не единственный вид взаимодействия частиц, которые находятся на больших расстояниях друг от друга. Если атомы или молекулы обладают постоянным магнитным моментом, то они могут взаимодействовать еще и посредством постоянного магнитного поля (приложение 3). Так, частицы, обладающие магнитными моментами  и
и  , подобно диполям (рис.3.2), будут оказывать ориентирующее воздействие друг на друга, которому при низких температурах отвечает энергия притяжения
, подобно диполям (рис.3.2), будут оказывать ориентирующее воздействие друг на друга, которому при низких температурах отвечает энергия притяжения
 , ,
| (3.24) |
а при высоких – энергия
 . .
| (3.25) |
Обычно магнитное притяжение атомов и молекул оказывается намного более слабым, чем дисперсионное или электростатическое. Однако о нем не следует забывать при расчетах полной энергии взаимодействия этих частиц.
|
из
5.00
|
Обсуждение в статье: Силы притяжения, действующие между атомами и молекулами на больших расстояниях |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

