 |
Главная |
Бесконкурентное ингибирование
|
из
5.00
|
В редких случаях степень торможения активности фермента может увеличиваться с повышением концентрации субстрата. Для этого типа торможения был предложен термин «бесконкурентное ингибирование».
Бесконкурентное ингибирование имеет место, когда ингибитор взаимодействует с ферментом только в составе фермент-субстратного комплекса [ES], но не со свободным ферментом.
Субстрат, связываясь с ферментом, изменяет его конформацию, что делает возможным связывание ингибитора. В свою очередь ингибитор, так меняет конформацию фермента, что катализ становится невозможным и продукты реакции не образуются. На рис. 6.6 представлена зависимость 1/V0 от 1/[S] в отсутствие и в присутствии бесконкурентного ингибитора.

| Рис. 6.6 | Графическое изображение бесконкурентного ингибирования в координатах Лайнуивера-Берка. –I – ингибитор отсутствует, +I – ингибитор присутствует. Начальная скорость реакции обозначена символом v. |
Таким образом, один из механизмов бесконкурентного торможения обусловлен возможностью соединения ингибитора с комплексом [ES] с образованием неактивного или медленно реагирующего тройного комплекса [EIS].
Ингибирование субстратом – частный случай бесконкурентного торможения, когда две молекулы субстрата связываются с ферментом, что препятствует образованию продукта.
Активность многих ферментов тормозится избытком субстрата, причем известно несколько механизмов этого процесса.
1. Если в образовании фермент-субстратного комплекса участвует несколько функциональных групп фермента, то возможно одновременное связывание в активном центре двух или более молекул субстрата, что приводит к образованию неактивного комплекса.
2. В случае избытка субстрата возможно его связывание не только в активном центре, но и с другими химическими группировкам, функционально связанным с активным центром. Такого рода взаимодействие может помешать ферментативной реакции.
3. Увеличение концентрации субстрата может повысить ионную силу реакционной среды и, как следствие, затормозить скорость ферментативной реакции.
Принцип метода
В теоретическом приложении к лабораторной работе №5 было указано, что скорости ферментативных реакций рассчитывают либо по убыли исходных веществ, т.е. субстратов, подвергающихся каталитическому воздействию, либо по образованию и накоплению продуктов реакции в единицу времени. Одним из примеров реакций, часто используемых в лабораторных практикумах для определения кинетических параметров, является реакция гидролиза крахмала под действием амилазы слюны. Следует, однако, помнить, что корректное определение главных кинетических параметров ферментативных реакций – константы Михаэлиса, КM, и максимальной скорости, Vmax, возможно только в условиях начальной стадии процесса, когда концентрация субстрата велика и практически соответствует его исходному количеству, фермент находится в состоянии насыщения и, следовательно, скорость реакции пропорциональна концентрации фермент-субстратного комплекса [ES]. Вполне понятно, что при высокой концентрации субстрата, как это имеет место в случае гидролиза крахмала, следить за начальной скоростью реакции по его убыли затруднительно. Поэтому наиболее грамотно определять начальную скорость процесса не по убыли субстрата, а по накоплению продукта реакции.
Исходя из сказанного выше, удобной системой для расчета КM и Vmax в условиях in vitro может быть ацетилхолинэстераза мембран теней эритроцитов, которая катализирует реакцию гидролиза сложноэфирной связи в ацетилхолине с образованием холина и ацетата:

В ферментативной кинетике успех определения кинетических параметров зависит не только от выбранной ферментной системы, но и от чувствительности и адекватности метода анализа продукта или продуктов реакции. В нашем случае в качестве субстрата ацетилхолинэстеразы целесообразно использовать не ацетилхолин, а его аналог – ацетилтиохолин:

Главная идея использования ацетилтиохолина в качестве субстрата ацетилхолинэстеразы заключается в том, что в результате гидролиза тиоэфирной связи в этом субстрате один из продуктов реакции – тиохолин содержит сульфгидрильную группу:
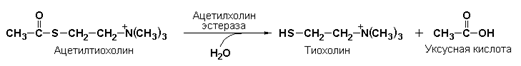
Накапливающийся тиохолин взаимодействует с 5,5'-дитиобис[2-нитробензойной кислотой] (реактив Эллмана) с образованием 2-нитро-5-меркаптобензойной кислоты, которая окрашена в желтый цвет, причем интенсивность окраски пропорциональна содержанию в реакционной смеси 2-нитро-5-меркаптобензойной кислоты и, следовательно, тиохолина.
Приведенные выше рассуждения позволяют сделать вывод о том, что система ацетилхолинэстераза-ацетилтиохолин является во всех отношениях удобной не только для расчета значений КM и Vmax реакции гидролиза ацетилтиохолина, но позволит также определить значение константы ингибирования этой реакции, КI, при использовании в качестве ингибитора естественного субстрата ацетилхолинэстеразы – ацетилхолина.
Контрольные вопросы
1. Влияние концентрации субстрата на скорость ферментативных реакций
2. Уравнение Михаэлиса–Ментен. Уравнение Лайнуивера-Берка
3. Графическое определение величины константы Михаэлиса
4. Типы ингибирования активности ферментов. Графическое определение величин констант Михаэлиса в отсутствие и в присутствии ингибиторов
5. Принцип метода определения кинетических параметров реакции гидролиза сложноэфирной связи под действием ацетилхолинэстеразы
Литература
1. Диксон М., Уэбб Э., Ферменты, т. 1, «Мир», М., 1982
2. Диксон М., Уэбб Э., Ферменты, т. 2, «Мир», М., 1982
3. Марри Р., Греннер Д., Мейес П., Родуэлл В., Биохимия человека, т. 1, «Мир», М., 1993
4. Горячковский А.М., Справочное пособие по клинической биохимии, ОКФА, Одесса, 1994
5. Степанов В.М., Молекулярная биология: структура и функции белков, под ред. академика Спирина А.С., «Высшая школа», М., 1996
6. Кнорре Д.Г., Мызина С.Д., Биологическая химия, «Высшая школа», М., 1998
7. Кольман Я., Рем К.-Г., Наглядная биохимия, «Мир», М., 2000
8. Северин Е.С., Биохимия, «Гэотар-мед», М., 2004.
9. Комов В.П.,Биохимия, М.: Дрофа, 2004.
10. Чиркин А.А., Практикум по биохимии, «Новое знание», Минск, 2002.
11. Кухта В.К., Морозкина Т.С., Олецкий Э.И., Таганович А.Д., Биологическая химия, «Бином», М., 2008.
12. Чиркин А.А., Данченко Е.О., Биохимия, «Медицинская литература», М., 2010.
Дополнительная литература
1. Nelson D.L., Cox M.M., Lehninger Principles of Biochemistry, W.H. Freeman (ed.), 2004.
2. Metzler D., Biochemistry, (The chemical reactions in living cells), Elsevier, Academic Press, V. 1-2, 2003-2004.
3. Berg J.M., Tymoczko J.L., Lubert Stryer, Biochemistry, W.H. Freeman (ed.), 2006.
Ход работы
| Цель работы: | Определение кинетических параметров ферментативных реакций. Регуляция активности ферментов |
| Задание I | Определить значения KM и Vmax реакции гидролиза крахмала под действием бактериальной амилазы |
*Определение кинетических параметров, KM и Vmax, реакции гидролиза крахмала под действием бактериальной амилазы
1. В 5 пробирок вносят по 1 мл препарата амилазы слюны. Затем в каждую добавляют по 1 мл воды.
2. Пробирки инкубируют в термостате 38°С в течение 1 мин.
3. Последовательно, точно отметив начальное время реакции, в каждую пробирку добавляют по 1 мл раствора крахмала в концентрации, указанной в таблице:
| № пробирки | |||||
| Концентрация крахмала, мМ | 0,5 | 0,25 | 0,125 |
4. В каждую пробирку добавляют 200 мкл раствора I2 в KI (реактива Люголя). Пробы инкубируют в течение 10 мин.
5. Определяют оптическую плотность при l=620 нм. Полученные результаты представляют в виде следующей таблицы:
| № пробирки | Концентрация крахмала, мМ | А620 |
| 0,5 | ||
| 0,25 | ||
| 0,125 | ||
6. Строят график зависимости Vотн от [S]. По графику Лайнуивера-Берка определяют значение КM
*Влияние активаторов и ингибиторов на кинетические параметры бактериальной амилазы
1. В 10 пробирок вносят по 1 мл раствора фермента.
2. В первые 5 пробирок (серия № 1) добавляют по 1 мл 1 % раствора NaCl, в оставшиеся (серия № 2) - по 1 мл 2 % раствора CuSO4.
3. Пробирки инкубируют в термостате при 38°С в течение 1 мин.
4. Добавление 1 мл субстрата в указанной в таблице концентрации (см. предыдущее задание) проводят попарно в каждую серию пробирок, например, через 2 мин.
5. В каждую пробирку добавляют 200 мкл раствора I2 в KI. Пробы инкубируют в течение 10 мин.
6. Проводят фотометрирование образцов при l=620 нм. Полученные результаты представляют в виде следующей таблицы:
| № пробирки | А620 | |
| Серия №1 (без ингибитора) | Серия №2 (с ингибитором) | |
7. Строят график зависимости Vотн от [S] для первой (с NaCl) и второй (с СuSO4) серий проб. Рассчитывают KM и Vmax для скорости реакции расщепления крахмала в отсутствии и присутствии ингибитора, пользуясь графиком Лайнуивера-Берка.
| Задание II | Определить кинетические параметры KM и Vmax реакции гидролитического расщепления ацетилтиохолина с участием холинэстеразы и характер ингибирующего действия ацетилхолина на гидролиз ацетилтиохолина под действием холинэстеразы мембран теней эритроцитов |
*Приготовление калий-фосфатного буферного раствора
2. В 100 мл стакан вносят 13,61 г КН2РО4, добавляют дистиллированной воды до отметки 70 мл и ставят на магнитную мешалку до полного растворения.
3. Доводят до значения рН 8,0 раствором гидроксида калия, а затем доводят до метки 100 мл дистиллированной водой.
*Приготовление раствора субстрата холинэстеразы (ацетилтиохолина йодида)
1. Для приготовления 0,075 М раствора растворяют 0,22 г ацетилтиохолин йодида в 10 мл дистиллированной воды. Держать на холоду!
*Приготовление реактива Эллмана
1. Для получения 10 мМ раствора реактива Эллмана 37 мг 5,5'-дитиобис[2-нитробензойной] кислоты растворяют в 10 мл 0,1 М калий-фосфатного буфера рН 7,0. Перемешивают до полного растворения.
2. В полученный раствор добавляют 15 мг бикарбоната натрия и снова перемешивают.
*Определение кинетических параметров, KM и Vmax, реакции гидролиза ацетилтиохолина под действием ацетилхолинэстеразы
1. В пяти пробирках в соответствии с приведенной ниже таблицей готовят разведения ацетилтиохолина (исходная концентрация 10 –3 М):
| № пробирки (разведения) | Концентрация АТХ, мМ | VАТХ , мл | Vбуфер* ), мл |
| 0,5 | |||
| 0,4 | 0,8 | 1,2 | |
| 0,2 | 0,4 | 1,6 | |
| 0,1 | 0,2 | 1,8 |
*) – 0,1 М натрий-фосфатный буфер рН 7,40 (далее – «буфер»)
2. В фотометрическую кювету вносят:
0,5 мл мембран эритроцитов,
0,2 мл буфера;
0,5 мл реактива Эллмана.
Смесь тщательно перемешивают.
3. Затем, по секундомеру, в кювету при тщательном перемешивании добавляют 0,5 мл раствора АТХ из пробирки №1 (см. таблицу).
4. Кювету помещают в спектрофотометр и через 10 секунд после внесения АТХ обнуляют значение оптической плотности при 412 нм.
5. Регистрируют изменение оптической плотности при 412 нм в течение 2 мин с интервалом 20 секунд (9 точек).
6. Для разведений субстрата в пробирках №2, №3, №4 и №5 (см. таблицу) манипуляции повторяют согласно пунктам 2-5.
7. Полученные данные заносят в таблицу.
| t, секунды | Оптическая плотность, А412 | ||||
| Разведение №1 | Разведение №2 | Разведение №3 | Разведение №4 | Разведение №5 | |
8. Результаты измерений отражают графически в виде зависимостей оптической плотности от времени, характеризующих кинетику данной ферментативной реакции при разных концентрациях субстрата (все пять графиков строят на одних координатных осях).
9. Затем строят график зависимости скорости данной ферментативной реакции от концентрации субстрата. Скорость реакции выражают в значениях оптической плотности от концентрации АТХ (то есть для каждого разведения), полученных в один и тот же промежуток времени. Для построения графика используют значения оптической плотности, полученные через 60 секунд от начала реакции. График строят в соответствии с ниже приведенной таблицей:
| № разведения | Концентрация АТХ, мМ | Данные для построения графика по уравнению Михаэлиса-Ментен | Данные для построения графика Лайнуивера-Берка | ||
| Конечная концентрация АТХ (в кювете), мМ | А412 при t=60 c | 1/[АТХ]*) | 1/А412 | ||
| 0,5 | |||||
| 0,4 | |||||
| 0,2 | |||||
| 0,1 |
*) – [АТХ] – конечная концентрация АТХ.
10. Полученную зависимость преобразуют в координатах Лайнуивера-Берка в соответствии с таблицей, и рассчитывают значения KM и Vmax, характеризующие гидролитическое расщепление АТХ под действием ацетилхолинэстеразы.
*Влияние ингибитора на кинетические параметры ацетилхолин-эстеразы
1. В фотометрическую кювету вносят:
0,5 мл мембран эритроцитов,
0,5 мл реактива Эллмана.
Смесь тщательно перемешивают
2. Затем, по секундомеру, в кювету при тщательном перемешивании одновременно добавляют 0,5 мл раствора АТХ из пробирки №1 и 0,2 мл раствора ацетилхолина (ингибитора).
Примечание: в данном случае используют разведения, приготовленные в предыдущем опыте.
3. Дальнейшие манипуляции соответствуют пунктам 4-10 предыдущего опыта.
Примечание: для наглядности, зависимости оптической плотности от концентрации АТХ в координатах Михаэлиса–Ментен и Лайнуивера-Берка в отсутствии и присутствии ингибитора строят на одних графиках.
4. Делают выводы о характере ингибирования.
Оформление работы
К занятию:
1. Кратко законспектировать теоретические материалы к лабораторной работе.
Во время занятия:
2. Описать этапы работы.
3. Оформить результаты в виде таблиц, графиков и полученных на их основе значений KM и Vmax.
Сделать выводы по каждому из опытов.
|
из
5.00
|
Обсуждение в статье: Бесконкурентное ингибирование |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

