 |
Главная |
Тепловой баланс реактора
|
из
5.00
|
Уравнение теплового баланса реактора гидроочистки:
| Qc + Qц +Qs +Qг.н = ∑ Qсм, | (2.16) |
где Qс, Qц – тепло, вносимое в реактор со свежим сырьем и циркулирующим водородсодержащим газом, кДж/ч.
Qs, Qг.н – тепло, выделяемое при протекании реакций гидрогенолиза сернистых и гидрирования непредельных соединений, кДж/ч.
ΣQсм – тепло, отводимое из реактора реакционной смесью, кДж/ч.
Средняя теплоемкость реакционной смеси при гидроочистке незначительно изменяется в ходе процесса, поэтому тепловой баланс реактора можно записать в следующем виде:
 , ,
| (2.17) | |
 , ,
| (2.18) |
где G – суммарное количество реакционной смеси, % масс.;
 – средняя теплоемкость реакционной смеси, кДж/(кг*К);
– средняя теплоемкость реакционной смеси, кДж/(кг*К);
∆S, ∆Сн – количество серы и непредельных, удаленных из сырья, % масс.;
t, t0 – температуры на входе в реактор и при удалении серы ∆S, °C;
qs, qн – тепловые эффекты гидрирования сернистых и непредельных соединений, кДж/кг
При оптимизации t0 учитывают следующие два фактора, действующие в противоположных направлениях: с повышением t0 уменьшается загрузка катализатора, которая требуется для достижения заданной глубины обессеривания ∆S но, с другой стороны, увеличивается скорость дезактивации катализатора, и следовательно, увеличиваются затраты, связанные с более частыми регенерациями и большим простоем установки за календарный год.
Температура на входе в реактор t0 = 370 °С.
Суммарное количество реакционной смеси на входе в реактор составляет 116,412 % масс. (таблица 2.6).
Количество серы, удаленное из сырья ∆S = 0,955 % масс.
Количество удаляемых непредельных соединений сырья ∆Сн=0 % масс.
Количество тепла, выделяемое при гидрогенолизе сернистых соединений (на 100 кг сырья) составит:
| QS = ∑qSi·gSi, | (2.19) |
где qSi – тепловые эффекты гидрогенолиза сераорганических соединений, кДж/кг [22, с.143];
gSi – количество разложенных сероорганических соединений, кг (при расчете на 100 кг сырья оно численно равно содержанию отдельных сероорганических соединений в % масс.).
QS =0,05·2100+0,35·3500+0,09·4800+ (0,47-0,005) ·8700 =5 807,5 кДж.
Количество тепла, выделяемое при гидрировании непредельных углеводородов Qг.н =0.
Среднюю теплоемкость циркулирующего водородсодержащего газа находят на основании данных по теплоемкости отдельных компонентов (таблица 2.7).
Таблица 2.7 – Теплоемкость индивидуальных компонентов циркулирующего водородсодержащего газа
| Показатель | Компонент | ||||
| Н2 | СН4 | С2Н6 | С3Н8 | С4Н10 | |
| cР, кДж/(кг·К) | 14,570 | 3,350 | 3,290 | 3,230 | 3,180 |
| cР, кДж/(кг·°С) | 3,480 | 0,800 | 0,786 | 0,772 | 0,760 |
Теплоемкость циркулирующего водородсодержащего газа можно найти по формуле:
| Сц = ∑ cРi · yi, | (2.20) |
где cРi – теплоемкость отдельных компонентов с учетом поправок на температуру и давление, кДж/(кг·К);
yi - массовая доля каждого компонента в циркулирующем водородсодержащем газе (см. таблицу 2.5).
Сц = 14,57·0,192+3,35·0,427+3,29·0,201+3,23·0,103+3,18·0,077 = 5,467 кДж/(кг*К).
Энтальпию паров сырья при 370 °С определяют по графику
[21, с. 333], для 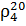 = 0,835 I370 = 1 155 кДж/кг.
= 0,835 I370 = 1 155 кДж/кг.
Поправку на давление находят по значениям температуры и давления.
Абсолютная критическая температура сырья определяется с использованием графика, представленного на рисунке 1.14 [21, с. 60]:
 , ,
| (2.21) |
где Тср – среднемолекулярная температура кипения, К.
Тср определяется в зависимости от М и ρ1515 графически
Тср =245 [c.18].

Ткр = 720 К [21, с.60].
Приведенная температура равна
Тпр = (370+273)/720= 0,893
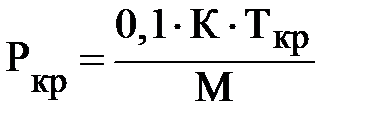

Приведенное давление:
| Рпр = Р/Ркр, | (2.22) |
Рпр = 4/4,29 = 0,93.
Для найденных значений Тпр и Рпр, по рис 1.17 [21, с. 63] получаем
∆ I·М/ Ткр = 25,140 кДж/(кмоль·К)
∆I = 7,28·Ткр/М = 7,28·4,2·675/195 = 92,82 кДж/ кг
I370с = Iс -∆I = 1 155 –92,82 = 1062,18 кДж/кг.
Теплоёмкость сырья с поправкой на давление:
| Сс= I370c/(t+273) | (2.23) |
Сс=1062,18/(370+273)= 1,65 кДж/(кг·К)
Средняя теплоёмкость реакционной смеси:
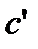 = (Сс·100 + Сц·16,412)/G = (Сс·100 + Сц·16,412)/G
| (2.24) |
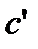 = (1,65·100+ 5,467·16,412)/ 116,412= 2,19 кДж/(кг·К).
= (1,65·100+ 5,467·16,412)/ 116,412= 2,19 кДж/(кг·К).
Температура на выходе из реактора:
t = 370+ (5 807,5 + 0)/( 116,412·2,19) = 393 ºС.
|
из
5.00
|
Обсуждение в статье: Тепловой баланс реактора |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

