 |
Главная |
Часть 2. Соли, получение, свойства
|
из
5.00
|
Средней силы и слабые растворимые, образуют растворы с довольно кислой средой: фосфорная, плавиковая (HF), уксусная
Слабые, летучие, неустойчивые: сероводородная, сернистая, угольная, азотистая. Среда в растворах этих кислот очень слабо кислая.
4) Нерастворимые: кремниевая, борная Н3ВО3.Не меняют окраску индикатора.
Свойства кислот.
Ряд напряжений металлов:
Li, Rb, K, Ba, Sr, Ca, Na, Mg, Al, Mn, Zn, Cr, Fe, Cd, Co, Ni, Sn, Pb,H,Sb, Bi, Cu, Hg, Ag, Pd, Pt, Au
| Свойство | Примеры | Примечания |
| 1.Электроли-тическая диссоциация в водных растворах. | HCl ⇄ H+ + Cl– (точнее, не Н+, а Н3О+-ион гидроксония) Многоосновные кислоты диссоциируют cтупенчато: H2SO3 ⇄ H+ + НSO3– (1 ступень) и HSO3– ⇄ H+ + SO32– (2 ступень) | Нерастворимые кислоты практически не диссоциируют. |
| 2. Действие на индикаторы. | Так как растворы кислот имеют кислую среду, они меняют окраску индикаторов. Причина – наличие в растворе ионов Н+(H3O+). Лакмус и метилоранж приобретают КРАСНУЮ окраску. | H2SiO3, H2S, H2CO3 - практически не меняют окраску индикаторов. |
| 3. Взаимодействие с основаниями и амфотерными гидроксидами. | H2SO4 + Ca(OH)2= CaSO4 + 2H2O HCl + Al(OH)3 = AlCl3 + H2O H2SiO3 + 2NaOH = Na2SiO3 + 2H2O H2SO4 + KOH(изб) = K2SO4 + H2O H2SO4(изб) + KOH = KHSO4 + H2O | Слабые кислоты реагирует только со щелочами. Возможно образование кислых солей. |
| 4. Взаимодействие с основными и амфотерными оксидами | 2 HCl + CaO = CaCl2 +H2O 2 H3PO4+Fe2O3 = FePO4+3H2O | Кремниевая кислота – только при сплавлении. |
| 5. Взаимодействие со средними, кислыми, основными солями. | А) Cоль1+кислота1=соль2+кислота2 2HCl +СаCO3 =СаCl2+CO2+ H2O ВaCl2 +H2SO4 = ВaSO4¯+ 2HCl Б) Средняя соль + её же кислота = кислая соль.H2SO4+Na2SO4= 2NaHSO4 В) Основная соль+кислота = средняя соль.(СuOH)2CO3+4HCl=2CuCl2+CO2+3H2O Al(OH)2Cl + 2HCl = AlCl3 + 2H2O | Реакция происходит, если соль образована более слабой кислотой, или если образуется осадок, газ, вода. |
| 6.Взаимодействие с металлами минеральных кислот: HCl, HBr, HI, HF, H2SO4(разб!), Н3РО4 | 2HCl + 2Na = 2NaCl + H2 H2SO4 + Zn = ZnSO4 + H2 Исключение: при реакции с металлами азотной и конц. серной кислот водород не выделяется, реакция идёт по-другому! (см.п. 7) Не реагируют с металлами: H2S, H2SiO3, H2SO3, H2CO3 | Металл в ряду активности – должен находиться левее водорода. |
| 7. Особые свойства HNO3 и H2SO4 - реакция с металлами | Cu+4HNO3 (конц.) =Cu(NO3)2+2NO2+2H2O 3Cu+8HNO3(разб.)=3Cu(NO3)2+2NO+4H2O 8K+5H2SO4 (конц.) = 4K2SO4+H2S+4H2O 3Zn+ 4H2SO4 (конц.) = 3ZnSO4+S+4H2O | Пассивация Al, Cr, Fe – не реагируют с холодной концентрированной HNO3 и H2SO4 |
| 8. Разложение при нагревании. | 1) H2SiO3 → t SiO2 + H2O 2HNO2 = NO + NO2 + H2O 4HNO3 → t 2H2O + 4NO2 + O2 2) 2HI → t H2 + I2 | Угольная, сернистая и азотистая кислоты разлагаются при комнатной температуре. |
Способы получения кислот
| Способ получения | Примеры | Примечания |
| 1. Взаимодействие оксидов с водой | SO3 + H2O = H2SO4 | Кислородсодержащие кислоты. Кроме H2SiO3 |
| 2. Взаимодействие простых веществ | H2 + S = H2S | Бескислородные кислоты. |
| 3. Вытеснение более слабых кислот из их солей более сильными кислотами. | 2HCl+Na2S = 2NaCl+ H2S↑ 2HCl+Na 2SiO3= 2NaCl+ Н2SiО3↑ | Кремниевую кислоту можно получить ТОЛЬКО таким способом. |
| 4. Окисление кислот (или оксидов в водном растворе) кислородом и другими окислителями. | SO2+Br2+H2O=H2SO4+HBr H3PO3 + O2 → t H3PO4 | Реакции протекают в водном растворе. |
Часть 2. Соли, получение, свойства.
Получение солей.
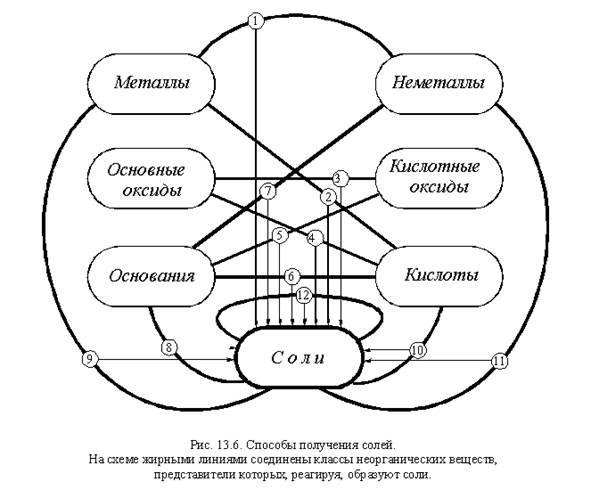
| Способ получения | Примеры | Примечания |
| 1. Металл + неметалл | 2K+Cl2 → t 2KCl | Соли бескислородных кислот |
| 2. Металл + кислота. | А) с минеральными кислотами (соляной, фосфорной, уксусной, разбавленной серной):Fe+H2SO4 (разб.) = FeSO4+H2 Б) с азотной и конц.серной 3Cu+8HNO3(разб.)=3Cu(NO3)2+2NO+4H2O | А) металлы левее Н |
| 3. Оксид + оксид | CaO+CO2 =CaCO3 ВаО + ZnO =BaZnO2 цинкат бария ZnO + SO3 = ZnSO4 | Идёт при нагревании. Соль должна существовать. |
| 4. Основный и амфотерный оксид + кислота. | А) H2SO4+CаO = CаSO4+H2O H2SO4+ZnO = ZnSO4+H2O Б) 2H2SO4(избыток) + СаО = H2O + Са(НSО4)2 | Для многоосновных кислот возможно образование кислой соли в избытке кислоты. |
| 5. Основание + кислотный оксид | Ca(OH)2(изб)+CO2 = CaCO3 +H2O карбонат кальция (средняя соль) Ca(OH)2+CO2(изб) = Ca(НCO3)2 +H2O гидрокарбонат кальция (кислая соль) | В случае избытка основания получается средняя соль, в избытке кислотного оксида – кислая соль. |
| 6. Основание + кислота ( а также аммиак + кислота) | H2SO4+2KOH(изб) = K2SO4+2H2O H2SO4(изб) + KOH = KНSO4+H2O гидросульфат калия Al(OH)3 + 2HCl =Al(OH)Cl2 +2Н2О гидроксохлорид алюминия NH3 + HCl = NH4Cl Хлорид аммония | Нерастворимые основания реагируют только с достаточно сильными кислотами. При избытке многоосновной кислоты – кислая соль, в случае избытка многокислотного основания – основная соль |
| 7*. Неметалл + основание | Si +2NaOH + H2O = Na2SiO3 + 2H2 | Только с кремнием (остальные неметаллы дают смеси солей) |
| 8. Основание + соль (средняя или кислая) | 3NaOH+FeCl3 =Fe(OH)3↓+3NaCl КОН+ KHSO4 = K2SO4+ H2O KOH + NH4NO3 = KNO3 + NH3 + H2O | И соль, и основание должны бытьрастворимы,а в продуктах должны быть – осадок, газ или вода. |
| 9. Металл + соль | Zn+CuSO4 =Cu+ZnSO4 | Более активный металл (но не реагирующий с водой) +растворимаясоль. |
| 10. Кислота + соль | H2S+CuCl2 = CuS ¯+ 2HCl HCl + CaCO3 = CаСl2 + CO2+ H2O Al(OH)2Cl+ 2HCl =AlCl3+2H2O | В продуктах – осадок, газ или вода. |
| 11*. Неметалл + соль | Cl2 + KI = KCl + I2 | Более активный галоген вытесняет из соли менее активный. |
| 12. Соль + соль (обе растворимые!) | AgNO3+KCl=AgCl↓+KNO3 | Реакцию идёт, если хотя бы одна из образующихся солей выпадает в осадок. |
* способ, применимый ТОЛЬКО для данного вещества (веществ).
Свойства солей.
Ряд напряжений металлов:
Li, Rb, K, Ba, Sr, Ca, Na, Mg, Al, Mn, Zn, Cr, Fe, Cd, Co, Ni, Sn, Pb,H,Sb, Bi, Cu, Hg, Ag, Pd, Pt, Au
| Свойства | Примеры | Примечания |
| 1) Диссоциация в водных растворах. | 1. Средние, двойные, смешанные соли диссоциируют полностью: (α = 1) NaCl à Na+ + Cl– КNaSO4 à К+ + Na+ + SO42– CaClBràCa2+ + Cl–+ Br– 2. Кислые соли: КHSO4à К+ + НSO4– (α = 1) HSO4– ⇄ H+ + SO42– (α <1) 3. Основные соли: FeOHCl àFeOH+ + Cl– (α = 1) FeOH+ ⇄ Fe2+ + OH–( α <1) 4. Комплексные соли: [Cu(NH3)4]SO4à[Cu(NH3)4]2++SO42– (α = 1) [Cu(NH3)4]2+ ⇄ Cu2+ + 4NH3 (α <1) | |
| 2)Взаимодействие с кислотами: | А) Cоль1+кислота1=соль2+кислота2 2HCl +СаCO3 =СаCl2+CO2+ H2O ВaCl2 +H2SO4 = ВaSO4¯+ 2HCl Б) Средняя соль + её же кислота = кислая соль.H2SO4+Na2SO4= 2NaHSO4 В) Основная соль+кислота = средняя соль.(СuOH)2CO3+4HCl=2CuCl2+CO2+3H2O Al(OH)2Cl + 2HCl = AlCl3 + 2H2O | Реакция происходит, если соль образована более слабой или летучей кислотой, или если образуется осадок,газ, вода. |
| 3) Взаимодействие с кислотными и амфотерными оксидами. | Na2CO3 + SiO2 → t СО2 ↑+ Na2SiO3 Na2CO3 + Al2O3 → t СО2↑+ NaAlO2 | Вытеснение твёрдым оксидом летучего оксида при сплавлении. |
| 4) Взаимодействие растворимых солей со щелочами. | CuSO4 + 2NaOH =Cu(OH)2¯+Na2SO4 NH4Cl + KOH = KCl + NH3+ H2O Кислые соли при действии щелочей превращаются в средние: KHCO3 + KOH = K2CO3 + H2O Кислая соль может реагировать с аммиаком: NH4HSO4 + NH3 = (NH4)2SO4 | Реакция происходит, если образуется осадок, газ или вода. |
| 5) Взаимодействие растворимых солей друг с другом. | AgNO3 + NaCl =AgCl¯+NaNO3 При взаимодействии двух кислых солей разных по силе кислот возможно вытеснение более слабой и летучей: NaHSO4+NaHS =H2S↑ + Na2SO4 | Реакция идёт, если взаимодействуют растворимые соли и при этом образуется осадок |
| 6) Взаимодействие с металлами. | Fe + CuSO4 =Cu + FeSO4 Металлы, стоящие левее в ряду активности и не реагирующие с водой вытесняют из растворимых солей стоящие правее металлы. | |
| 7) Разложение при нагревании. | А) карбонаты и гидрокарбонаты. Карбонаты(кроме Na,K,Rb,Cs) - разлагаются на 2 оксида. Гидрокарбонаты - до карбонатов. СаСO3 → t СаO + СО2. 2КНСО3 → t К2СО3 + СО2 + Н2О Б) соли аммония: Без ОВР(выделяется аммиак) – карбонат, сульфат, сульфит, сульфид, хлорид, фосфат. (NH4)2CO3 → t 2NH3 + CO2 + H2O С ОВР:нитрат, нитрит, дихромат: NH4NO3→ t N2O + 2H2O NH4NO2→ t N2 + 2H2O (NH4)2Cr2O7 → t N2 + 4H2O + Cr2O3 В) Галогениды (кроме фторидов): 2AgCl → t 2Ag + Cl2 Г) Нитраты: Левее магния (кроме лития) 2КNO3 → t 2КNO2+ O2 От магния до меди включительно + литий 2Cu(NO3)2→ t 2CuO + 4NO2 + O2 После меди: 2AgNO3→ t 2Ag +2NO2 + O2 | Соли аммония - выделяется аммиак или идёт ОВР. |
|
из
5.00
|
Обсуждение в статье: Часть 2. Соли, получение, свойства |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

