 |
Главная |
Влияние различных загрязнителей атмосферы на озон
|
из
5.00
|
Хлор – наиболее опасный катализатор распада озона [14, с.99]. Он активно соединяется с озоном, давая монооксид хлора и кислород. В свою очередь монооксид хлора легко присоединяет второй атом кислорода, при этом хлор освобождает и может вступить в реакцию со следующей молекулой озона.
Cl× + O3 ® ClO + O2;
ClO + O× ® Cl× + O2.
Одна молекула хлора за среднее время своего существования в верхних слоях атмосферы способна разложить 100 тысяч молекул озона. По сравнению с хлором следующий по активности разрушитель озона – оксид азота – почти безопасен: одна молекула NO разлагает в среднем всего 10 молекул озона. Хотя оксиды азота по сравнению с хлором в 10 тысяч раз менее активны как разрушители озона, их выброс в атмосферу многократно превышает выброс хлора. Озон могут разрушать и другие вещества: оксид углерода, водород, оксид серы, – но они связывают озон в отношении 1:1 и по сравнению с хлором и оксидами азота (NO, NO2) могут считаться безвредными.
Хлор попадает в атмосферу различными путями. Некоторое его количество теряется при утечках и авариях в химической промышленности, где это вещество широко используется, в частности в органическом синтезе. Но наиболее значительными «поставщиками» хлора в атмосфере являются фреоны, соединения фтора и хлора с углеродом. Наиболее распространенные фреоны:
CF4 – фреон 14, CClF3 – фреон 13, CCl2F2 – фреон 12, CHClF2 – фреон 22, CF2ClCFCl2 – фреон 113, CF2ClBr – фреон 12B1, CF3Br – фреон 13B1.
Фреоны характеризуются уникальным набором свойств, которые обеспечили им широкое использование в промышленности. Эти вещества имеют низкие температуры кипения, не ядовиты, не горючи, взрывобезопасны, химически инертны. Фреоны широко используются как газы-носители (пропилленты) в различного рода аэрозольных баллончиках, в миллионах бытовых и промышленных холодильниках как хладагент. Будучи чрезвычайно инертными, фреоны минуют тропосферу без изменений. Только в стратосфере они подвергаются фотохимическому разложению по радикальному механизму:
CFCl3 + hn ® CFCl2 + Cl; CF2Cl2 + hn ® CF2Cl + Cl.
Заметный вклад в разрушение озона вносят реактивная авиация (на высоте более 20 км) и ракеты самого разного назначения – метеорологические, исследовательские, выводящие на околоземные орбиты спутники связи, разведывательные спутники, космические корабли. При каждом запуске космического челнока системы «Шатл» его твердотопливные ускорители на высотах до 50 км, то есть в самом озоновом слое, выбрасывают 187 тонн хлора и хлористого водорода и 7 тонн оксидов азота. Этого количества хватает на то, чтобы уничтожить 10 миллионов тонн озона, или 0,3 % его общего содержания в атмосфере.
Природным хлорсодержащим компонентом, способным проникать в стратосферу и вступать в серию реакций, ведущих к выделению атома хлора, является хлористый метил. Он выделяется в больших количествах из морской воды, выбрасывается вулканами, а также образуется при горении биомассы.
Приведенные в середине 1970-х г. измерения показали, что хлорсодержащим компонентом стратосферы является HCl. Здесь имеет место достаточно интенсивный сток атомарного хлора с образованием этого газа:
Cl× + HO×2 ® HCl + O2; Cl× + CH4 ® CH3× + HCl.
Другими резервуарными газами служат нитрат оксида хлора и хлорноватистая кислота:
ClO + NO2 ® ClONO2; ClO + HO2× ® HOCl + O2.
Активные по отношению к озону формы регенерируются в реакциях:
HCl + HO× ® Cl× + H2O;
HOCl + hn ® Cl× + HO×;
ClONO2 + hn ® ClO + NO2.
Из оксида хлора под действием атомарного кислорода вновь образуется атом хлора.
Бром поступает в стратосферу в составе СН3Br, а также фторброма и фторхлорбромуглеводородов (галонов). В наибольших количествах в атмосфере содержатся CF3Br (галон – 1301) и CF2ClBr (галон – 1211). Продолжительность жизни галонов в нижней тропосфере оценивается примерно в 70 лет. Поэтому они, как и фреоны, постепенно переносятся через тропопаузу в стратосферу.
Под действием солнечной радиации в ближней УФ области спектра галоны разлагаются с выделением атомов брома:
CF3Br + hn ® CF3 + Br×;
CF2ClBr + hn ® ×CF2Cl + Br×.
Выделяющийся из морской воды, а также используемый в качестве фунгицида бромистый водород частично распадается в тропосфере в результате взаимодействия с радикалами гидроксила. Однако скорость этой реакции мала, и время жизни СН3Br достаточно для того, чтобы значительная часть его проникла через тропопаузу. Органические соединения брома разлагаются уже в нижней стратосфере, поэтому роль атомов Br особенно велика в химических процессах, протекающих на высотах 12–15 км. Разрушение озона и регенерация активного брома происходят в реакциях
Bi× + O3 ® BrO + O2; BrO + O× ® Br× + O2.
Считается, что бромный цикл наиболее эффективен по отношению к озону [15]. Это объясняется, во-первых, малыми скоростями реакций атомов брома и BrO, приводящих к неактивным резервуарным газам (HBr, BrONO2, HOBr). Во-вторых, образовавшиеся в этих реакциях соединения распадаются легче, чем их хлорсодержащие аналоги. Наконец, оксид брома реагирует с ClO в результате чего возникают две активные частицы – атомы хлора и брома:
ClO + BrO ® Cl× + Br× + O2.
Таким образом, разрушение стратосферного озона происходит с участием множества радикалов.
При этом отдельные циклы действуют не изолированно, а взаимодействуют между собой. Укажите эти циклы…
[1] 3CCl4 + 2SbF3 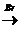 3CCl2F2 + 2SbCl3;
3CCl2F2 + 2SbCl3;
[2] BrO + BrO ® 2 Br× + O2;
[3] ClO + NO2 ® ClONO2;
[4] CCl4 + 2HF  CCl2F2 + 2HCl.
CCl2F2 + 2HCl.
|
из
5.00
|
Обсуждение в статье: Влияние различных загрязнителей атмосферы на озон |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

