 |
Главная |
Антибиотики. Классификация по химической структуре , по механизму и спектру действия.
|
из
5.00
|
За тот период, который прошел со времени открытия П.Эрлиха, было получено более 10 000 различных антибиотиков, поэтому важной проблемой являлась систематизация этих препаратов. В настоящее время существуют различные классификации антибиотиков, однако ни одна из них не является общепринятой.
В основу главной классификации антибиотиков положено их химическое строение.
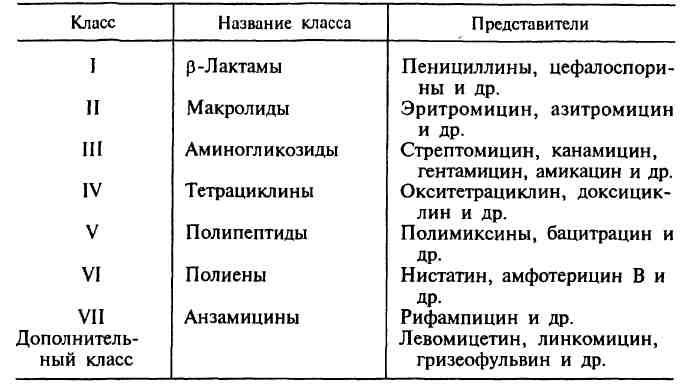
Наиболее важными классами синтетических антибиотиков являются хинолоны и фторхинолоны (например, ципрофлоксацин), сульфаниламиды (сульфадиметоксин), имидазолы (метронидазол), нитрофураны (фурадонин, фурагин).
По спектру действия антибиотики делят на пять групп в зависимости от того, на какие микроорганизмы они оказывают воздействие. Кроме того, существуют противоопухолевые антибиотики, продуцентами которых также являются актиномицеты. Каждая из этих групп включает две подгруппы: антибиотики широкого и узкого спектра действия.
Антибактериальные антибиотики составляют самую многочисленную группу препаратов. Преобладают в ней антибиотики широкого спектра действия, оказывающие влияние на представителей всех трех отделов бактерий. К антибиотикам широкого спектра действия относятся аминогликозиды, тетрациклины и др. Антибиотики узкого спектра действия эффективны в отношении небольшого круга бактерий, например полет-миксины действуют на грациликутные, ванкомицин влияет на грамположительные бактерии.
В отдельные группы выделяют противотуберкулезные, противолепрозные, противосифилитические препараты.
Противогрибковые антибиотики включают значительно меньшее число препаратов. Широким спектром действия обладает, например, амфотерицин В, эффективный при кандидозах, бластомикозах, аспергиллезах; в то же время нистатин, действующий на грибы рода Candida, является антибиотиком узкого спектра действия.
Антипротозойные и антивирусные антибиотики насчитывают небольшое число препаратов.
Противоопухолевые антибиотики представлены препаратами, обладающими цитотоксическим действием. Большинство из них применяют при многих видах опухолей, например митомицин С.
Действие антибиотиков на микроорганизмы связано с их способностью подавлять те или иные биохимические реакции, происходящие в микробной клетке.
В зависимости от механизма действия различают пять групп антибиотиков:
1. антибиотики, нарушающие синтез клеточной стенки. К этой группе относятся, например, β-лактамы. Препараты этой группы характеризуются самой высокой избирательностью действия: они убивают бактерии и не оказывают влияния на клетки микроорганизма, так как последние не имеют главного компонента клеточной стенки бактерий — пептидогликана. В связи с этим β -лактамные антибиотики являются наименее токсичными для макроорганизма;
2. антибиотики, нарушающие молекулярную организацию и синтез клеточных мембран. Примерами подобных препаратов являются полимиксины, полиены;
3. антибиотики, нарушающие синтез белка; это наиболее многочисленная группа препаратов. Представителями этой группы являются аминогликозиды, тетрациклины, макроли-ды, левомицетин, вызывающие нарушение синтеза белка на разных уровнях;
4. антибиотики — ингибиторы синтеза нуклеиновых кислот. Например, хинолоны нарушают синтез ДНК, рифампицин — синтез РНК;
5. антибиотики, подавляющие синтез пуринов и аминокислот. К этой группе относятся, например, сульфаниламиды.
37 Осложнения антибиотикотерапии, их предупреждение.
Как и всякие лекарственные средства, практически каждая группа антимикробных химиопрепаратов может оказывать побочное действие, причем и на макроорганизм, и на микробы, и на другие лекарственные средства.
Осложнения со стороны макроорганизма
Наиболее частыми осложнениями антимикробной химиотерапии являются:
Токсическое действие препаратов. Как правило, развитие этого осложнения зависит от свойств самого препарата, его дозы, способа введения, состояния больного и проявляется только при длительном и систематическом применении антимикробных химиотерапевтических препаратов, когда создаются условия для их накопления в организме. Особенно часто такие осложнения бывают, когда мишенью действия препарата являются процессы или структуры, близкие по составу или строению к аналогичным структурам клеток макроорганизма. Токсическому действию антимикробных препаратов особенно подвержены дети, беременные, а также пациенты с нарушением функций печени, почек.
Побочное токсическое влияние может проявляться как нейротоксическое (например, гликопептиды и аминогликозиды оказывают ототоксическое действие, вплоть до полной потери слуха за счет воздействия на слуховой нерв); нефротоксическое (полиены, полипептиды, аминогликозиды, макролиды, гликопептиды, сульфаниламиды); общетоксическое (противогрибковые препараты — полиены, имидазолы); угнетение кроветворения (тетрациклины, сульфаниламиды, левомицетин/хлорамфеникол, который содержит нитробензен — супрессор функции костного мозга); тератогенное [аминогликозиды, тетрациклины нарушают развитие костей, хрящей у плода и детей, формирование зубной эмали (коричневая окраска зубов), левомицетин/хлорамфеникол токсичен для новорожденных, у которых ферменты печени не полностью сформированы («синдром серого ребенка»), хинолоны — действуют на развивающуюся хрящевую и соединительную ткани].
Предупреждение осложнений состоит в отказе от противопоказанных данному пациенту препаратов, контроле за состоянием функций печени, почек и т. п.
Дисбиоз (дисбактериоз). Антимикробные химиопрепараты, особенно широкого спектра, могут воздействовать не только на возбудителей инфекций, но и на чувствительные микроорганизмы нормальной микрофлоры. В результате формируется дисбиоз, поэтому нарушаются функции ЖКТ, возникает авитаминоз и может развиться вторичная инфекция (в том числе эндогенная, например кандидоз, псевдомембранозный колит). Предупреждение последствий такого рода осложнений состоит в назначении, по возможности, препаратов узкого спектра действия, сочетании лечения основного заболевания с противогрибковой терапией (например, назначением нистатина), витаминотерапей, применением эубиотиков и т. п.
Отрицательное воздействие на иммунную систему.К этой группе осложнений относят прежде всего аллергические реакции. Причинами развития гиперчувствительности может быть сам препарат, продукты его распада, а также комплекс препарата с сывороточными белками. Возникновение такого рода осложнений зависит от свойств самого препарата, от способа и кратности его введения, индивидуальной чувствительности пациента к препарату. Аллергические реакции развиваются примерно в 10 % случаев и проявляются в виде сыпи, зуда, крапивницы, отека Квинке. Относительно редко встречается такая тяжелая форма проявления аллергии, как анафилактический шок. Такое осложнение чаще дают бета-лактамы (пенициллины), рифамицины. Сульфаниламиды могут вызвать гиперчувствительность замедленного типа. Предупреждение осложнений состоит в тщательном сборе аллергоанамнеза и назначении препаратов в соответствии с индивидуальной чувствительностью пациента. Кроме того, антибиотики обладают некоторым иммунодепрессивным действием и могут способствовать развитию вторичного иммунодефицита и ослаблению напряженности иммунитета.
Эндотоксический шок (терапевтический).Это явление, которое возникает при лечении инфекций, вызванных грамотрицательными бактериями. Введение антибиотиков вызывает гибель и разрушение клеток и высвобождение больших количеств эндотоксина. Это закономерное явление, которое сопровождается временным ухудшением клинического состояния больного.
Взаимодействие с другими препаратами.Антибиотики могут способствовать потенцированию действия или инактивации других препаратов (например, эритромицин стимулирует выработку ферментов печени, которые начинают ускоренно метаболизировать лекарственные средства разного назначения).
Побочное воздействие на микроорганизмы.
Применение антимикробных химиопрепа-ратов оказывает на микробы не только прямое угнетающее или губительное воздействие, но также может привести к формированию атипичных форм микробов (например, к образованию L-форм бактерий или изменению других свойств микробов, что значительно затрудняет диагностику инфекционных заболеваний) и персистирующих форм микробов. Широкое использование антимикробных лекарственных средств ведет также к формированию антибиотикозависимости (редко) и лекарственной устойчивости — антибиотикорезистентности (достаточно часто).
38 Механизмы лекарственной устойчивости возбудителей инфекционных болезней. Пути ее преодоления.
Антибиотикорезистентность — это устойчивость микробов к антимикробным химиопрепаратам. Бактерии следует считать резистентными, если они не обезвреживаются такими концентрациями препарата, которые реально создаются в макроорганизме. Резистентность может быть природной и приобретенной.
Природная устойчивость. Некоторые виды микробов природно устойчивы к определенным семействам антибиотиков или в результате отсутствия соответствующей мишени (например, микоплазмы не имеют клеточной стенки, поэтому не чувствительны ко всем препаратам, действующим на этом уровне), или в результате бактериальной непроницаемости для данного препарата (например, грамотрицательные микробы менее проницаемы для крупномолекулярных соединений, чем грамположительные бактерии, так как их наружная мембрана имеет «маленькие» поры).
Приобретенная устойчивость. Приобретение резистентности — это биологическая закономерность, связанная с адаптацией микроорганизмов к условиям внешней среды. Она, хотя и в разной степени, справедлива для всех бактерий и всех антибиотиков. К химиопрепаратам адаптируются не только бактерии, но и остальные микробы — от эукариотических форм (простейшие, грибы) до вирусов. Проблема формирования и распространения лекарственной резистентности микробов особенно значима для внутрибольничных инфекций, вызываемых так называемыми «госпитальными штаммами», у которых, как правило, наблюдается множественная устойчивость к антибиотикам (так называемая полирезистентность).
Генетические основы приобретенной резистентности. Устойчивость к антибиотикам определяется и поддерживается генами резистентности (r-генами) и условиями, способствующими их распространению в микробных популяциях. Приобретенная лекарственная устойчивость может возникать и распространяться в популяции бактерий в результате:
•мутаций в хромосоме бактериальной клетки с последующей селекцией (т. е. отбором) мутантов.Особенно легко селекция происходит в присутствии антибиотиков, так как в этих условиях мутанты получают преимущество перед остальными клетками популяции, которые чувствительны к препарату. Мутации возникают независимо от применения антибиотика, т. е. сам препарат не влияет на частоту мутаций и не является их причиной, но служит фактором отбора. Далее резистентные клетки дают потомство и могут передаваться в организм следующего хозяина (человека или животного), формируя и распространяя резистентные штаммы. Мутации могут быть: 1) единичные (если мутация произошла в одной клетке, в результате чего в ней синтезируются измененные белки) и 2) множественные (серия мутаций, в результате чего изменяется не один, а целый набор белков, например пени-циллинсвязывающих белков у пенициллин-резистентного пневмококка);
• переноса трансмиссивных плазмид резистентности (R-плазмид).Плазмиды резистентности (трансмиссивные) обычно кодируют перекрестную устойчивость к нескольким семействам антибиотиков. Впервые такая множественная резистентность была описана японскими исследователями в отношении кишечных бактерий. Сейчас показано, что она встречается и у других групп бактерий. Некоторые плазмиды могут передаваться между бактериями разных видов, поэтому один и тот же ген резистентности можно встретить у бактерий, таксономически далеких друг от друга. Например, бета-лактамаза, кодируемая плазмидой ТЕМ-1, широко распространена уграмотрицательных бактерий и встречается укишечной палочки и других кишечных бактерий, а также у гонококка, резистентного кпенициллину, и гемофильной палочки, резистентной к ампициллину;
• переноса транспозонов, несущих r-гены(или мигрирующих генетических последовательностей). Транспозоны могут мигрировать с хромосомы на плазмиду и обратно, а также с плазмиды на другую плазмиду. Таким образом гены резистентности могут передаваться далее дочерним клеткам или при рекомбинации другим бактериям-реципиентам.
Реализация приобретенной устойчивости. Изменения в геноме бактерий приводят к тому, что меняются и некоторые свойства бактериальной клетки, в результате чего она становится устойчивой к антибактериальным препаратам. Обычно антимикробный эффект препарата осуществляется таким образом: агент должен связаться с бактерией и пройти сквозь ее оболочку, затем он должен быть доставлен к месту действия, после чего препарат взаимодействует с внутриклеточными мишенями. Реализация приобретенной лекарственной устойчивости возможна на каждом из следующих этапов:
• модификация мишени.Фермент-мишень может быть так изменен, что его функции не нарушаются, но способность связываться с химиопрепаратом (аффинность) резко снижается или может быть включен «обходной путь» метаболизма, т. е. в клетке активируется другой фермент, который не подвержен действию данного препарата.
• «недоступность» мишениза счет снижения проницаемости клеточной стенки и клеточных мембран или «эффлюко-механизма, когда клетка как бы «выталкивает» из себя антибиотик.
• инактивация препарата бактериальными ферментами.Некоторые бактерии способны продуцировать особые ферменты, которые делают препараты неактивными (например, бета-лактамазы, аминогликозид-модифицирующие ферменты, хлорамфениколацетилтрансфераза). Бета-лактамазы — это ферменты, разрушающие бета-лактамное кольцо с образованием неактивных соединений. Гены, кодирующие эти ферменты, широко распространены среди бактерий и могут быть как в составе хромосомы, так и в составе плазмиды.
Для борьбы с инактивирующим действием бета-лактамаз используют вещества — ингибиторы (например, клавулановую кислоту, сульбактам, тазобактам). Эти вещества содержат в своем составе бета-лактамное кольцо и способны связываться с бета-лактамазами, предотвращая их разрушительное действие на бета-лактамы. При этом собственная антибактериальная активность таких ингибиторов низкая. Клавулановая кислота ингибирует большинство известныхбета-лактамаз. Ее комбинируют с пеницил-линами: амоксициллином, тикарциллином, пиперациллином.
Предупредить развитие антибиотикорезистентности у бактерий практически невозможно, но необходимо использовать антимикробные препараты таким образом, чтобы не способствовать развитию и распространению устойчивости (в частности, применять антибиотики строго по показаниям, избегать их использования с профилактической целью, через 10—15 дней ан-тибиотикотерапии менять препарат, по возможности использовать препараты узкого спектра действия, ограниченно применять антибиотики в ветеринарии и не использовать их как фактор роста).
39 Методы определения чувствительности бактерий к антибиотикам.
Для определения чувствительности бактерий к антибиотикам (антибиотикограммы)обычно применяют:
• Метод диффузии в агар. На агаризованную питательную среду засевают исследуемый микроб, а затем вносят антибиотики. Обычно препараты вносят или в специальные лунки в агаре, или на поверхности посева раскладывают диски с антибиотиками («метод дисков»). Учет результатов проводят через сутки по наличию или отсутствию роста микробов вокруг лунок (дисков). Метод дисков — качественныйи позволяет оценить, чувствителен или устойчив микроб к препарату.
Определение чувствительности бактерий к антибиотикам методом дисков.Исследуемую бактериальную культуру засевают газоном на питательный агар или среду АГВ в чашке Петри.
Среда АГВ: сухой питательный рыбный бульон, агар-агар, натрий фосфат двузамещенный. Среду готовят из сухого порошка в соответствии с инструкцией.
На засеянную поверхность пинцетом помещают на одинаковом расстоянии друг от друга бумажные диски, содержащие определенные дозы разных антибиотиков. Посевы инкубируют при 37 °С до следующего дня. По диаметру зон задержки роста исследуемой культуры бактерий судят о ее чувствительности к антибиотикам.
Для получения достоверных результатов необходимо применять стандартные диски и питательные среды, для контроля которых используются эталонные штаммы соответствующих микроорганизмов. Метод дисков не дает надежных данных при определении чувствительности микроорганизмов к плохо диффундирующим в агар полипептидным антибиотикам (например, полимиксин, ристомицин). Если эти антибиотики предполагается использовать для лечения, рекомендуется определять чувствительность микроорганизмов методом серийных разведений.
Определение чувствительности бактерий к антибиотикам методом серийных разведений.Данным методом определяют минимальную концентрацию антибиотика, ингибирующую рост исследуемой культуры бактерий. Вначале готовят основной раствор, содержащий определенную концентрацию антибиотика (мкг/мл или ЕД/мл) в специальном растворителе или буферном растворе. Из него готовят все последующие разведения в бульоне (в объеме 1 мл), после чего к каждому разведению добавляют 0,1 мл исследуемой бактериальной суспензии, содержащей 106—107 бактериальных клеток в 1 мл. В последнюю пробирку вносят 1 мл бульона и 0,1 мл суспензии бактерий (контроль культуры). Посевы инкубируют при 37 °С до следующего дня, после чего отмечают результаты опыта по помутнению питательной среды, сравнивая с контролем культуры. Последняя пробирка с прозрачной питательной средой указывает на задержку роста исследуемой культуры бактерий под влиянием содержащейся в ней минимальной ингибирующей концентрации (МИК) антибиотика.
Оценку результатов определения чувствительности микроорганизмов к антибиотикам проводят по специальной готовой таблице, которая содержит пограничные значения диаметров зон задержки роста для устойчивых, умеренно устойчивых и чувствительных штаммов, а также значения МИК антибиотиков для устойчивых и чувствительных штаммов.
К чувствительным относятся штаммы микроорганизмов, рост которых подавляется при концентрациях препарата, обнаруживаемых в сыворотке крови больного при использовании обычных доз антибиотиков. К умеренно устойчивым относятся штаммы, для подавления роста которых требуются концентрации, создающиеся в сыворотке крови при введении максимальных доз препарата. Устойчивыми являются микроорганизмы, рост которых не подавляется препаратом в концентрациях, создаваемых в организме при использовании максимально допустимых доз.
40 Принципы рациональной антибиотикотерапии.
Профилактика развития осложнений состоит прежде всего в соблюдении принципов рациональной антибиотикотерапии(антимикробной химиотерапии):
• Микробиологический принцип.До назначения препарата следует установить возбудителя инфекции и определить его индивидуальную чувствительность к антимикробным химиотерапевтическим препаратам. По результатам антибиотикограммы больному назначают препарат узкого спектра действия, обладающий наиболее выраженной активностью в отношении конкретного возбудителя, в дозе, в 2—3 раза превышающей минимальную ингибирующую концентрацию. Если возбудитель пока неизвестен, то обычно назначают препараты более широкого спектра, активные в отношении всех возможных микробов, наиболее часто вызывающих данную патологию. Коррекцию лечения проводят с учетом результатов бактериологического исследования и определения индивидуальной чувствительности конкретного возбудителя (обычно через 2-3 дня). Начинать лечение инфекции нужно как можно раньше (во-первых, в начале заболевания микробов в организме меньше, во-вторых, препараты активнее действуют на растущих и размножающихся микробов).
• Фармакологический принцип.Учитывают особенности препарата — его фармакокинетику и фармакодинамику, распределение в организме, кратность введения, возможность сочетания препаратов и т. п. Дозы препаратов должны быть достаточными для того, чтобы обеспечить в биологических жидкостях и тканях микробостатические или микробоцидные концентрации. Необходимо представлять оптимальную продолжительность лечения, так как клиническое улучшение не является основанием для отмены препарата, потому что в организме могут сохраняться возбудители и может быть рецидив болезни. Учитывают также оптимальные пути введения препарата, так как многие антибиотики плохо всасываются из ЖКТ или не проникают через гематоэнцефалический барьер.
• Клинический принцип.При назначении препарата учитывают, насколько безопасным он будет для данного пациента, что зависит от индивидуальных особенностей состояния больного (тяжесть инфекции, иммунный статус, пол, наличие беременности, возраст, состояние функции печени и почек, сопутствующие заболевания и т.п.) При тяжелых, угрожающих жизни инфек-циях особое значение имеет своевременная ан-тибиотикотерапия. Таким пациентам назначают комбинации из двух-трех препаратов, чтобы обеспечить максимально широкий спектр действия. При назначении комбинации из нескольких препаратов следует знать, насколько эффективным против возбудителя и безопасным для пациента будет сочетание данных препаратов, т. е. чтобы не было антагонизма лекарственных средств в отношении антибактериальной активности и не было суммирования их токсических эффектов.
• Эпидемиологический принцип.Выбор препарата, особенно для стационарного больного, должен учитывать состояние резистентности микробных штаммов, циркулирующих в данном отделении, стационаре и даже регионе. Следует помнить, что антибиотикоре-зистентность может не только приобретаться, но и теряться, при этом восстанавливается природная чувствительность микроорганизма к препарату. Не изменяется только природная устойчивость.
• Фармацевтический принцип.Необходимо учитывать срок годности и соблюдать правила хранения препарата, так как при нарушении этих правил антибиотик может не только потерять свою активность, но и стать токсичным за счет деградации. Немаловажна также и стоимость препарата.
|
из
5.00
|
Обсуждение в статье: Антибиотики. Классификация по химической структуре , по механизму и спектру действия. |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

