 |
Главная |
Определение pH стандартных буферных растворов
|
из
5.00
|
Используемые в качестве эталонов для измерений растворы введены давно. Одним из первых таких стандартных растворов использовали «буфер» Вейбеля, представлявший собой раствор 0.01 н. относительно HCl и 0.09 н.-KCl. Величину раН+ рассчитывали разными методами и приписывали различные значения. Кроме этого «буферного раствора» в литературе рекомендуются наборы буферных растворов, имеющих значения рН от 2 до 9, а также универсальные буферные растворы, оценка рН которых производилась разными авторами по-разному.
Не было единой точки, зрения на методику измерений. Таким образом, различия в полученных значениях инструментальных величин рН для одного и того же исследуемого раствора доходили до 0,1, а иногда и более единиц рН.
Однако рекомендованные буферные растворы обладали большой величиной буферной емкости ( 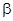 ), количественно характеризуемой значением производной
), количественно характеризуемой значением производной 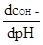 и численно выражаемой количеством эквивалентов щелочи на 1 литр раствора, необходимым для изменения рН
и численно выражаемой количеством эквивалентов щелочи на 1 литр раствора, необходимым для изменения рН
раствора на единицу. Растворы использовались чаще всего как среда с постоянной величиной рН, хорошо сохраняющая это постоянство, но
само численное значение рН оценивалось приближенно.
Начиная с 1950 г. появились работы Бейтса и сотр., в которых поднят вопрос об оценке величины рН таких образцовых растворов и о требованиях, которым должны отвечать сами растворы и вещества, из которых их изготавливают. Эти требования сводятся к следующим:
1) для изготовления буферных образцовых растворов вещества должны быть подобраны так, чтобы обеспечить определенное и не обязательно максимальное значение буферной емкости раствора;
2) вещества должны быть такими, чтобы их легко можно было получать в чистом виде (это обеспечивает возможность получения растворов с хорошо воспроизводимыми значениями рН);
3) для определения величин paH+буферных образцовых растворов следует использовать измерение э. д. с. цепей без переноса типа :
Pt(H2) |буферный раствор + Cl-|AgCl, Ag (3.2.1)
и расчетные методы для определения коэффициентов активности отдельного иона.
Метод расчета paH+ растворов, предложенный в работах Бейтса и сотр., заключался в том, что по величинам э. д. с. цепи (3.2.1)
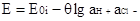 (3.2.2)
(3.2.2)
измеренным в буферных растворах с различным содержанием хлорид-ионов и стандартной э. д. с. этой цепи E0i можно найти величину
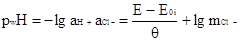 (3.2.3)
(3.2.3)
где mCl- - концентрация хлорид - иона в буферном растворе.
Экстраполируя величину pwH на нулевое содержание хлорид - иона в растворе, можно получить значение pwH0 , отвечающее величине 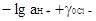 , где
, где 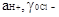 - соответственно активность иона водорода и коэффициент активности хлорид - иона при ионной силе буферного раствора, не содержащего добавок хлорида. Из последнего по соотношению
- соответственно активность иона водорода и коэффициент активности хлорид - иона при ионной силе буферного раствора, не содержащего добавок хлорида. Из последнего по соотношению
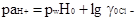 (3.2.4)
(3.2.4)
рассчитывается искомая величина. Коэффициент активности 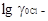 определяется по уравнению Дебая
определяется по уравнению Дебая
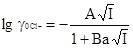 (3.2.5)
(3.2.5)
где А, В - дебаевские коэффициенты; а - расстояние наибольшего сближения ионов; I— ионная сила буферного раствора.
Наибольшим недостатком предложенного метода расчета 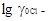 (количественное соответствие между рассчитанной величиной и ее истинным значением) является неопределенность параметра а. В связи с этим Бейтс ограничил применение описанного метода буферными растворами с ионной силой не более 0,1. При этом проверка показала, что вариации параметра а в физически разумных границах 4-6 ангстрем изменяют величину раН+ на 0,01 единицы рН, что лежит в пределах погрешности самой определяемой экспериментально величины рwН.
(количественное соответствие между рассчитанной величиной и ее истинным значением) является неопределенность параметра а. В связи с этим Бейтс ограничил применение описанного метода буферными растворами с ионной силой не более 0,1. При этом проверка показала, что вариации параметра а в физически разумных границах 4-6 ангстрем изменяют величину раН+ на 0,01 единицы рН, что лежит в пределах погрешности самой определяемой экспериментально величины рwН.
Не имея возможности проверить определяемое значение раН+ буферного раствора экспериментально, мы не можем согласиться с тем, что это значение нужно рассматривать только как некую условно приписанную данному буферному раствору величину.
Исследования Бейтса и сотр. положили начало практическим работам по стандартизации величины раН+Шкала кислотности водных растворов былареализована в виде набора буферных растворов, охватывающих интервал рН от 1 до 12..
Вопрос о величинах диффузионных потенциалов неизбежных спутников измерений э. д. с. в цепях с жидкостными границами не был решен. Бейтс и сотр. исследовали остаточные диффузионные потенциалы, использовав разработанные буферные растворы и выбрав один из них в качестве основного стандарта. Результаты показали, что погрешности в определении раН+ «исследуемого» раствора по отношению к выбранному за стандарт не превышали 0,01 единицы рН в том случае, если значения раН+исследуемого раствора отличались от стандартного в кислую сторону более, чем на 4 единицы, а в щелочную - на 3 единицы рН. Для более щелочных растворов погрешности, связанные с наличием остаточного диффузионного потенциала, превышали 0,01.
Из сказанного выше следует, что рассматриваемый метод стандартизации измерений рН (оценка раН+ буферных растворов) не является
безукоризненным.
Пользуясь этим приемом, нельзя создать образцовые буферные растворы с ионной силой более 0,1, так как в этом случае уравнение Дебая не может быть применено для расчета коэффициента активности хлорид - иона. Кроме того, некоторые исследователи не согласны с тем, что предлагается несколько первичных стандартов, а не один, по отношению к которому и производятся все измерения. Неопределенность параметра ав уравнении Дебая также вызывает трудности.
Н. П. Комарь предложил иной метод так называемой «юстировки» рН-метрических цепей, который, как казалось раньше, не только решает проблему создания образцовых растворов с большой ионной силой, но и открывает пути экспериментального определения коэффициентов активности отдельного вида ионов.
Сущность метода заключается в следующем. Электродвижущая сила цепи, обычно применяемой для измерения рН:
Электрод, обратимый к Н+|HCl(mHCl) |KCl|AgCl,Ag (3.2.6)
может быть представлена уравнением
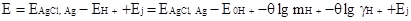 (3.2.7)
(3.2.7)
Считая хлористый водород полностью диссоциированным на ионы, можно вместо mH+в уравнение (38) подставить концентрацию mHCl.
Тогда мы приходим к уравнению



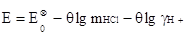 (3.2.8)
(3.2.8)
где 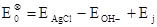 .И, наконец, представляя
.И, наконец, представляя 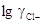 как функцию ионной силы I в виде полинома
как функцию ионной силы I в виде полинома
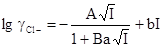 (3.2.9)
(3.2.9)
можно прийти к выражению для э.д.с. цепи (37):
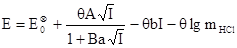 (3.2.10)
(3.2.10)
Оставляя постоянной концентрацию хлористого водорода и меняя ионную силу в растворе добавкой постороннего (фонового) электролита, например, соли (КС1, KNО3, NaCl), можно получить ряд значений Ецепи с определенным ионным фоном.
Это позволяет, используя способ наименьших квадратов, определить постоянные уравнения (3.2.10) - 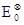 , а и b.
, а и b.
Зная эти параметры, можно по уравнению (3.2.10) рассчитать 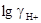 для любой ионной силы и найти величину
для любой ионной силы и найти величину 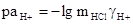 для всех исследуемых растворов.
для всех исследуемых растворов.
Таким образом, любой из исследованных растворов с любой интересующей нас ионной силой может быть использован для «юстировки» цепи (3.2.6) по этим растворам.
Достаточно один раз измерить э. д. с. цепи типа (3.2.6) (уже с другими электродами) в растворе с рассчитанным ранее значением paH+ для вычисления Е0, и такую цепь можно использовать для определения paH+ неизвестных растворов.
Преимуществом этого метода является то, что параметры а и b в уравнении дебаевского типа вычисляются по экспериментальным данным. При этом устраняется неопределенность при нахождении а в уравнении Дебая по методу, описанному ранее.
Однако метод, предложенный Н. П. Комарем, не лишен некоторых недостатков. Так, для определения из экспериментальных данных коэффициентов активности отдельного вида ионов он сделал допущение, что диффузионный потенциал Еjне зависит от ионной силы раствора. Поэтому полученные коэффициенты активности не могут рассматриваться как величины, найденные без каких - либо нетермодинамических допущений, т.е. нельзя считать, что paH+ стандартного раствора не содержат никаких погрешностей. Кроме того, при измерении рН исследуемых растворов не. исключаются погрешности, связанные с наличием остаточных диффузионных потенциалов, так как из двух измерений э. д. с. цепи (со стандартным раствором для определения Е0и с исследуемым) мы фактически используем для расчета э. д. с. цепи, аналогичной цепи :
Pt(H2) | 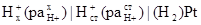
При этом остаточный диффузионный потенциал 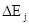 , равный разности диффузионных потенциалов Ej на границах исследуемый раствор- раствор соединительного моста, соединительный раствор - стандартный раствор, искажает инструментальную величину рН.
, равный разности диффузионных потенциалов Ej на границах исследуемый раствор- раствор соединительного моста, соединительный раствор - стандартный раствор, искажает инструментальную величину рН.
Таким образом, применение метода Н. П. Комаря хотя и позволяет использовать в качестве стандартов растворы с известным раH+ с различными ионными силами на различных ионных фонах, но не устраняет ошибок, связанных с остаточным диффузионным потенциалом.
Кроме того, наборы таких растворов (с известным раH++ и ионными силами от ~0,01 до ~3,5 mимеют значения раH+, не сильно отличающиеся друг от друга (на 0,5 - 1,0 единиц) с абсолютными величинами - в кислой области около 2, в щелочной - около 12. Значит, по величине раH+ они могут существенно отличаться от рН исследуемого раствора, что, в свою очередь, увеличивает остаточный диффузионный потенциал.
Оптимальным условием для определения рН исследуемых растворов и снижения остаточного диффузионного потенциала до нуля было бы равенство стандартного и исследуемого растворов, по раH+, ионной силе и составу фонов. Однако в практике измерения рН такое невозможно.
Сопоставления результатов измерения рН некоторых модельных растворов, проведенные этими методами, показали, что результаты незначительно отличаются друг от друга, что и следовало ожидать, поскольку в основу положено уравнение одного типа (Дебаевское), а погрешности за счет диффузионных потенциалов различаются несущественно, и уточнения за счет величины параметра а не выходят за пределы погрешности метода (приблизительно 0,01 ед. рН).
ВЫВОД:
В работе были изучены методы определения кислотности неводных растворов, стандартизация ее измерения. Рассмотрены методы определения pH стандартных буферных растворов в соответствии с допустимыми погрешностями.
СПИСОК ЛИТЕРАТУРЫ:
1. Кислотность неводных растворов. В. В. Александров, 152 с. граф. 20 см., Харьков Вища школа Изд-во при Харьк. ун-те 1981
2. Измайлов Н.А., Электрохимия растворов, 3 изд., испр., М., «Химия», 1976, 488 с.
3. Бейтс Р. Определение pH: Теория и практика. Л.: Химия, 1968, 398 с.
4. Васильев В. П. Аналитическая химия. В 2 кн. Кн. 2. Физико-химические методы анализа: Учеб. для студ. вузов, обучающихся по химико-технол. спец. - 2-е изд., перераб. и доп. - М.:Дрофа, 2002. - 384 с., ил. - с. 191.
5. Кнорре Д. Г., Крылова Л. Ф., Музыкантов В. С. Физическая химия: Учеб. пособие для вузов. - М.: Высш. школа, 1981. - 328 с., ил., с. 263-264.
|
из
5.00
|
Обсуждение в статье: Определение pH стандартных буферных растворов |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

