 |
Главная |
Влияние промежуточных соединений на механизм (порядок) реакции.
|
из
5.00
|
Промежуточные соединения принимают участие в процессе, поэтому механизм реакции со временем меняется, а следовательно, меняется порядок реакции. Для изучения этого влияния определяют временной порядок реакции.
Определить зависимость порядка реакции от времени можно следующим образом:
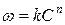 , логарифмируем это выражение и получаем
, логарифмируем это выражение и получаем
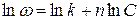 .
.
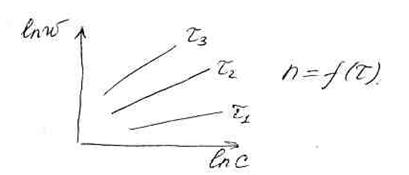
1) Если порядок реакции не зависит от времени ( 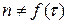 ), то в координатах “
), то в координатах “  ” мы получаем прямую линию, наклон которой неизменен по времени протекания реакции.
” мы получаем прямую линию, наклон которой неизменен по времени протекания реакции.
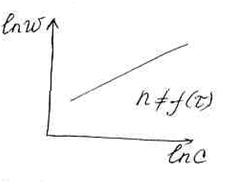
2) Если порядок реакции зависит от времени (  ), то получаем веер прямых с различными углами наклона.
), то получаем веер прямых с различными углами наклона.
ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ.
ПРАВИЛО ВАНТ-ГОФФА. УРАВНЕНИЕ АРРЕНИУСА.
Температурная зависимость для простых реакций выражается правилом Вант-Гоффа.
Правило Вант-Гоффа: для простых гомогенных реакций при увеличении температуры на 100С скорость химической реакции возрастает в 2  4 раза.
4 раза.
Выражается это следующей формулой:
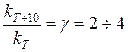
 – температурный коэффициент Вант-Гоффа.
– температурный коэффициент Вант-Гоффа.
Правило Вант-Гоффа в случае изменения температуры более чем на 100С выражается формулой:
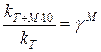 ,
,
где М – коэффициент, кратный 10.
Более того зависимость скорости реакции от температуры определяется уравнением Аррениуса:

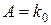 – предэкспоненциальный множитель.
– предэкспоненциальный множитель.
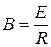 , гдеR – универсальная газовая постоянная, Е – энергия активации.
, гдеR – универсальная газовая постоянная, Е – энергия активации.
Тогда получим следующее выражение:
 уравнение Аррениуса
уравнение Аррениуса
Энергия активации – это минимальная энергия, которой должны обладать молекулы для взаимодействия.
Для реакции АВ+С → АС+В изменение энергии вдоль пути реакции можно представить следующим образом:
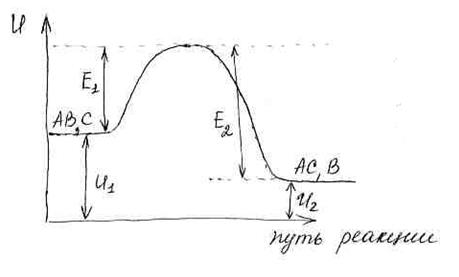
 – внутренняя энергия исходных веществ;
– внутренняя энергия исходных веществ;
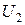 – внутренняя энергия продуктов реакции;
– внутренняя энергия продуктов реакции;
 – энергия активации прямой реакции;
– энергия активации прямой реакции;
 – энергия активации обратной реакции.
– энергия активации обратной реакции.
С увеличением температуры изменяется не энергия активации процесса, а увеличивается потенциальная энергия самих молекул.
 тепловой эффект процесса.
тепловой эффект процесса.
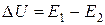
ТЕРМОДИНАМИЧЕСКИЙ ВЫВОД УРАВНЕНИЯ АРРЕНИУСА.
 – уравнение изохоры Вант-Гоффа.
– уравнение изохоры Вант-Гоффа.
 – константа равновесия химической реакции, есть отношение констант скоростей прямой и обратной реакций.
– константа равновесия химической реакции, есть отношение констант скоростей прямой и обратной реакций.
 ;
; 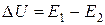 ,
,
тогда 
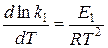 ;
;
 .
.
В общем случае получим уравнение Аррениуса в дифференциальной форме:

Проинтегрируем по температуре:
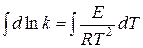
Если энергия активации не зависит от температуры ( 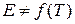 ), то получим:
), то получим:

Обозначим  , получим уравнение Аррениуса в интегральной форме:
, получим уравнение Аррениуса в интегральной форме:
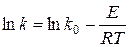
Преобразуем это уравнение и получим уравнение Аррениуса в экспоненциальной форме:

|
из
5.00
|
Обсуждение в статье: Влияние промежуточных соединений на механизм (порядок) реакции. |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

