 |
Главная |
РЕАКЦИИ В РАСТВОРАХ ЭЛЕКТРОЛИТОВ.
|
из
5.00
|
КИНЕТИКА РЕАКЦИЙ В РАСТВОРАХ.
Существует три типа реакций в растворах:
1. Скорость реакции не меняется в зависимости от среды.
2. Скорость реакции зависит от среды (например, 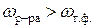 ).
).
3. Реакции в растворах сильных электролитов (  (заряд ионов, ионная сила)).
(заряд ионов, ионная сила)).
I. ПРОТЕКАНИЕ РЕАКЦИИ С ТОЧКИ ЗРЕНИЯ ТАС.
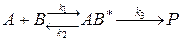
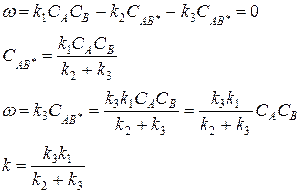
1) Предположим, что:
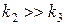 , тогда
, тогда 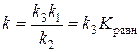
В этом случае скорость определяющей является вторая стадия, и растворитель не оказывает существенного влияния на скорость процесса.
2) 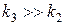 , тогда
, тогда 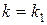
В этом случае скорость определяющей является стадия подвода вещества А к веществу В, которая определяется физическими свойствами среды.
скорость 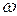
/ \
диффузия вязкость
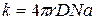
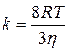
r – расстояние между центрами 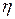 – вязкость среды
– вязкость среды
молекул Аи В
D – коэффициент диффузии
Na – число Авогадро
Таким образом, по ТАС скорость реакции зависит от свойств растворителя в том случае, если скорость определяющей является 1 стадия, т. е. стадия подвода молекул друг к другу.
ПРОТЕКАНИЕ РЕАКЦИИ С ТОЧКИ ЗРЕНИЯ ТЕОРИИ АКТИВИРОВАННОГО КОМПЛЕКСА (ТАК).
В основе этой теории лежит уравнение Эйринга:
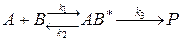
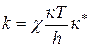 , где
, где 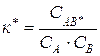
Для реакций в растворе, учитывая взаимодействие молекул с растворителем, мы должны вместо величины концентрации подставить величину активности.
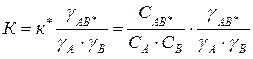 ;
; 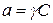
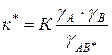
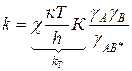 ;
; 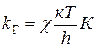
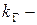 константа скорости в газовой фазе.
константа скорости в газовой фазе.
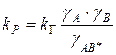 уравнение Бренстеда-Бьеррума
уравнение Бренстеда-Бьеррума
Мономолекулярные реакции.
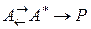
Предполагаем, что 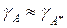 , тогда
, тогда
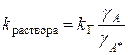
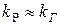
Скорость мономолекулярной реакции не зависит от характера среды.
ПРИМЕР.
Реакция Среда k∙105
Разложение Газовая фаза 3,4
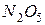 Хлороформ 3,7
Хлороформ 3,7
Дихлорэтан 4,2
Нитроэтан 3,4
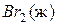 4,1
4,1
Бимолекулярные реакции.
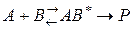
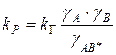 ;
; 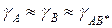
тогда вышеприведенное уравнение будет иметь вид:
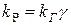
Для медленной реакции Меншуткина
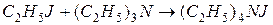
в гексане – 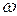
в ацетоне – 100 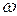
в нитробензоле – 1380 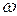
По ТАК важным фактором влияния растворителя на скорость реакции является значение коэффициента активности данного вещества в данной реакции.
РЕАКЦИИ В РАСТВОРАХ ЭЛЕКТРОЛИТОВ.
В разбавленных растворах зависимость коэффициента активности иона от ионной силы раствора описывается уравнением Дебая-Хюккеля:
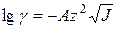 ,
,
где 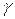 – коэффициент активности;
– коэффициент активности;
А – const, зависящая от растворителя;
z – заряд иона;
J – ионная сила раствора.
Заряд активированного комплекса в этом случае будет равен:
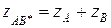
Прологарифмируем уравнение Бренстеда-Бьеррума:
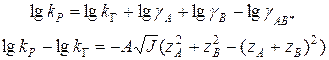
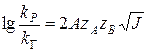 уравнение реакции в растворах электролитов
уравнение реакции в растворах электролитов
Для реакций в растворе электролитов характерно три вида соотношений 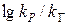 . Рассмотрим все 3 вида. В координатах
. Рассмотрим все 3 вида. В координатах 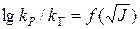 при достаточно малых значениях
при достаточно малых значениях 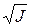 хорошо выполняется линейная зависимость.
хорошо выполняется линейная зависимость.
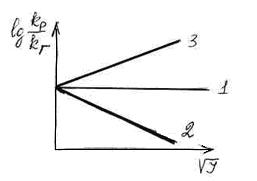
1. Случай 1 наблюдается, если 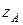 или
или 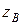 = 0 (т. е. имеются незаряженные частицы одного из веществ). Тогда
= 0 (т. е. имеются незаряженные частицы одного из веществ). Тогда 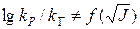 .
.
2. Если заряды разноименные, то при 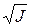 ↑
↑ 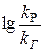 ↓ (при увеличении ионной силы значение
↓ (при увеличении ионной силы значение 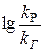 падает).
падает).
3. Если ионы 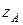 и
и 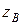 одноименные, то при увеличении ионной силы увеличивается логарифмическое соотношение констант скоростей в газовой фазе и в растворе (
одноименные, то при увеличении ионной силы увеличивается логарифмическое соотношение констант скоростей в газовой фазе и в растворе ( 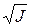 ↑ и
↑ и 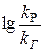 ↑).
↑).
Следует заметить, что данные закономерности соблюдаются лишь в случае сильно разбавленных растворов.
Более сложная зависимость дается уравнением Гаммета.
ЦЕПНЫЕ РЕАКЦИИ.
Цепными называются реакции, при которых одна активная нестабильная частица взаимодействует с веществом с образованием одной или нескольких активных частиц.
Цепные реакции состоят из большого числа повторяющихся стадий:
I. Зарождение цепи.
II. Рост цепи.
III. Обрыв цепи.
По цепному механизму протекают процессы горения, многие фотохимические реакции, некоторые реакции полимеризации и поликонденсации при получении полимеров. По цепному механизму происходит распад ядер урана и плутония в атомных реакторах.
Цепные реакции делят на неразветвленные и разветвленные.
Неразветвленными называют цепные реакции, когда в процессе развития цепи число свободных валентностей в звене цепи остается постоянным.
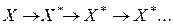
(Боденштейн, 1918 г.)
Разветвленными называют цепные реакции, когда развитие цепи идет с увеличением свободных валентностей в звене цепи.
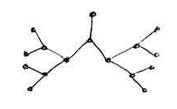
(Семенов Н. Н., 1926 г. Нобелевская премия)
Рассмотрим более подробно все три стадии цепной реакции.
I. Зарождение цепи.
Зарождение цепи начинается с элементарного химического акта, в результате которого в системе появляются частицы со «свободными валентностями» – атомы двухатомной молекулы или радикалы.
Радикальные частицы имеют по одному электрону на ВЗМО и отличаются высокой реакционной способностью.
1. Активные атомы. Например, в смеси 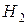 и
и 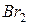 в газообразном состоянии молекулы
в газообразном состоянии молекулы 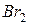 могут частично диссоциировать на атомы.
могут частично диссоциировать на атомы.
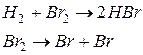
Атомарный бром может быть инициатором цепной реакции.
2. Активные радикалы. Например, при получении полимерных материалов в качестве инициаторов цепной реакции используют перекисные соединения. Пероксид бензоила распадается на радикалы:

Эти радикалы, присоединяясь по двойной связи к мономеру, образуют новую частицу со свободной валентностью.
II. Рост цепи.
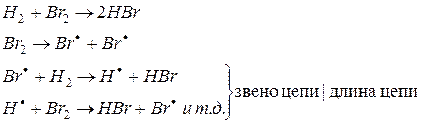
Совокупность последовательных реакций продолжения цепи, из многократного повторения которой складывается цепной процесс, называется звеном цепи.
Длина цепи – число звеньев на стадии продолжения цепи.
III. Обрыв цепи.
1) Обрыв цепи может происходить за счет столкновения радикальных частиц со стенками сосуда
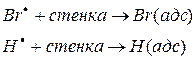
адс – адсорбированный.
2) Дезактивация может произойти за счет тройных соударений с молекулами примесей или инертных газов.
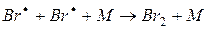
Двойные столкновения к дезактивации не приводят.
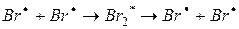
|
из
5.00
|
Обсуждение в статье: РЕАКЦИИ В РАСТВОРАХ ЭЛЕКТРОЛИТОВ. |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

