 |
Главная |
Оксиды и пероксиды щелочных металлов
|
из
5.00
|
Общая характеристика металлов.
Металлы – это элементы, проявляющие в своих соединениях только положительные степени окисления, и в простых веществах которые имеют металлические связи. Металлическая кристаллическая решетка - решетка, образованная нейтральными атомами и ионами металлов, связанными между собой свободными электронами. У металлов в узлах кристаллической решетки находятся атомы и положительные ионы. Электроны, отданные атомами, находятся в общем владении атомов и положительных ионов. Такая связь называется металлической. Для металлов наиболее характерны следующие физические свойства: металлический блеск, твердость, пластичность, ковкость и хорошая проводимость тепла и электричества. Теплопроводность и электропроводность уменьшается в ряду металлов:
Аg Сu Аu Аl Мg Zn Fе РЬ Hg
Многие металлы широко распространены в природе. Так, содержание некоторых металлов в земной коре следующее: алюминия — 8,2%; железа — 4,1%; кальция — 4,1%; натрия — 2,3%; магния — 2,3%; калия - 2,1%; титана — 0,56%.
Большое количество натрия и магния содержится в морской воде: — 1,05%, — 0,12%.
В природе металлы встречаются в различном виде:
— в самородном состоянии: серебро , золото , платина , медь , иногда ртуть
— в виде оксидов: магнетит Fe3O4, гематит Fe2О3 и др.
— в виде смешанных оксидов: каолин Аl2O3 • 2SiO2 • 2Н2О, алунит (Na,K)2O • АlО3 • 2SiO2 и др.
— различных солей:
сульфидов: галенит PbS, киноварь НgS,
хлоридов: сильвин КС1, галит NaCl, сильвинит КСl• NаСl, карналлит КСl • МgСl2 • 6Н2О, сульфатов: барит ВаSO4, ангидрид Са8О4 фосфатов: апатит Са3(РО4)2, карбонатов: мел, мрамор СаСО3, магнезит МgСО3.
Многие металлы часто сопутствуют основным природным минералам: скандий входит в состав оловянных, вольфрамовых руд, кадмий — в качестве примеси в цинковые руды, ниобий и тантал — в оловянные.
Железным рудам всегда сопутствуют марганец, никель, кобальт, молибден, титан, германий, ванадий.
Элементы I группы Li, Na, K, Rb, Cs, Fr
Общая характеристика: К элементам главной подгруппы I-ой группы Периодической системы относятся Li, Na, K, Rb, Cs, Fr. Их принято называть щелочными металлами. История открытия химических элементов IA группы.
Эти металлы в своих рядах являются первыми, т.е. именно у них начинается заполнение электронами нового электронного слоя. Их валентную электронную конфигурацию можно в общем виде обозначить так: ns1, где n - номер периода, в котором находится металл. Плотность, температура плавления, температура кипения простых веществ элементов IA группы.
Щелочные металлы имеют серебристо-белый цвет, а цезий - золотисто-желтый. Хранят щелочные металлы под слоем керосина или бензола. Металлические К, Rb, Cs самопроизвольно загораются на воздухе.
Первый потенциал ионизации, сродство к электрону и электроотрицательность по Полингу атомов элементов IA группы.
При комнатной температуре щелочные металлы находиться в твердом (кристаллическом) состоянии, хотя все они имеют очень невысокую температуру плавления. Первые три металла легче воды и плавают на ее поверхности, вступая в бурную реакцию:
2 Me + 2 H2O = 2 MeOH + H2.
Щелочные металлы самые активные из всех металлов. Поэтому иногда говорят, что атомы щелочных металлов "стремятся отдавать свой валентный электрон, чтобы приобрести устойчивую электронную оболочку инертного газа". Это не совсем так: чтобы у атома щелочного металла отнять электрон и превратить его в положительно заряженный ион:
Me - e + ПИ = Me+
необходимо затратить достаточно большую энергию ПИ (потенциал ионизации). При переходе от Li к Cs она уменьшается и поэтому активность металла, т.е. способность к химическому взаимодействию - увеличивается. И уж совсем неожиданны данные о сродстве к электрону (СЭ) у атомов щелочных металлов: изолированные атомы щелочных металлов "с удовольствием", т.е. с выделением энергии (СЭ) присоединяют к себе электрон:
Me + e = Me- + СЭ.
Отсюда следует очень важный вывод, что поведение изолированных атомов щелочных металлов - это одно, а их поведение в молекулах, т.е. при взаимодействии с атомами других химических элементов - это качественно другая ситуация. В молекулах атомные орбитали преобразовываются в молекулярные орбитали, валентные электроны атомов в молекуле находятся в совместном пользовании или сильно смещаются к одному из атомов вплоть до образования ионной связи.
Типичные степени окисления элементов IA группы в различных соединениях +1. Таким образом, имеются две степени окисления у элементов IA группы: 0 - в молекулах Ме2 и в металлическом состоянии и +1 - в соединениях ( ярко выраженная ионная связь. Очень высокая химическая активность щелочных металлов обусловлена низкими ПИ, легко разрушаемой кристаллической структурой и малой плотностью.
Получение
Li, Na, K (Ме) получают электролизом расплавов их хлоридов или гидроксидов:
2KCl = 2K+ + 2Cl-,
катод 2K+ + 2e = 2K; анод 2Cl- -2e = Cl2.
Температуры плавления хлоридов и гидроксидов щелочных металлов, oС
| Анион | Li | Na | K | Rb | Cs |
| Cl- | 610 | 801 | 776 | 723 | 645 |
| OH- | 473 | 322 | 405 | 385 | 343 |
Гидроксиды МеОН имеют меньшую, чем у хлоридов, температуру плавления, они термически вполне устойчивы, а при электролизе из расплавов идет процесс:
4МеOH = 4Ме + 2H2O + O2.
Используя относительно меньшую, чем у Al, Si, Ca, Mg, температуру кипения, можно получать щелочные металлы восстановлением их из оксидов, хлоридов, карбонатов при высоких температурах:
3Li2O + 2Al 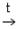 6Li + Al2O3,
6Li + Al2O3,
4NaCl + 3CaO + Si 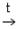 4Na + 2CaCl2 + CaSiO3.
4Na + 2CaCl2 + CaSiO3.
Свойства: Щелочные металлы - очень сильные восстановители. Они энергично реагируют с большинством неметаллов, разлагают воду и бурно взаимодествуют с кислотами. В общем виде (обозначая атом щелочного металла просто Ме) эти реакции будут выглядеть так:
2Me + H2 = 2MeH (гидриды),
2Me + Г2 = 2MeГ (галогениды),
2Me + S = Me2S (сульфиды),
3Me + P = Me3P (фосфиды),
6Me + N2 = 2Me3N (нитриды),
2Me + 2H2O = 2MeOH + H2.
Гидриды щелочных металлов реагируют с водой и кислородом:
MeH + H2O = MeOH + H2,
2MeH + O2 = 2 MeOH.
Из солей щелочных металлов с галогенами гидролизуются только фториды:
MeF + H2O = MeOH + HF.
Li используют в некоторых сплавах и для получения трития в термоядерном синтезе. Na и K применяют для получения Ti, Zr, Nb, Ta:
TiCl4 + 4Na = Ti + 4NaCl.
Li, Na, и K используют в реакциях органического синтезах. Na эффективен при осушке органических растворителей. Сs применяется для изготовления фотоэлементов, так как у его атомов самое малое значение ПИ из всех химических элементов.
Оксиды и пероксиды щелочных металлов
Атомы щелочных металлов (Ме) в соединениях одновалентны. Поэтому общая формула оксидов - Me2O, пероксидов - Me2O2. Приведем перечень всех соединений щелочных металлов с кислородом:
· Li2O,
· Na2O, Na2O2 (пероксид),
· K2O, K2O2 (пероксид), KO2 (надпероксид), KO3 (озонид),
· Rb2O, Rb2O2 (пероксид), RbO2 (надпероксид),
· Cs2O, Cs2O2 (пероксид), CsO2 (надпероксид).
Литий не образует пероксидов, у Na - один пероксид, у K, Rb и Cs есть надпероксиды типа MeO2, у калия известен озонид. Все это надо учитывать при изучении взаимодействия щелочных металлов с кислородом и озоном:
4 Li + O2  2 Li2O,
2 Li2O,
2 Na + O2 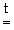 Na2O2,
Na2O2,
K + O2 = KO2.
Оксиды щелочных металлов можно получить из надпероксидов:
2МеO2 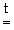 Ме2O2 + О2
Ме2O2 + О2
и пероксидов:
Ме2O2 + 2Ме  2 Ме2O.
2 Ме2O.
Li2О обычно получают при нагревании его карбоната:
Li2CO3  Li2O + CO2.
Li2O + CO2.
Оксиды щелочных металлов, растворяясь в воде, дают щелочи:
Ме2O + H2O = 2 МеOH.
Пероксиды и надпероксиды также реагируют с водой:
Ме2O2 + 2 H2O = 2 МеOH + H2O2,
2 МеO2 + 2 H2O = 2 МеOH + H2O2 + O2,
с кислотными оксидами и кислотами:
Me2O + SO3 = Me2SO4,
Me2O + 2HNO3 = 2MeNO3 + H2O,
Me2O2 + H2SO4 = Me2SO4 + H2O2,
4MeO2 + 2CO2 = 2Me2CO3 + 3O2.
Пероксиды и надпероксиды являются сильными окислителями:
Me2O2 + 2FeSO4 + 2H2SO4 ® Fe2(SO4)3 + Me2SO4 + 2H2O,
но могут и сами окисляться:
5Me2O2 + 2KMnO4 +8H2SO4 ® 2MnSO4 + 5Me2SO4 + K2SO4 + 8H2O + 5O2 .
Надпероксид калия поглощает СО2 и регенерирует кислород:
4KO2 + 2H2O + 2CO2 = 4KHCO3 + O2.
Гидроксиды
Гидроксиды имеют общую формулу МеОН.
Получение
Гидроксиды получают с помощью обменных реакций из сульфатов и карбонатов:
Me2SO4 + Ba(OH)2 = BaSO4¯ + 2 MeOH,
Me2CO3 + Ca(OH)2 = CaCO3¯ + 2 MeOH,
электролизом водных растворов хлоридов щелочных металлов:
2 МеCl + 2 H2O = 2 МеOH + H2 + Cl2,
катод: 2H+ + 2e = H2; анод: 2Cl- - 2e = Cl2.
Свойства
Галогениды щелочных металлов в воде полностью диссоциируют на ионы - это самые сильные основания. Твердые щелочи очень гигроскопичны и это позволяет использовать их в качестве эффективных осушителей. Они энергично взаимодействуют с кислотными и амфотерными оксидами и гидроксидами, с многоосновными кислотами могут давать кислые соли.
2Al + 2 MeOH + 6 H2O = 2Me[Al(OH)4] + 3H2,
Cl2 + 2MeOH = MeCl + MeClO + H2O,
MeOH + HCl = MeCl + H2O,
NH4Cl + MeOH = MeCl + NH3 + H2O,
CuCl2 + 2MeOH = Cu(OH)2¯ + 2MeCl,
NaH2PO4 + NaOH = Na2HPO4 + H2O,
2 MeOH + CO2 = Me2CO3 + H2O,
2 MeOH + H2SO4 = Me2SO4 + 2 H2O.
Натриевые соли очень широко используются в химической промышленности, их применение рассматривается в соответствующих группах неметаллов.
Калийные соли используют как удобрение и при получении стекла.
|
из
5.00
|
Обсуждение в статье: Оксиды и пероксиды щелочных металлов |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

