 |
Главная |
МЕТОД ПОТЕНЦИАЛОВ СОБСТВЕННОЙ ПОЛЯРИЗАЦИИ
|
из
5.00
|
При исследованиях скважин методом потенциалов собственной поляризации (СП) изучают естественные электрические поля, возникающие в скважине и породах в результате физико-химических процессов — диффузии солей в растворах электролитов, фильтрации жидкости, окислительно-восстановительных реакций. Эти процессы порождают потенциалы диффузионные, течения, окислительно - восстановительные. Главную роль в формировании естественных электрических полей в скважине, заполненной буровым раствором на водной основе, играют потенциалы диффузионного происхождения. Исследования методом СП проводят, регистрируя диаграмму изменения по разрезу скважины разности потенциалов между электродом М, перемещающимся по стволу скважины, и электродом N, расположенным на земной поверхности близ устья скважины.
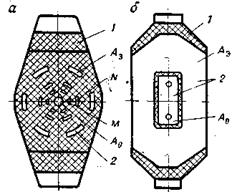
| Рис. 26. Схема расположения электродов на измерительных башмаках бокового микрозонда. Зонд: а - четырехэлектродный; б - двух-электродный; 1 - изоляция; 2 - металл |
Диффузионная ЭДС
При непосредственном контакте растворов электролита различной концентрации на границе растворов в результате диффузии ионов, на которые диссоциирует электролит, из раствора большей концентрации в раствор меньшей, возникает двойной электрический слой с разностью потенциалов Ед:
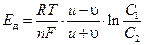 (1.26)
(1.26)
где Ед - диффузионная ЭДС; R - универсальная газовая постоянная; Т - абсолютная температура растворов, K; n - валентность электролита; F - число Фарадея; u и 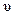 —подвижности катиона и аниона; C1, С2 - концентрация растворов.
—подвижности катиона и аниона; C1, С2 - концентрация растворов.
При данной последовательности индексов при С под знаком логарифма величина Ед, рассчитываемая по формуле (1.26), определяет потенциал раствора «2» по отношению к раствору «1». Если подставить в формулу (1.26) значения констант R, F, величину Т = 293К, соответствующую комнатной температуре t = 20 °C, и перейти от натурального логарифма к десятичному, то для растворов одновалентного электролита n = 1 получим
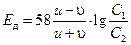 (1.27)
(1.27)
где Ед – выражается в миливольтах
Выражение (1.27) можно записать и так
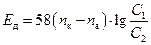 (1.28)
(1.28)
где nк и nа — числа переноса катионов и анионов, характеризующие доли электричества, переносимого при диффузии катионами и анионами.
Обозначив множитель перед логарифмом в формуле (1.28) символом Кд, получим
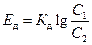 (1.29)
(1.29)
где Кд - коэффициент диффузионной ЭДС.
В пластовых водах нефтяных и газовых месторождений и в буровом растворе наиболее распространенной является поваренная соль NaCl, диссоциирующая в водном растворе на катионы Na+ и анионы С1-. Подставив в формулу (1.27) средние значения подвижностей u = 40,  = 60 для Na+ и С1-, будем иметь
= 60 для Na+ и С1-, будем иметь
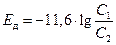 (1.30)
(1.30)
Таким образом, для растворов NaCl при t = 20°С Kд = -11,6 мВ. При контакте растворов NaCl разбавленный раствор С2 заряжается, отрицательно по отношению к более концентрированному раствору С1.
Из выражений (1.27), (1.30) следует, что диффузионная разность потенциалов возникает при различии концентраций C1, С2 и подвижностей u, 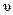 . Величина и знак диффузионной ЭДС зависят при постоянной температуре от химического состава электролитов в растворах и соотношения концентраций граничащих растворов.
. Величина и знак диффузионной ЭДС зависят при постоянной температуре от химического состава электролитов в растворах и соотношения концентраций граничащих растворов.
|
из
5.00
|
Обсуждение в статье: МЕТОД ПОТЕНЦИАЛОВ СОБСТВЕННОЙ ПОЛЯРИЗАЦИИ |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

