 |
Главная |
Приведем конечное уравнение для энергии.
|
из
5.00
|
En = (nn +1/2) hw , где nn = 0, 1,2 …… ¥ колебательное квантовое число

Графики волновых функций и соответствующие собственные значения для низших nn для линейного гармонического осциллятора
Интересно отметить следующие особенности:
- система энергетических уровней дискретна с постоянным интервалом, равным DE = hw .
- Состояние с нулевой энергий отсутствует, и это есть следствие соотношения неопределенностей, так как если частица будет находиться на самом дне потенциальной ямы, то это будет означать, что ее координата и импульс одновременно точно определены, что невозможно.
- Минимальная энергия e0 = ½* hw - называют нулевой энергией.
Задачи на колебательные спектры.
Инфракрасное излучение и колебания молекул
Инфракрасным излучением называют излучение с длинами волн от 0.5 до 1000 мкм. В единицах волновых чисел v0 =1/l , этот интервал составляет 4000-400 см-1
В ИК-диапазоне проявляются переходы между колебательными и вращательными уровнями энергии молекул. Химические связи в молекулах испытывают колебательные движения. Колебательная энергия молекул квантована, т.е. поглощаемая энергия изменяется не непрерывно, а скачкообразно. В результате колебательный (инфракрасный) спектр молекулы представляет собой ряд пиков (полос поглощения), отвечающих разным колебательным энергетическим переходам. Именно в этом диапазоне волновых чисел осуществляют регистрацию ИК-спектров органических и природных соединений .
Задача на гармонический осциллятор на экзамене
1. Рассчитайте область, в которой будут проявляться валентные колебания вязи С-С линейных алканов в sp3- sp3 гибридизации если k = 4,5 *102 н/м
Решение: k = mw2 , где w = 2p*n круговая (циклическая) частота колебаний и
n - частота колебаний. w = 2p n = 2p с/l = 2p сv0 ,
где v0 =1/l - волновое число и скорость света с = 2*108 м/с и
NA = 6,023*1023 г/моль = 6,023*1026 кг/моль
k = mw2 =m4p2 c2v02 ; отсюда
v0 = 1/2p c Ök/m ( в волновых числах)
m = (1/Na) * 12*12/(12+12) = 0,9961 *10-26 кг
v0 = 1,183 *105 м-1 = 1183 см-1
2. Рассчитайте силовую константу для молекулы 1H35Cl , если частота колебания, выраженная в волновых числах равна v0= 2990 см-1 .
Решение. k = mw2 = m4p2 u2 = m4p2 c2/l2 = m4p2 c2v02
m = 1/Na* [M1*M2/(M1+M2)] = 1,615*10-24 г = 1,615*10-27 кг
с = 3*108 м/с v0= 2990 см-1 = 299000 м-1 = 2,99 *105 м-1
k = m4p2 c2v02 =512,48 н/м
3. Рассчитайте область, в которой будут проявляться валентные колебания вязи С-С линейных алканов в sp3- sp3 гибридизации.
По Краткому справочнику физико – химических величин Равделя 1983 стр.187
«Силовые постоянные связей в двухатомных и многоатомных молекул»
находим значение силовой постоянной для sp3- sp3 типа связи
k = 4,5 *102 н/м
Решение: k = m4p2 c2 k = m4p2 c2v02
v0 = 1/2p c Ök/m ( в волновых числах)
m = 1/Na * 12*12/(12+12) = 0,9967 *10-26 кг
v0 = 2 *105 м-1 = 2000 см-1
Волновое число попадает в правильный интервал от 4000 до 400 см-1
Жесткий ротатор
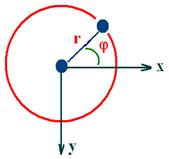
Вращательные спектры. Двухатомную молекулу можно упрощенно рассматривать как модель жесткого ротатора с моментом инерции I. Систему, состоящую из двух масс m1 и m2, находящихся друг от друга на фиксированном расстоянии r, и вращающихся вокруг общего центра масс, называют жестким ротатором.
Момент инерции ротатора I = mr2 , где m = m1 m2/( m1+ m2 ) - приведенная масса
Выражение для энергии вращательного движения имеет вид:
E(J) = (h2/2I)*J(J+1) где J = 0,1,2…. J – вращательное квантовое число
Выражение для волновой функции Ф(j) = А*exp(-imJj)
Имеем два квантовых числа mJ и J, т.к. в модели две переменные j и r, а так как один из параметров постоянен (r) , то и mJ = ±J

Правило отбора для разрешенных переходов имеет вид: DJ = ± 1,следовательно чисто вращательный спектр состоит из ряда эквидистантных линий с двумя ветвями Р и R.
Выражение для энергии имеет вид: E = (h2/2I)*J(J+1) ,
Окончательно для модели жесткого ротатора:
Ф(j) = А*exp(-imJj) и E = (h2/2I)*J(J+1).
Разница между двумя соседними линиями равна
DE = (h2/2I)*[ (J+1)(J+2) - J(J+1)] = (h2/2I)*2(J+1)
При возбуждении излучением DE = hDn = hc/l = hcv = h2pc*v ;
h2pc*v = (h2/2I)*2(J+1)
Окончательно.
волновое число v = (h /2pcI)*(J+1) = 2B(J+1) ,
где B = h/4pIс - вращательная постоянная для двухатомной молекулы
Это спектральная характеристика В позволяет экспериментально определить длину связи в молекуле.
Величину v = (EJ+1 –EJ)/hc = TJ называют вращательным термом.
Задачи на жесткий ротатор (Вращательные и колебательно – вращательные спектры)
В инфракрасном колебательно- вращательном спектре поглощение полосы СО среднее значение разницы между двумя соседними линиями составляет 3,86 см-1. Пренебрегая изменением межъядерного расстояния при переходе из одного колебательного состояния в другое, определите вращательную постоянную, момент инерции и межъядерное расстояние.
Решение. Разница между двумя соседними линиями Dn = 2В . Отсюда
В =h/4pIc = 3,86/2 =1,93см-1 = 193м-1
I = h/4pBc = 1,05 10-34 Дж*с/ (4*3,14*193м-1 *3*108 м/c) = 14,5*10-47 кг*м2
I = mr2 r = ÖI/m m = 1,14 *10-26 кг r = ÖI/m = 1,128 *10-10 м = 1,128 А
Водородоподобный атом.
Выражение для энергии водородоподобного атома в атомных единицах:
 (ат.ед.эн) =
(ат.ед.эн) =  (эрг) == -Z2me4/[(4pe0 )2 2h 2 * (1/ n2 )]
(эрг) == -Z2me4/[(4pe0 )2 2h 2 * (1/ n2 )]
(Джоуль)
1. Вывод энергия электрона в атоме квантуется.
Выражение в атомных единицах энергии дает нам единицу измерения энергии Ен
- хартри. Она равна Ен = 1 а.е. = 27,21 эВ = 2626 Кдж/моль.
Связь с другими величинами
1 эВ = 96, 485 кДж/моль = 96, 485*1000/6,02*1023 = 1,6*10-19 Дж
2. Все АО с одним значением n имеют одинаковое значение энергии, т.е. вырождены
Для n= 1 получаем 1–AO , для n = 2 получаем 4-АО и т.д. ,
т.е. степень вырождения равна n2
Число АО = n2 =1 при n=1
Число АО = n2 =4 при n=2 т.к. Е = f( n) то все 4 AO вырождены по энергии
Число АО = n2 = 9 при n=3 9 – кратное выражение по энергии.
3. Упростим выражение для переходе с n1 на уровень n2
DE = -Z2me4/(4pe0 )2 2h2 * (1/ n12 - 1/ n22 ) = hw
1/ l= v = Ry ((1/ n22 - 1/ n12) - волновое число, где
Константа Ридберга Ry= me4/8e20 h3 c = 1,09737* 107 м-1 (или *105 см-1) в волновых числах.
4. Правила отбора. Рассмотрим подробнее переход с n1 на n2
Dn – может быть любое, Dl = ±1
В излучение атома водорода Н наблюдается несколько спектральных серий
Спектральные серии.
Серия Лаймена n1=1 n2 > 1
Серия Бальмера n1=2 n2 > 2
Серия Пашена n1=3 n2 > 3
Серии Брэккета n1=4 n2 > 4

Задачи на экзамен.
Задача 1. Рассчитайте энергию, длину волны и частоту перехода v электрона с уровня водородоподобного атома с n1 на n2 .
Из лекций: энергия электрона в атоме водорода равна: Е = Z2/2n2 (a.e.) = 1/2n2(a.e.),
т.к. Z =1 для атома водорода Н.
Для n=1 получим E1 = ½ а.е. = ½ Eн = -13,6 эВ
Энергия электрона на последующих уровней
n =2 E = - ½*1/n2 = -13,6 /4 = - 3,4 эВ
n= 3 E = - ½*1/n2 = -13,6 /9 = - 1,51 эВ
Переход электрона с n =1 на n =2 DЕ = -3,4 + 13,6 = 10,2 эВ
DЕ = 10,2 эВ * 1,6*10-19 Дж = 1,62 *10-18 Дж
v = DE/hc = 1,62 *10-18 Дж / (6,62*10-34 Дж*с *3*108 м/с )=8,157 *106 м-1
v = 1/ l , отсюда l = 1/v = 1,23 *10- 7 м –это область УФ - излучения
Задача 2. Решение уравнения Шредингера для атома водорода. Спектр атомарного водорода. Спектральные серии. Рассчитайте длину волны (А) первых трех линий серии Брэккета в спектре атома водорода (n1=4). Ry=109737 см-1.
1/ l= v = Ry ((1/ n22-1/ n12) = 1,09737*107*((1/ n12 - 1/ n22) м-1
Если n1=4, то n2=5 принимает значение , равное 5,6,7
Для n1=4 и n2=5 1/ l= v = 1,09737*107*((1/42 - 1/52) м-1 = 2,47*105 м-1
Аналогично для n2=6 и n2=7
|
из
5.00
|
Обсуждение в статье: Приведем конечное уравнение для энергии. |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

