 |
Главная |
Преимущества использования кислорода вместо воздуха
|
из
5.00
|
Содержание.
Ø Введение ––––––––––––––––3
Ø Окисление ––––––––––––––– 4-11
§ Хлорирование –––––––––– 4-7
§ Кислородом –––––––––––– 7-9
§ Озонирование –––––––––– 9-11
Ø Нейтрализация ––––––––––––– 11-15
Ø Восстановление –––––––––––– 15 – 18
Ø Электрохимические методы ––– 18-26
§ Электроокисление –––– 21
§ Элетровосстановление ––-– 23
§ Электродиализ ––––––– 24-26
Ø Выводы -–––––––––––––––––––––26
Ø Дополнительные материалы –––– 27-30
Ø Литература -–––––––––––– 31
Качество сточных вод, образующихся на промышленных предприятиях, и концентрация в них загрязняющих веществ (ЗВ) определяется технологией производства и видом используемого исходного сырья, возможностью утилизации отходов, удельным расходом воды на единицу продукции. Выбор подходящего метода очистки необходимо осуществлять, исходя из качественно-количественных показателей состава загрязнённой воды и гигиенических требований. Среди разнообразных методов предпочтение отдаётся наиболее эффективным и дешёвым с низкой энергоёмкостью, используя доступные вещества.
Химические и электрохимические методы применяются для очистки СВ предприятий от токсичных веществ (на локальных очистных и общезаводских сооружениях) (возможно в совокупности с другими методами) например, перед сбросом в канализацию (т.е. дальше вместе с бытовыми СВ на городские очистные сооружения). Также эти методы могут использоваться на городских очистных сооружениях после биологической очистки (т.е. как доочистка) перед сбросом воды в поверхностные водоёмы. Несмотря на то, что эти методы эффективны при обезвреживании токсичных соединений, обеззараживании, доочистке от УВ, ПАВ и т.д., их целесообразно применять с другими методами (механическими, физико-химическими) из-за высокой стоимости, а также для достижения высокой степени очистки. Ещё химические методы используются для обеззараживания воды, например, при заборе воды из водохранилищ для коммунально-бытовых нужд (водопроводная вода).
К данным методам относятся:
· Окисление
· Восстановление
· Нейтрализация
· Электроокисление
· Электровосстановление
· Электродиализ
Тот или иной метод применяется в зависимости от состава СВ, объёма, а также стоимости очистки.
Дальше постараюсь в общем описать принципы работы данных способов и привести примеры их использования.
Окисление.
Очистка производственных СВ. Метод применяют для окисления HCN,цианидов, H2S, HS- метилмеркаптана, хлорпроизводных органических в-в, фенолов, ПАВ, нефти.
Важным моментом является выбор окислителя. Ниже приведены основные окислители и значения окислительно-восстановительного потенциала. Как правило, чем больше E0 , тем эффективней окислитель:
Cl2 E0=1,36 (B)
HClO 1,50 (pH<7) ; 0,88 (pH>=7)
ClO4- 1,38 ; 0,56
O3 2,07
H2O2 1,77 ; 0,88
MnO4- 1,7-1,5 ; 0,57
FeO42- 2,20 ; 0,72
CH3COOOH 1,8
Самые распространённые, дешёвые и простые – кислородом воздуха и хлорированием.
Хлорирование.
Для обезвреживания цианидов согласно СНиП 2.04.03-85 применяют окисление реагентами, содержащими активный хлор:
Cl2 + H2O=>HCl + HClO
HClO = H+ + ClO-
К таким реагентам относятся жидкий хлор, хлорная известь, гипохлориты Са и Na. Чаще всего используют NaClO, обеспечивающий наибольшую технологическую безопасность процесса. Водный р-р NaClO выпускают в промышленном масштабе С=180-200 г/л. Вследствие гидролиза раствор имеет щелочную реакцию:
NaClO+ H2O= HClO + Na+ + OH -
При pH=6-8 в растворе присутствуют HClO и ClO - в соизмеримых кол-вах, идёт р-я диспропорционирования:
2HClO + ClO- => ClO3- +2Cl - + 2H +
При Т>70° С реакция становится преобладающей.
Цианиды переходят в цианаты:
CN - + ClO- => CNO - + Cl -
Последние быстро подвергаются гидролизу:
CNO - +2H2O => HCO3 - + NH3
Аммиак окисляется до азота:
2NH3 + 2ClO- => N2 + 2H2O + 2HCl
Суммарная реакция:
2CN- + 5 ClO- + H2O => 5Cl - +2 HCO3- + N2 + Q
Чтобы избежать перегрева, концентрацию циансодержащего раствора подбирают, чтобы она не превышала 10,6 г/л по CN- (20 г/л NaCN). Вследствие гидролиза такой раствор имеет щелочную среду pH≈11,2. Обезвреженный раствор pH≈8,7. При pH<9,2 возникает опасность образования хлорциана при взаимодействии цианидов с оксидом хлора (Cl2O), образующимся по реакции разложения хлорноватистой кислоты.
CN-+Cl2O = ClCN + ClO-
Образование хлорциана легко обнаруживается по слезоточивому действию. Начальная раздражающая С 0,002 мг/л.
Чтобы этого избежать, в раствор необходимо добавлять щёлочь.
2СN+5ClO- +2OH- => CO32- +N2+5Cl-+H2O+Q
2NaCN+5NaClO+2NaOH=>2Na2CO3+N2+5NaCl+H2O
Q=1815,83 кДж/моль
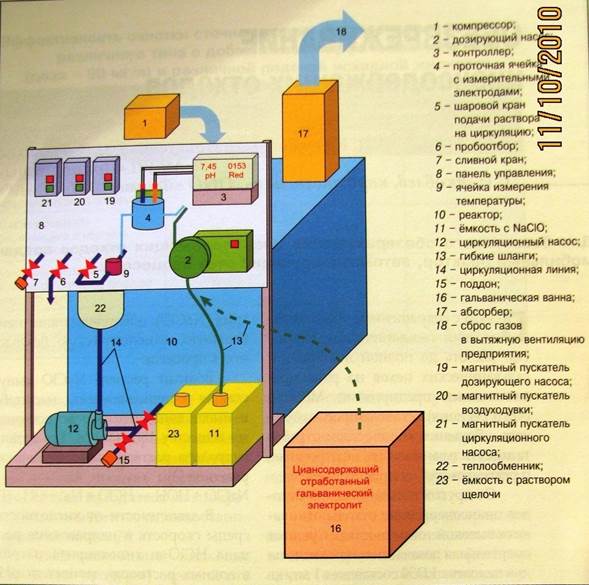
На рисунке представлен общий вид мобильной установки по обезвреживанию цианидов, в которой проходят вышеперечисленные реакции. Основа установки – реактор 10 из толстостенного полиэтилена V≈0,6-1 м3 . Циансодержащий раствор из ёмкости 16 и раствор гипохлорита из 11 по шлангам 13 насосом 2 подаются в реактор. Выполнение условий для оптимального протекания процесса определяется в проточной ячейке с измерительными электродами 4, соединённой с контроллером 3. Последний даёт команды насосу для подачи растворов цианидов, а также расчётного количества гипохлорита из ёмкости 11 и щёлочи из 23 для поддержания pH≈11. Система циркуляции раствора обеспечивает поддержание Т не более 70° С. Это достигается засчёт наличия ячейки измерения Т 9, передающей показания на контроллер, с которого команды поступают на шаровой кран 5 для подачи раствора на циркуляцию, которая осуществляется с помощью насоса 12 через теплообменник 22. Выделяющиеся газы через абсорбер 17 в системы вентиляции 18. По завершении через пробоотборник 6 отбирается проба для анализа на отсутствие цианидов в растворе.
Рис.1 Пример установки (опытная, мобильная) по обезвреживанию СВ от цианидов.
При хлорировании воды с последующей сорбцией на активном угле происходит удаление аммонийного азота. При хлорировании воды, содержащей аммонийный азот, в зависимости от рН, соотношения дозы активного хлора и концентрации аммонийного азота образуется смесь монохлораминов, дихлораминов, треххлористого азота, сорбируемых при фильтрации активным углем, и молекулярного азота, уходящего в атмосферу.
Недостатком способа является увеличение концентрации хлоридов в очищенной воде, особенно при обработке сточных вод с относительно высокой концентрацией аммонийного азота; преимуществом - увеличение срока службы угля до замены или регенерации за счет окисления органических веществ хлором на пористой поверхности угля, более высокая степень очистки от органических веществ, полное обеззараживание воды, удаление аммонийного азота с превращением в молекулярный азот, уходящий в атмосферу.
Окисление О2 воздуха под давлением.
Крупнотоннажным отходом нефтеперерабатывающей и химической промышленности являются сернисто-щелочные стоки. Они содержат сульфиды, гидросуьфиды, меркаптаны, фенолы и т.д. Их обезвреживают методом карбонизации и окисления О2 воздуха. При наличии в таких СВ заметного количества нафтеновых кислот их целесообразно выделять с последующей переработкой в мылонафт. Если количество СЩС невелико, то их можно подвергать биологической очистке. Сточные воды с высоким содержанием H2S поступают в основном с установок первичной переработки, кат. крекинга, замедленного коксования, гидроочистки, гидрокрекинга. Наибольшее распространение в промышленности получил способ окисления в жидкой фазе кислородом под давлением. Окисление проходит последовательно:
S2- - S0 – SnO62- - S2O32- - SO32- - SO42-
S2- => S2O32- ; SO32-
2S2-+2O2+H2O => S2O32- + 2OH-
NaHS + CO2 + H2O = NaHCO3 + H2S
Скорость возрастает при использовании катализаторов. Известен способ локального обезвреживания СЩС, основанный на жидкофазном гетерогенно-каталитическом окислении кислородом воздуха при Т 60-90° С в присутствии полифталоцианина кобальта, нанесённого на полимерную основу. Сульфиды окисляются до тиосульфатов и сульфатов. Однако при высокой С(10000-20000 мг/л) сульфидов необходимо увеличивать расход воздуха, энергозатраты, продолжительность. Поэтому проводятся различные исследования по улучшению качества очистки. Например предварительная нейтрализация СЩС H2SO4 (например, отработанной с установки кат. алкилирования). NaHS можно выделять как товарный продукт.
Очистку бензина прямой гонки от сернистых соединений традиционно проводят щелочью. Для этих целей используется 15-20 % раствор NaOH. В ходе очистки протекают реакции:
RSH + NaOH → RSNa + H2O
НS- + NaOH → Na2S + H2O
CO2 + 2NaOH → Na2CO3 + H2O
Натриевые соли кислых компонентов хорошо растворяются в воде и при расслаивании смеси щелочью – нефтепродукт переходят в водную фазу, которая и образует сернисто-щелочные стоки. Так как сульфид натрия является солью сильно основания и слабой кислоты, то в водном растворе он гидролизуется. В результате гидролиза в водном растворе будут находиться одновременно NaOH, Na2S и NaНS.
При рН = 7,0 – 13,75 основным продуктом окисления Na2S, NaНS, H2S является тиосульфат. В щелочной среде (рН = 9,0 – 9,5) протекают реакции с образованием сульфитов, сульфатов. При этом рН сточной воды понижается. При окислении в щелочной среде (рН = 12,15 – 12,75) сульфидов и гидросульфидов до сульфита и сульфата изменения рН сточной воды не происходит.
Повышение температуры и давления увеличивает скорость и глубину окисления сульфидов и гидросульфидов, не изменяя механизм реакции.
В случае применения катализаторов скорость окисления возрастает. Высокими каталитическими свойствами обладают графитовые материалы. При использовании кристаллического графита окисление гидросульфида и сульфида натрия идет в основном до тиосульфата, а при использовании коллоидно-дисперсных материалов – до элементарной серы. Исследования показали, что скорость окисления пропорциональна концентрации сульфидов. Скорость окисления сульфидов повышается с увеличением давления.
Обогащение необработанной воды кислородом является важным шагом в получении высококачественной питьевой воды (посредством удаления метана, железа (II), марганца (II), ионов аммония и т.д.). Концентрация кислорода в поступающей в распределительные трубопроводы воды свыше 6 мг/л обеспечивает надежную защиту от коррозии.
Парциальное давление чистого кислорода превышает это значение для воздуха, в результате концентрация кислорода в воде будет до 4,8 раз больше, чем при использовании воздуха. Обогащение воды чистым кислородом позволяет повысить эффективность протекания различных процессов и уменьшить затраты.
На примере фирмы:
Система SOLVOX® решает проблему дефицита кислорода посредством нагнетания в воду чистого кислорода. В зависимости от конкретных требований, кислород может нагнетаться с помощью форсунок (SOLVOX®-D) или реакторов (SOLVOX®-R) непосредственно в трубопровод перед фильтрами или перед распределительными трубопроводами.
· SOLVOX®-D: Нагнетание кислорода с помощью форсунки со сферической головкой.
· SOLVOX®-R: Встроенное или перепускное нагнетание кислорода с использованием реакторов из нержавеющей стали (значения расхода от 15 до 1000 м3 H2O/час).
Желаемое количество кислорода контролируется вручную или автоматически.
Преимущества использования кислорода вместо воздуха
· Высокий окислительный потенциал чистого кислорода
· Повышение производительности системы фильтрации
· Отсутствие нежелательного выделения азота в водопроводном кране
· Повышение качества питьевой воды
· Почти полное отсутствие воздействия очистки на двуокись углерода, таким образом, баланс извести / двуокиси углерода остается неизменным
· Улучшение вкуса
Озонирование.
При озонировании окисляются как растворенные, так и взвешенные органические вещества. Так как взвешенные вещества можно удалить более дешёвыми способами (механической очисткой, флотация…) для снижения расхода О3 озонирование применяют на завершающей стадии очистки СВ. Озон можно получать непосредственно на очистных сооружениях. Среди преимуществ также можно отметить высокую реакционною способность, бактерицидное действие (обеззараживающее) отсутствие в воде остатков озона. Поэтому О3 является перспективным методом.
Озонирование как метод глубокой очистки биологически очищенных городских сточных вод, несмотря на высокую себестоимость, является универсальным, так как оно позволяет одновременно снизить концентрацию загрязнений по ХПК на 40%, по БПК5 на 60-70%, содержание взвешенных веществ на 60%, ПАВ на 90%, фенолов на 40%, азота на 20%, канцерогенных веществ на 80%, а также снять окраску вод на 60% с одновременным обеззараживанием воды. Рекомендуемая доза О3 составляет 10-15 мг/л при времени его контакта с СВ 15 мин.
Совмещение озонирования с процессом удаления взвеси флотацией получило название озонофлотации. Озонофлотатор – аппарат, в который подаётся сточная вода, прошедшая реактор для растворения в ней озоновоздушной смеси. Одновременно в аппарате создаются условия образования мелких пузырьков озоновоздушной смеси, которые увлекают с собой взвесь и окисляют её при подъёме. Взвесь образует на поверхности жидкости флотопену, которая удаляется на обработку. Сбор флотопены с поверхности жидкости на практике осуществить сложно, и это является одним из препятствий для внедрения метода.
Обеззараживание; СВ, содержащие фенолы, циклопентан, тетраэтилсвинец, ПАВы, нефть и др.
Перед подачей на биологическую очистку. Переводит трудноокисляемые в биоразлагаемые в-ва.
ПАВ: например, алкиларилсульфонаты, алкилнафталинсульфонаты.
Скорость при фиксации веществ (при сорбции на Сакт)
H2S + O3 → S + Н2О + О2
3H2S + O3 → 3S + 3Н2О
Пример озонатора ( для оборотной системы) на фото:
В комплект озонирующей установки (представлена модель «Озон-20ПВ-2Б-С», выпускаемая в период 2005 года) входит:
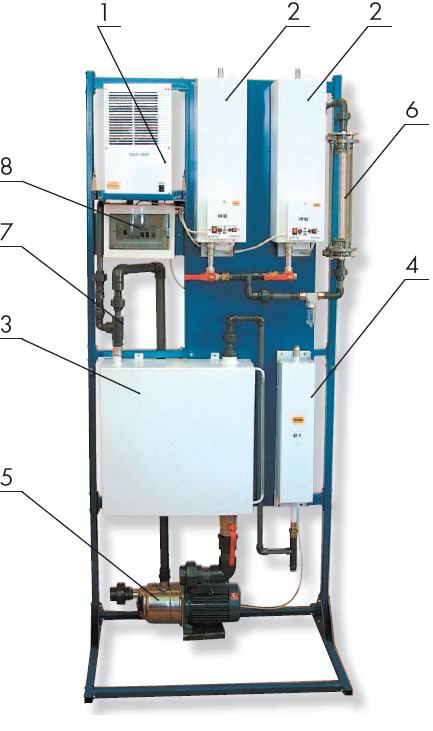
1 - Генератор озона, 2 - Осушитель воздуха,
3 - Контактно-смесительная камера, 4 - Деструктор озона, 5 - Насос, 6 - Ротаметр, 7 - Эжектор, 8 - Блок управления
Принцип работы станции (рис. внизу справа) основан на растворении озона в воде методом вакуумного эжектирования. Вода из емкости при помощи насоса подается на вход вакуумного эжектора. Вакуумное реле генератора замыкает цепь питания газоразрядного реактора и начинается выработка озона. Озоновоздушная смесь подсасывается эжектором и интенсивно перемешивается с потоком воды, проходящим через эжектор с большой скоростью. В результате вода насыщается мельчайшими пузырьками озоновоздушной смеси, а на поверхности раздела жидкой и газовой фаз начинается массоперенос газообразного озона в воду. Насыщенная озоном вода поступает обратно в емкость через специальные смесительные насадки - турбо-миксеры.
ORP-контроллер непрерывно контролирует значение окислительно-восстановительного потенциала в емкости. При достижении заданного верхнего порога значения потенциала по сигналу контроллера насос отключается и поступление озона в воду прекращается. При последующем снижении величины потенциала до нижнего порогового значения потенциала по сигналу контроллера насос включается и процесс озонирования воды возобновляется.Поддержание уровня воды в емкости происходит автоматически.
 Рис. - установка с аналогичным принципом работы:
Рис. - установка с аналогичным принципом работы:
Нейтрализация.
Этот метод позволяет предотвратить коррозию водоотводящих сетей и очистных сооружений, нарушение биохимических процессов в биологических окислителях и водоёмах.
Для нейтрализации кислых сточных вод применяют взаимную нейтрализацию кислых и щелочных сточных вод, обработку известковым молоком. При небольших объёмах кислой воды эффективно фильтрование через фильтрующие материалы (известняк, мел, доломит, магнезит и т.п.). В результате нейтрализации СВ образуются нерастворимые и плохо растворимые соли Са, которые могут отложиться на стенках оборудования. Поэтому необходима периодическая очистка открытых желобов и кратковременная промывка трубопроводов чистой водой.
|
из
5.00
|
Обсуждение в статье: Преимущества использования кислорода вместо воздуха |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

