 |
Главная |
Вскрытие тантало-ниобиевых концентратов
|
из
5.00
|
Глава 6
ВСКРЫТИЕ КОНЦЕНТРАТОВ РЕДКИХ МЕТАЛЛОВ ЩЕЛОЧАМИ И ФТОРСИЛИКАТНЫМИ РЕАГЕНТАМИ
ВСКРЫТИЕ ЩЕЛОЧЬЮ
В технологии редких металлов для вскрытия силикатных или фосфорных руд применяют едкий натр, иногда едкое кали. Щелочи используют в виде концентрированных растворов при температуре 200°С или в виде расплава. Температура плавления едкого натра 318° С. В качестве продуктов такого вскрытия получаются окислы, гидратированные окислы и гидроокиси металлов и растворимые в воде фосфаты и силикаты натрия.
Вскрытие щелочью проводят обычно периодически в реакторах с мешалками или непрерывно во вращающихся печах. В последнем случае 50%-ный раствор щелочи впрыскивается форсункой. Обогрев печи за счет внутреннего сжигания газа недопустим, так как при этом едкие щелочи переходят в карбонаты, а вскрытие концентратов редких металлов карбонатами происходит при гораздо более высокой температуре.
В последнее время все большее значение в технологии приобретают процессы спекания с щелочными реагентами в таких высокопроизводительных аппаратах, как печи кипящего слоя и циклонной плавки.
Вскрытие монацита
В основе вскрытия монацита щелочью (рис. 31) лежит реакция
Th3(PO4)4 + 12NaOH ® 3ThO2 + 4Na3PO4 + 6H2O
Для РЗЭ реакцию можно записать так:
2LnPO4 + 3NaOH = Ln(OH)3 + Na3PO4
На каждую тонну монацита расходуется примерно 1,2 т щелочи и 1 г воды.
Достаточно полное разложение концентрата достигается лишь при тонком измельчении монацита (96,5% -0,043 мм). Такой концентрат постепенно загружают в концентрированный раствор щелочи, нагретый до 130° С. Реакция идет при нагревании с обратным холодильником до 140-145° в течение 4 ч. Необходимо предусмотреть вентиляцию для удаления торона. Исключительно важно не перегревать смесь выше 145°С, иначе получаются окислы тория и РЗЭ, впоследствии медленно и не полностью растворяющиеся в азотной кислоте. Расход едкого натра можно уменьшить и процесс вскрытия значительно интенсифицировать, если проводить его в обогреваемой шаровой мельнице. Истирающее воздействие шаров ускоряет реакцию, так как разрушает пленки гидроокисей, которые образуются на зернах минерала. В этом случае монацит предварительно измельчают только до частиц крупностью 1-5 мм.
Продукт реакции после вскрытия разбавляют промывными водами до содержания едкого натра 30%. Пульпу кипятят, при этом увеличиваются размеры частиц гидроокиси, и затем фильтруют.
Чтобы тринатрийфосфат не выпал в осадок, поддерживают температуру 110° С.

Рис. 31. Технологическая схема переработки монацита сплавлением с едким натром.
Гидратированные окислы тория и РЗЭ, содержащие некоторое количество урана, промывают несколько раз водой, чтобы отмыть их от фосфат-ионов.
Кек, состоящий из смеси гидратированных окислов, растворяют в азотной кислоте и направляют на разделение методом экстракции. Фильтрат, содержащий тринатрийфосфат и едкий натр, упаривают до 47%-ного NaOH. При этом тринатрийфосфат кристаллизуется, a NaOH можно вновь использовать для вскрытия.
Перед процессом экстракции можно разделить торий и РЗЭ на соответствующие концентраты. Для этого гидроокись тория осаждают предварительно едким натром при рН=5,8. Если исходный монацит содержал некоторое количество апатита, который .практически не вскрывается едким натром, но вскрывается азотной кислотой, то нитратные растворы непригодны для экстракции из-за наличия в них РО43-. Чтобы избавиться от апатита, перед щелочным вскрытием концентрат предварительно кипятят в азотной кислоте в течение 3 ч. При вскрытии монацита щелочью в раствор, переходит примерно 99,5% тория и РЗЭ. Вскрытие монацита едким натром является перспективным способом. Преимуществом его перед сернокислотным методом является отделение уже на первой стадии фосфора от тория и РЗЭ с получением тринатрийфосфата. Экстракционная очистка урана, тория и РЗЭ при использовании этой схемы существенно облегчается отсутствием значительных количеств сульфат- и фосфат-ионов в осадках гидроокисей.
Вскрытие циркона
Цирконовый концентрат без специального измельчения подают во вращающуюся печь, куда под давлением впрыскивают предварительно нагретый 50%-ный раствор NaOH. Спек имеет форму порошка и не прилипает к стенкам печи. Средний состав спека: 30% ZrO2 + HfO2; 52% Na2О; 15% SiO2; 3% Н2О.
Реакция спекания описывается уравнением
ZrSiО4 + 4NaOH ® Na2ZrO3 + Na2SiO3 + 2H2O
Горячий спек обрабатывают при интенсивном перемешивании водой, силикат натрия растворяется. Остаток отфильтровывают на барабанном вакуумном фильтре, кек репульпируют и фильтруют вторично. Средний состав продукта: 43% ZrO2 + HfO2; 4% Na2О; 4% SiO2; 49% Н2О
Полученные гидратированные двуокиси циркония и гафния поступают в реактор с мешалкой с контролируемой подачей HNO3. При этом тепла реакции недостаточно, и суспензию подогревают дополнительно. В этих условиях получается хорошо фильтруемый осадок кремнекислоты и прозрачный концентрированный раствор нитратов. циркония и гафния. Он содержит менее 1% кремнекислоты по отношению к двуокиси циркония и загрязнен примесями железа, титана и др. Этот раствор, разбавленный рекуперированной азотной кислотой, направляют на экстракцию.
В зависимости от того, в виде какого соединения необходимо получить цирконий, дальнейшую переработку спека можно проводить растворением его в различных кислотах.
Если продуктом являются сернокислые соли циркония для кожевенной промышленности, осадок растворяют в серной кислоте. Раствор представляет собой весьма сложную систему из-за одновременного протекания процессов комплексообразования, гидролиза и гидролитической полимеризации. В растворах небольшой кислотности возможно образование многоядерных соединений, в основе которых лежит тетрамерный ион циркония с оловыми мостиками. Такие ионы могут быть связаны в более сложные цепи через оловые или оксо-мостики. Не исключено образование линейных многоядерных соединений. В кислых растворах также возможно образование многоядерных соединений, в которых связь между атомами циркония осуществляется через сульфогруппы.
Имеется несколько методов получения различных соединений циркония в условиях, исключающих загрязнение посторонними ионами. Растворение в серной кислоте позволяет добиться хорошей очистки от кремневой кислоты. Хорошая очистка достигается при растворении осадка в концентрированной соляной кислоте и осаждении из нее так называемого оксихлорида циркония ZrOCl2.8H20. В настоящее время доказано, что в этой молекуле отсутствует ион цирконила и в основе ее лежит четырехчленный каркас из ионов циркония, связанных гидроксильными группами.

Рис. 32. Технологическая схема переработки циркона сплав-лением с едким натром.
На рис. 32 приведена одна из возможных технологических схем. Очистку циркония от сопутствующих примесей по этой схеме ведут кристаллизацией Zr(SО4)2.4H20. Для этого к раствору сульфата с концентрацией циркония 120-130 г/л добавляют концентрированную H2SO4 в количестве один объем кислоты на два объема раствора. Фильтрацию ведут через фильтр из пористого стекла или керамики. Осадок промывают смесью разбавленной серной и соляной кислот.
Вскрытие тантало-ниобиевых концентратов
Вскрытие едким натром
Щелочи применяют для вскрытия колумбито-танталитовых концентратов и феррониобия. Танталит и колумбит являются прочными минералами. Состав минералов можно выразить общей формулой (Fe, Mn)[(Ta, Nb)О3]2. Минералы представляют собой изоморфную смесь четырех солей: Fe(TaO3)2, Мn(ТаО3)2, Fе(NbО3)2 и Мn(NbО3)2. Они не разлагаются минеральными кислотами (за исключением плавиковой кислоты). При сплавленин их с щелочами образуются соответствующие танталаты и ниобаты. Эти процессы могут быть представлены реакциями:
Fе(NbО3)2 + 10NaOH = 2Na5NbО5 + FeO + 5Н2O;
Fе(ТаО3)2 + 10NaOH = 2Na5ТаО5 + FeO + 5Н2O;
Аналогично могут быть написаны реакции для Мn(ТаО3)2 и Мn(NbО3)2. Кроме окислов FeO и МnО из-за окисления кислородом воздуха образуются Fе3O4 и Mn3O4. Окись железа, двуокись кремния, окись алюминия, окись олова, вольфрамит, рутил и ильменит при сплавлении с NaOH образуют соответствующие натриевые соли. Сплавление проводят в железных тиглях при нагревании до 800° С. На 1 весовую часть концентрата при этом берут 3 части NaOH. Это в 3-4 раза больше теоретически необходимого.
Едкий натр расплавляют в тигле, и его температуру поднимают до 400° С. Затем в плав порциями добавляют измельченный до 0,1 мм концентрат. При этом наблюдаются вспенивание и перемешивание смеси выделяющимися парами воды. Затем температуру повышают до 600° С и смесь выдерживают в течение 30 мин. После этого расплавленную массу выливают в воду и проводят выщелачивание при температуре 80—90° С и отношении твердой и жидкой фаз 1 : 3¸4.
При этом получается сильнощелочной раствор, в который переходит большая часть примесей Si, Sn, W, A1 и т. д. в виде растворимых натриевых солей. Осадок содержит гидратированные сложные ниобаты и танталаты натрия, гидраты окислов и гидроокиси железа и марганца и титанат натрия.
После отстаивания раствор декантируют и осадок промывают 5%-ным горячим раствором NaOH (для уменьшения растворимости ниобата натрия). Осадок разлагают 20%-ной соляной кислотой при нагревании:
7Na2О.6Nb2О5 + 14HCl + xH2O ® 6Nb2О5.xH2О + 14NaCl;
4Na2О.3Ta2О5 + 8HCl + xH2O ® 6Ta2О5.xH2О + 8NaCl.
Разложение ведут в керамических аппаратах при подогреве острым паром. По достижении полного разложения темно-коричневый осадок переходит в белый. Железо и марганец переходят в раствор в виде хлоридов.
Осадок многократно промывают горячей водой, подкисленной НСl, фильтруют и сушат при 100-120° С. Этот продукт содержит до 96-99% (Nb, Ta)2O5 в пересчете на безводный продукт и является исходным для разделения тантала и ниобия экстракцией.

Рис. 33. Технологическая схема вскрытия колумбита-танталита сплавлением с NaOH.
На рис. 33 представлена технологическая схема процесса.
Вскрытие едким кали
При вскрытии танталита-колумбита едким кали получается более хорошая очистка от сопутствующих элементов вследствие образования растворимых в воде ниобата и танталата калия. Сплавление ведется в железных тиглях (аналогично процессу сплавления с едким натром). При выщелачивании в раствор переходят К2ТаО5, K2NbO5, K2SiO3, K2WO3, К2SnO3 и частично К2ТiO3.
При добавлении к раствору хлористого натрия осаждаются малорастворимые танталат и ниобат натрия. Примеси Si, W, Sn и частично Ti остаются в растворе. Затем осадок ниобатов и танталатов разлагают серной или соляной кислотой до окисей. Едкое кали в этом процессе можно заменить поташом; при этом необходимо повысить температуру вскрытия.
Технологическая схема представлена на рис. 34.
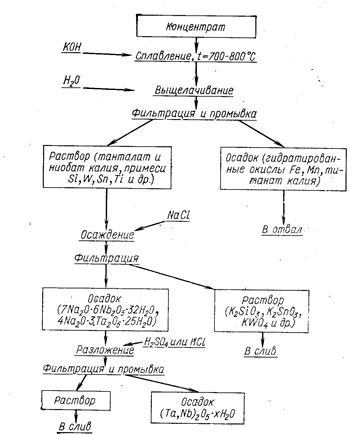
Рис. 34. Технологическая схема вскрытия танталта-колумбита сплавлением с КОН.
|
из
5.00
|
Обсуждение в статье: Вскрытие тантало-ниобиевых концентратов |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

