 |
Главная |
Вскрытие феррониобия сплавлением с едким кали
|
из
5.00
|
Феррониобий можно выплавлять непосредственно из колумбита. Он содержит около 60% Mb, 9% Та, 24% Fe и примеси Ti, W, Mn, Al и др. Сплав растворяют при нагревании в концентрированном растворе едкого кали. При этом выделяется водород: 2Nb + 10KOH = 2K5NbO5 + 5H2.
Феррониобий, измельченный до крупности 0,147 мм, медленно добавляют в нагретый раствор едкого кали. Водород поддерживает восстановительную атмосферу и препятствует образованию железа (III). Образующиеся в процессе реакции ниобат и танталат калия переходят в раствор, а соединения железа и титана остаются в осадке. В осадке остается также до 5% ниобия.
Осадок тщательно промывают и фильтруют. Процесс ведется при 70° С. Осадок сбрасывают, а из раствора добавлением твердой поваренной соли осаждают нерастворимые ниобаты и танталат натрия. Их отфильтровывают, промывают 5%-ным раствором NaCl и затем обрабатывают соляной кислотой. При этом танталаты и ниобаты разлагаются до соответствующих гидратированных окислов.
СПЕКАНИЕ С ИЗВЕСТЬЮ
Вскрытие минералов редких металлов спеканием их с известью широко применяют в технологии. Окись кальция является дешевым и общедоступным реагентом. Ее получают обжигом известняка. СаСО3 можно непосредственно использовать для вскрытия минералов редких металлов.
Процесс спекания характеризуется тем, что он проходит при температуре ниже температуры плавления реагентов и продуктов реакции. Вместе с тем жидкая и газовая фазы играют исключительно важную роль в большинстве практически осуществляемых реакций. При измельчении реагентов до размера порядка 10-3 см поверхность контакта между фазами по крайней мере в 10000 раз меньше общей поверхности. В присутствии жидкой фазы поверхностью реакционного контакта является полная поверхность зерен компонентов. Это приводит к повышению скорости процесса вскрытия. Жидкая фаза возникает в результате образования эвтектических смесей с продуктами, в том числе с промежуточными продуктами реакции, и эвтектических смесей продуктов реакции с различными веществами примесей.
В технологии широко применяют специальные добавки, образующие жидкую фазу (обычно хлористый кальций, фтористый кальций, поваренную соль и т. п.). Количество жидкой фазы должно быть небольшим, она должна равномерно распределяться и прочно удерживаться на поверхности твердых частиц. Образование жидкой фазы в большом количестве нарушает перемещение реагентов по длине вращающейся печи и может приводить к образованию настылей.
Термодинамические реакции, протекающие в твердой фазе, обычно идут до конца, если они являются экзотермическими. Считается, что для того, чтобы реакция проходила в нужном направлении, достаточно выделения 1 ккал/ (г-атом} реакционной смеси. Это объясняется тем, что при твердофазных реакциях изменение энтропии весьма незначительно и величина DG° = DH° - TDS° в случае экзотермических реакций практически всегда отрицательна. Положение, однако, существенно меняется, если в результате реакции образуются твердые растворы, смешанные кристаллы, стекловидная или газовая фаза, т. е. если идут процессы, увеличивающие энтропийную составляющую.
Следует подчеркнуть, что одного термодинамического анализа недостаточно для решения вопроса о том, пойдет ли реакция. Высокое значение энергии активации, большой размер зерен, малая поверхность соприкосновения реагентов и значительные диффузионные сопротивления могут термодинамически вероятную реакцию сделать практически невозможной.
Особую роль в стимулировании твердофазных реакций играют полиморфные превращения любой из фаз. Как правило, химическая реакция начинается и интенсивно проходит при температуре полиморфного превращения. Это связано с повышенной концентрацией дефектов кристаллической структуры непосредственно после такого превращения и с тем фактом, что в момент переориентировки частицы обладают особенно большой подвижностью и реакционной способностью.
Механизм твердофазных реакций изучен недостаточно. Средством управления скоростью таких реакций являются регулирование размеров зерен исходных реагентов, регулирование строения их решеток, температуры процесса, а также введение в реакционную смесь различных добавок, ускоряющих или стабилизирующих процесс. Однако без детального выяснения механизма действия всех этих факторов невозможны их обоснованный выбор и оптимальное сочетание.
Вскрытие литиевых руд
Метод основан на спекании литиевых минералов с известью или известняком с последующим выщелачиванием водой. После очистки от примесей и упаривания из раствора кристаллизуется гидроокись лития LiOH.H2O, непосредственно являющаяся товарным продуктом. Спекание проводят при 1000°С. Реакция может быть представлена уравнением
Li2O . Al2O3 . 4SiO2 + 5СаО ® Li2O + СаО.Al2O3 + 4(СаО . 4SiO2)
Однако выщелачивание едкого лития в воду проходит значительно полнее, если в пульпе присутствует избыток СаО. Это привело к выводу, что процесс может быть представлен по аналогии с взаимодействием натриевого алюмосиликата с окисью кальция как
Li2O . Al2O3 . 4SiO2 + 8СаО ® Li2O.Al2O3 + 4(2СаО . SiO2)
В процессе выщелачивания алюминат лития реагирует с Са(ОН)2:
Li2O . Al2O3 + Са(ОН)2 ® LiOН + СаО.Al2O3
Образовавшиеся в процессе спекания алюминаты натрия и калия взаимодействуют с известью по аналогичной реакции с образованием едких щелочей. Моногидрат лития имеет наименьшую растворимость и выкристаллизовывается из упаренного раствора, в то время как едкий натр, едкое кали и алюминаты натрия и калия остаются в маточном растворе.
Вскрытие спеканием с известью применяют к сподуменовым лепидолитовым рудам. На рис. 35 приведена технологическая схема переработки сподумена спеканием с известью или известняком.
Измельчение сподумена и известняка проводят до размеров зерна <0,25 мм. Обращают особое внимание на тщательность смешения шихты, чего достигают обычно совместным доизмельчением обоих компонентов в шаровой мельнице, работающей в замкнутом цикле с классификатором. Размер частиц в сливе не должен превышать 0,074 мм.
Спекание осуществляют во вращающихся трубчатых печах. Так, на заводе в Санбрайте (США), производящем 25-30 т едкого лития в сутки, работает печь длиной 120 м и диаметром 3,5 м. Спекание ведут при температуре 1150-1200° С. Необходимо не допускать перегрева и превращения массы в жидкотекущую, так как при этом уменьшается переход лития в воднорастворимую форму и образуются настыли в печи. Горячий спек высыпают в бассейн, заполненный оборотными растворами, и выщелачивают в шаровой мельнице, работающей в замкнутом цикле с классификатором. Выщелачивание проводят при температуре 90° С и отношении твердой и жидкой фаз 1 : 3. Пульпапоступает на сгущение. Осадок после первого сгустителя многократно промывают и сбрасывают. Содержание в нем лития не превышает 0,10-0,15%. Отвальный шлам может быть использован для производства вяжущих материалов. Его состав: 33,0-50,8% 2CaO.SiО2, 16,1-22,0% ЗСаО.Al2O3, 6,4-9,9% 2CaO.Fe2О3, 10,4-16,6% СаСО3.
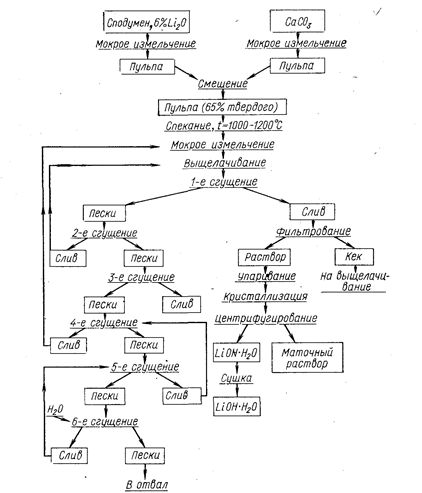
Рис. 35. Технологическая схема вскрытия сподумена спеканием с известью.
Раствор после выщелачивания содержит около 10 г/л окиси лития. Его упаривают в вакуумных выпарных аппаратах в 8 - 10 раз, в осадок выпадают карбонаты лития и кальция, которые отфильтровывают из раствора и передают на выщелачивание. Фильтрат упаривают до плотности 1,20 г/см3 и охлаждают до 40-50° С. При этом происходит кристаллизация LiOH.H2O. Если необходима дополнительная очистка, можно промытые кристаллы перекристаллизовать еще раз.
В фильтрате после центрифугирования в результате многократного оборота накапливаются едкие натр и кали, а также алюминаты натрия и калия. Поэтому этот оборотный раствор периодически выводится из цикла и перерабатывается отдельно. В нем концентрируются рубидий и цезий.
Интересным вариантом вскрытия сподумена известью является способ, основанный на обработке концентрата известковым молоком под давлением при температуре 190-290оС. Процесс схематически можно описать реакцией
Li2O . Al2O3 . 4SiO2 + 4СаО + 4Н2О ® 2LiOH + 2Al(OH)3 + 4CaSiO3
Кремний и большая часть алюминия остаются в осадке. Натрий, содержащийся в сподумене, переходит в раствор. Частично в раствор переходит алюминий в виде алюмината натрия. Очистка раствора от этих примесей проводится карбонизацией.
При пропускании углекислого газа через раствор резко снижается щелочность раствора. При этом алюминат натрия разлагается, и в осадок выпадает гидроокись алюминия.
После выделения примесей раствор упаривают и вновь карбонизируют. В осадок выпадает карбонат лития, который после отмывки горячей водой является товарным продуктом. Известковая схема переработки литиевых минералов обладает существенными достоинствами. Она универсальна, так как применима почти для всех литиевых минералов. Известь — широкодоступный и дешевый реагент. Отходы процесса могут служить сырьем для цементных заводов. Основная операция вскрытия—спекание — осуществляется во вращающихся печах, широко применяемых в цементной промышленности. Известковый способ позволяет получить едкий литий из сподумена, минуя стадию осаждения промежуточных соединений.
К недостаткам схемы относится получение разбавленных растворов едкого лития, что влечет за собой большие объемы технологической аппаратуры и значительные затраты на упаривание.
Вскрытие циркона
Вскрытие циркона спеканием с известью основано на реакции образования цирконата кальция, растворимого в кислотах:
ZrSiO4 + 2CaO = CaSiO3 + CaZrO3
В зависимости от температуры, выдержки во времени и состава шихты могут образовываться и другие силикаты: 2CaO . 2SiO2 и 2CaO.SiO2
Реакция спекания идет с достаточной скоростью лишь при 1400-1500° С. Однако температура может быть понижена до 1000-1100° С добавкой хлорида натрия или кальция. Ускорение происходит в результате перевода реакции в жидкую фазу расплава соответствующего хлорида. Спекание проводят во вращающейся печи.
Выщелачивание спека ведут в два приема. Первоначально спек обрабатывают разбавленной соляной кислотой на холоду. При этом цирконат кальция не разлагается, а в раствор переходят хлористый кальций и кремнекислота вследствие растворения избытка извести и частичного разложения силиката кальция. Примеси железа и алюминия также переходят в раствор. Раствор декантируют и остаток обрабатывают 20-30%-ной соляной кислотой при нагревании до 80-90° С. В этих условиях цирконат кальция разлагается. Разлагается также основная масса силиката кальция. Кремнекислота переходит в раствор в коллоидном состоянии. Чтобы перевести ее в осадок, к раствору добавляют коагулянт.
Растворимость оксихлорида циркония сильно зависит от концентрации соляной кислоты и температуры. Для выделения кристаллов оксихлорида циркония из раствора его упаривают до концентрации 220 г/л. Затем раствор охлаждают, и 95% циркония кристаллизуется. Состав соли отвечает формуле ZrOCl2.8H2O.
Если в результате этой операции очистка оказывается недостаточной, проводят еще одну перекристаллизацию. Растворив соль в воде и добавив аммиачный раствор, осаждают гидратированную двуокись циркония ZrO2.xH2O. Она может быть прокалена до двуокиси ZrO2 или растворением в азотной кислоте переведена в азотнокислый раствор для последующей очистки циркония от гафния.
После первого выщелачивания раствор, содержащий хлорид кальция, кремнекислоту и хлориды железа и алюминия, обрабатывают серной кислотой. Получающуюся соляную кислоту возвращают на стадию выщелачивания, а осадок сбрасывают.
На рис. 36 приведена технологическая схема.

Рис. 36. Технологическая схема вскрытия циркона спеканием с известью.
|
из
5.00
|
Обсуждение в статье: Вскрытие феррониобия сплавлением с едким кали |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

