 |
Главная |
Описание технологической схемы
|
из
5.00
|
Введение
Использование полинитроароматических соединений в органическом синтезе привлекает как доступностью исходного сырья, так и широкими синтетическими возможностями, обусловленными наличием нитрогрупп.
С одной стороны, полинитросоединения являются промышленно производимыми продуктами - производные нитробензола широко используются как взрывчатые вещества, так и промежуточные продукты в синтезе красителей.
Ароматические полинитросоединения, благодаря способности нитрогрупп к восстановлению и нуклеофильному замещению, а также возможности модификации других заместителей в цикле, представляют большую ценность в качестве субстратов в органическом синтезе. Например, ароматическая нитрогруппа оказывает активирующее, в силу своей электроноакцепторной природы, влияние на другие заместители в ароматическом кольце. В 2,4,6-тринитротолуоле благодаря наличию трех нитрогрупп становятся возможными реакции конденсации метильной группы с электрофильными агентами (альдегидами, нитрозосоединениями и др.) [1].
Активированные ароматические нитрогруппы подвергаются замещению различными нуклеофилами, особенно легко протекает внутримолекулярная разновидность этой реакции, в которой нуклеофильная группа содержится в исходном субстрате. Реакция внутримолекулярной динитроциклизации открывает путь к синтезу различных конденсированных гетероциклов. Значительный интерес представляет синтез бензоконденсированных шести - и особенно семичленных гетероциклов, так как среди них имеется большое количество лекарственных веществ, в частности, регулирующие работу ЦНС - транквилизаторы, снотворные, антидепрессанты, нейролептики и т. п [2].
Продукты нитрования бензойной кислоты - моно - и динитробензойные кислоты - широко применяются в качестве полупродуктов в органическом синтезе, фармацевтике, фотохимии и химии красителей [3]. В частности, 3,5-динитробензойная кислота используется в синтезе аминобензойных кислот, являющихся полупродуктами при получении азокрасителей, лекарственных препаратов, нитробензоилхлоридов, пигментов.
Реакции с хлорангидридами 3,5-динитробензойной кислоты используют для идентификации спиртов, аминов и алифатических простых эфиров.
Кроме того, 3,5-динитробензойная кислота используется для приготовления рентгеноконтактного препарата типа “Триомброст”, для приготовления витамина 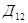 , служащего для витаминизации кормом, применяемых в сельском хозяйстве [3].
, служащего для витаминизации кормом, применяемых в сельском хозяйстве [3].
Таким образом, можно сделать вывод о важности проектирования производства 3,5-динитробензойной кислоты мощностью 13 тонн в год, как для развития сельского хозяйства, так и для других отраслей промышленности.
Аналитический обзор
Одним из наиболее интересных представителей является 3,5-динитробензойная кислота (3,5-ДНБК). Так нитрование бензойной кислоты меланжем при 70-1000С в течение 20ч приводит к получению ДНБК с выходом 53% [4]. При использовании нитрующей смеси на основе дымящей ( 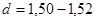 ) азотной и концентрированной серной кислот и при температурах 70-1450С за 6ч выход составил 35%, а за 24 ч - 55-58% [4].
) азотной и концентрированной серной кислот и при температурах 70-1450С за 6ч выход составил 35%, а за 24 ч - 55-58% [4].
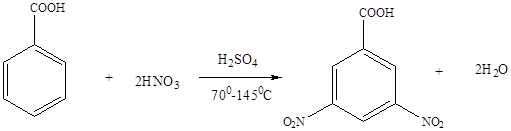
Немаловажное техническое преимущество нитрующей смеси перед меланжем состоит в том, что она может быть сохраняема в железной аппаратуре и передаваема по железным трубам, так как не разъедает этого металла. Количество серной кислоты рассчитывается по минимальной крепости (общей кислотности) смеси, при которой еще заметен нитрующий эффект. Если увеличить количество азотной кислоты при сохранении того же количества серной кислоты в правильно составленной нитрующей смеси, то часть азотной кислоты останется без взаимодействия. Если увеличить количество серной кислоты, это вызовет лишний расход серной кислоты в отработанной кислоте. На заводах часто при составлении нитрующей смеси пользуются отработанной кислотой предыдущих нитрований, соответствующим образом ее подкрепляя добавкой более крепкой серной и по расчету азотной кислоты [5].
Кроме того известно применение в качестве исходного продукта для получения ДНБК 3-нитробензойной кислоты. Но и при этом выход не превышал 66% [6].
Приведенные методы получения ДНБК отличаются невысоким выходом продукта, так как нитрование при высоких температурах способствует интенсивному протеканию нежелательных реакций окисления, которые в конечном счете могут стать причиной взрыва [6]. Однако снижение температуры, уменьшающее вероятность протекания побочных процессов, в равной степени снижает скорость и основной реакции нитрования. Последняя лимитируется скоростью образования и степенью сольватации иона нитрония 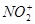 . На концентрацию и скорость образования ионов нитрония большое влияние также оказывает концентрация воды в нитрующей смеси (увеличения содержания воды ингибирует этот процесс) [6]. Очевидно, что благоприятными факторами, увеличивающими выход 3,5-ДНБК, будут снижение температуры нитрования, уменьшение содержания воды и увеличение избытка азотной кислоты в реакционной смеси.
. На концентрацию и скорость образования ионов нитрония большое влияние также оказывает концентрация воды в нитрующей смеси (увеличения содержания воды ингибирует этот процесс) [6]. Очевидно, что благоприятными факторами, увеличивающими выход 3,5-ДНБК, будут снижение температуры нитрования, уменьшение содержания воды и увеличение избытка азотной кислоты в реакционной смеси.
Установлено, что при замене серной кислоты в нитрующей смеси на олеум возможно проведение процесса в более мягких температурных условиях с повышенным выходом. Изучено влияние ряда факторов на нитрование бензойной кислоты дымящей азотной кислотой в среде 5-60% олеума [7].
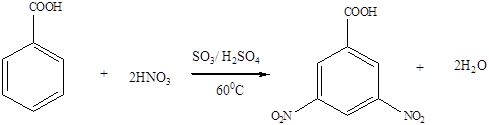
Таблица №1
Зависимость выхода 3,5-динитробензойной кислоты от температуры реакции.
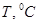
| Выход, % | 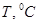
| Выход, % |
| 30 | Следы | 55 | 73 |
| 40 | 5 | 60 | 75 |
| 45 | 39 | 65 | 71 |
| 50 | 67 | 70 | 64 |
При исследовании зависимости выхода ДНБК от температуры (таблица) обнаружено, что максимальный выход ДНБК колеблется в области 55-650С. С увеличением температуры возрастает роль побочных процессов окисления и уменьшается выход ДНБК. Существенным фактором процесса нитрования является его длительность. При увеличении температуры синтеза с 50 до 700С максимум на кривой зависимости выхода ДНБК от длительности нитрования (рис.1) смещается с 12-14ч до 5-8ч, однако максимальный выход ДНБК при этом падает [4].
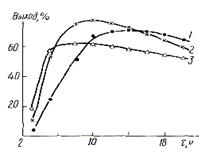
Рис1. Влияние длительности синтеза на выход ДНБК при различных температурах: 1-50; 2-60; 3-700C.
На получениие ДНБК существенно влияет избыток нитрующего агента (рис.2).
Оптимальным является соотношение азотной и бензойной кислот, равное (2,4-2,8):
1. Следует отметить, что увеличение этого соотношения в данных условиях может привести к спонтанному выбросу реакционной смеси.
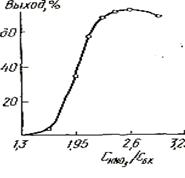
Рис2. Влияние избытка азотной кислоты на выход ДНБК.
Нитрование бензойной кислоты в олеуме с различным содержанием серного ангидрида (рис.3) показало, что выход ДНБК резко увеличивается в области содержания серного ангидрида 5-20% и в дальнейшем возрастает незначительно.
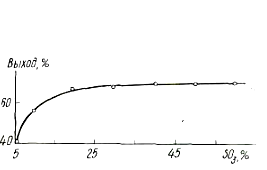
Рис3. Влияние содержания серного ангидрида в олеуме на выход ДНБК.
Таким образом, изучение приведенных выше закономерностей позволило в мягких условиях получить ДНБК высокой степени чистоты с выходом 70-80%. Ниже приведена методика нитрования бензойной кислоты в оптимальных условиях.
К охлажденной до 100С смеси 5,5мл дымящей азотной кислоты ( 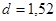 ) и 35 мл 20% олеума прибавляли порциями при перемешивании 12,2г (0,1 моль) бензойной кислоты. После гомогенизации смеси прибавляли по каплям еще 5,4мл
) и 35 мл 20% олеума прибавляли порциями при перемешивании 12,2г (0,1 моль) бензойной кислоты. После гомогенизации смеси прибавляли по каплям еще 5,4мл 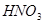 таким образом, чтобы общее количество ее составило 0,26моль. Затем в течение 1,5ч поднимали температуру до 600С. Через 5-6ч наблюдали выпадение осадка ДНБК. Еще через 6ч охлаждали реакционную смесь до комнатной температуры и выливали на 200г тонкоизмельченного льда. Осадок отфильтровали, промывали холодной водой и сушили при 1200С в течение 6ч. Выход 16,4г (77,3 мас. %).Т. пл. 205-2060С, по данным [7], т. пл. 204-2050С. ИК-спектр: 1550см-1 (
таким образом, чтобы общее количество ее составило 0,26моль. Затем в течение 1,5ч поднимали температуру до 600С. Через 5-6ч наблюдали выпадение осадка ДНБК. Еще через 6ч охлаждали реакционную смесь до комнатной температуры и выливали на 200г тонкоизмельченного льда. Осадок отфильтровали, промывали холодной водой и сушили при 1200С в течение 6ч. Выход 16,4г (77,3 мас. %).Т. пл. 205-2060С, по данным [7], т. пл. 204-2050С. ИК-спектр: 1550см-1 (  ), 1690 см-1 (
), 1690 см-1 ( 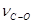 , димер) [8].
, димер) [8].
Патентный поиск
Патентный поиск проводился с целью найти известные ранее способы получения 3,5-динитробензойной кислоты, близкие по технологии к рассматриваемой в данном проекте, информацию о компаниях-производителях.
Патентный поиск производился на основе следующих бумажных и электронных носителей патентной информации:
Международный классификатор изобретений, 7-я редакция;
База данных Роспатента: http://www.Fips.ru (рефераты изобретений к заявкам РФ с 1994г.)
База данных Европейского Патентного Ведомства:
http://www.europea-patent office.ru
В результате был найден патент на получение 3,5-динитробензойной кислоты методом нитрования бензойной кислоты смесью олеума и азотной кислоты.
Таблица №2
Используемые патентные документы
| Номер патентного изобретения | Название патента | Дата публикации |
| 30504 Украина, МПК | Получение 3,5-динитробензойной кислоты | 15.11.2000г. |
Технологическая часть
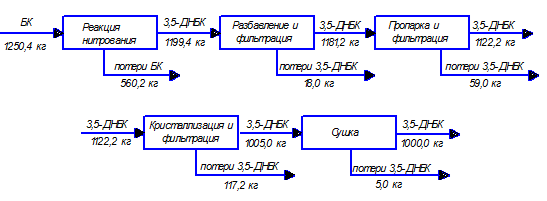
Описание технологической схемы
Процесс получения 3,5-динитробензойной кислоты проходит в четыре стадии. На первой стадии исходное сырье - 98% азотная кислота и 20% олеум, охлажденные до 100С, загружаются в реактор Р1, куда затем при помощи ленточного транспортера загружается бензойная кислота. Реакционная масса подогревается горячей водой из бойлерной до температуры 600С, после чего выдерживается в течение 6 часов. В случае превышения данного температурного порога срабатывает сирена и реакционная масса сбрасывается в аварийную емкость. Для отвода нитрозных газов, выделяющихся в процессе реакции предусмотрен трубопровод под вакуумом, по которому окислы азота подаются на абсорбцию.
Затем реакционная масса с помощью трубы передавливания подается в разбавитель Р2 из промежуточной емкости Е4. В аппарате происходит разбавление реакционной массы водой для снижения содержания в ней серной кислоты. Содержание серной кислоты понижается в разбавителе до 20%. Далее суспензия динитробензойной кислоты сбрасывается на вакуум-фильтр ВФ1 и промывается водой.
Маточник и промывные воды при этом собираются емкости Е5 и отправляется на регенерацию, а сырая динитробензойная кислота инжектируется на пропарку в аппарат Р3. Процесс пропаривания происходит при 1000С в течение 4 часов, ввиду сильной гидрофобности 3,5-динитробензойной кислоты.
Пропаренная ДНБК снова сбрасывается на вакуум-фильтр ВФ2 и промывается водой. Маточник и промывные воды при этом собираются в емкости Е6 и отправляется на разбавление. ДНБК загружается вручную в реактор Р4, куда загружается и этиловый спиртм из емкости Е7 для процесса кристаллизации. Процесс проходит при 800С. Затем кристаллизованная ДНБК фильтруется, сушится в сушильных шкафах и расфасовывается. Часть маточника при этом возвращается в процесс ввиду экономии этилового спирта.
Расчет материального баланса получения 3,5-динитробензойной кислоты
Выходы по стадиям:
1-я стадия - реакция нитрования - 55,2%
2-я стадия - разбавление и фильтрация - 98,5%
3-я стадия - пропарка и фильтрация - 95,0%
4-я стадия - кристаллизация и фильтрация - 89,5%
5-я стадия - сушка - 99,5%
Расчет количества бензойной кислоты, необходимого для получения 1000кг
3,5-динитробензойной кислоты:
Чтобы получить 1000 кг готовой динитробензойной кислоты, на стадию сушки необходимо подать с учетом выхода:
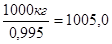 кг - поступает на стадию сушку
кг - поступает на стадию сушку
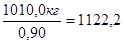 кг - поступает на стадию кристаллизации и фильтрации
кг - поступает на стадию кристаллизации и фильтрации
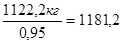 кг - поступает на стадию пропарки и фильтрации
кг - поступает на стадию пропарки и фильтрации
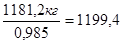 кг - поступает на стадию разбавления и фильтрации
кг - поступает на стадию разбавления и фильтрации
1-я стадия - реакция нитрования
Реакция нитрования протекает в 2 стадии:
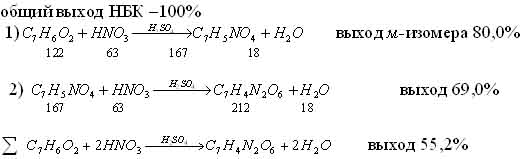
На первой стадии мононитрования бензойная кислота нитруется до изомеров в соотношении мета-: (орто - + пара-) =80: 20.
Таким образом, для получения 1199,4 кг динитробензойной кислоты необходимо бензойной кислоты:
Из 122,0 г/м бензойной кислоты образуется 212,0 г/м динитробензойной кислоты
Из 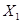 кг БК - 1199,4 кг ДНБК
кг БК - 1199,4 кг ДНБК
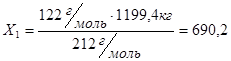 кг БК
кг БК
С учетом выхода на каждой стадии реакции получаем, что для получения 1000кг ДНБК необходимо:
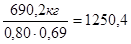 кг БК
кг БК
Бензойная кислота содержит 0,1% примесей, тогда общая масса БК, которую необходимо взять для реакции, составит:
 кг БК
кг БК
Рассчитаем количество мета-изомера, образующегося на первой стадии реакции, с учетом выхода:
Из 122,0 г/м БК - 167,0 г/м м-ДНБК
Из 1250,4кг БК - 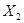 кг м-ДНБК
кг м-ДНБК
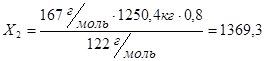 кг м-ДНБК
кг м-ДНБК
Проверка по второй стадии реакции с учетом выхода: из 167,0 г/м м-ДНБК - 212,0 г/м ДНБК, из 1369,3 кг м-ДНБК - 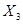 кг ДНБК
кг ДНБК
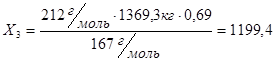 кг ДНБК
кг ДНБК
По методике к смеси 15,8г 98% азотной кислоты и 66,1г 20% олеума прибавляют порциями при перемешивании 12,2г бензойной кислоты.
Следовательно, для нитрования 1250,4кг бензойной кислоты потребуется пропорциональное количество азотной кислоты и олеума [8]:
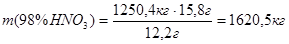 , в которой
, в которой
моногидрата - 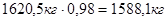
воды - 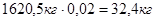
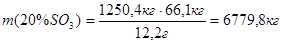 , в котором
, в котором
свободного 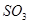 -
- 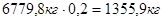
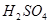 -
- 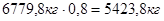
Рассчитаем количество требующегося по реакции моногидрата 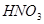 :
:
1) в первой реакции расходуется:
122,0 г/м БК - 63,0 г/м 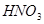
1250,4 кг БК - 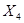 кг
кг 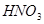
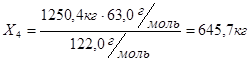
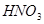
2) во второй реакции расходуется:
167,0 г/м БК - 63,0 г/м 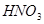
1369,3 кг БК - 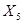 кг
кг 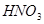
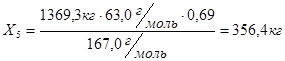
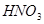
Таким образом, всего на нитрование идет моногидрата 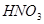 :
:
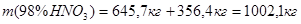
Следовательно, после нитрования осталось моногидрата 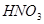 :
:
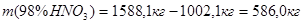
Рассчитаем количество образовавшейся по реакции 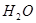 :
:
1) по первой реакции образуется:
122,0 г/м БК - 18,0 г/м 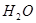
1250,4 кг БК - 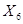 кг
кг 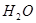
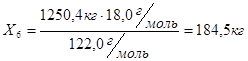
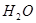
2) по второй реакции образуется:
167,0 г/м БК - 18,0 г/м 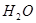
1369,3 кг БК - 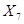 кг
кг 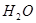
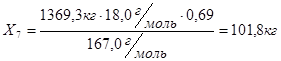
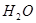
Таким образом, всего при нитровании образуется 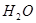 :
:
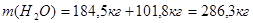
С учетом воды, содержащейся в азотной кислоте, общая масса составит:
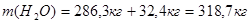
Рассчитаем количество 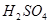 , образующейся в результате реакции при “связывании" воды сернистым ангидридом:
, образующейся в результате реакции при “связывании" воды сернистым ангидридом:
Х9 1355,9 Х8
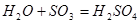
18,0 80,0 98,0
Из 80,0 г/м 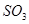 - 98,0 г/м
- 98,0 г/м 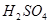
Из 1355,9 кг 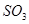 -
- 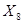 кг
кг 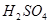
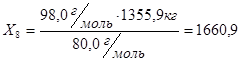 кг
кг 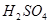
Следовательно, общее количество серной кислоты складывается из кислоты образующейся при связывании воды и кислоты, содержащейся в 20%олеуме:
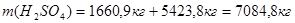
Рассчитаем количество 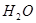 , вступающее в реакцию:
, вступающее в реакцию:
80,0 г/м 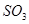 - 18,0 г/м
- 18,0 г/м 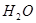
1355,9 кг 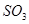 -
- 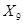 кг
кг 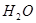
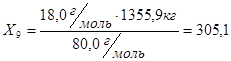 кг
кг 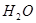
В процессе нитрования происходит раскисление орто - и пара-нитробензойных кислот и непрореагировавшей мета - нитробензойной кислоты [9].
586,0
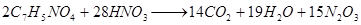
334,0 1764,0 616,0 342,0 1140,0
Рассчитаем общее количество нитробензойных кислот, участвующих в реакции раскисления:
334 г/м НБК - 1764,0 г/м 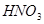
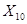 кг НБК - 586,0кг
кг НБК - 586,0кг 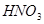
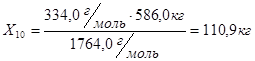 НБК
НБК
Рассчитаем количество газообразных продуктов и воды, выделившихся в результате реакции:
Из 334,0 г/м НБК - 616,0 г/м 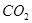
Из 110,9 кг НБК - 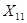 кг
кг 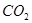
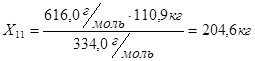
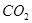
Из 334,0 г/м НБК - 1140,0 г/м 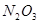
Из 110,9 кг НБК - 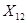 кг
кг 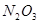
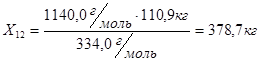
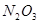
Из 334,0 г/м НБК - 342,0 г/м 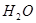
Из 110,9 кг НБК - 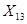 кг
кг 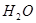
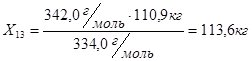
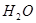
Следовательно, количество воды не вступившее в реакцию составит:
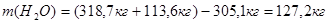
Рассчитаем общее количество непрореагировавших орто - и пара-нитробензойных кислот и мета - нитробензойной кислоты:
Из 122,0 г/м БК - 167,0 г/м 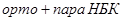
Из 1250,4кг БК - 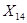 кг
кг 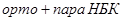
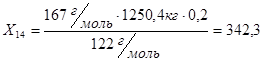 кг
кг 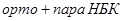
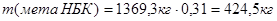
Следовательно, общее количество непрореагировавших орто - и пара-нитробензойных кислот и мета - нитробензойной кислоты равно:
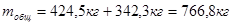
Таким образом, в суспензии ДНБК останется непрореагировавших НБК:
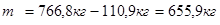
Таблица №3
Материальный баланс стадии нитрования
| Приход | кг | Расход | кг |
| 1. Бензойная кислота: ОВ 1250,4кг примеси 1,1кг | 1251,5 | 1. Суспензия ДНБК в отработанной кислоте:
ДНБК 1199,4 кг
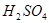 7084,8 кг 7084,8 кг
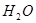 127,2 кг
НБК 655,9кг
примеси 1,1кг 127,2 кг
НБК 655,9кг
примеси 1,1кг
| 9068,4 |
| 2. Азотная кислота (98%): ОВ 1588,1 кг вода 32,4 кг | 1620,5 | 2. 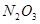
| 378,7 |
3. Олеум (20%):
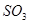 1355,9кг 1355,9кг
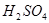 5423,8кг 5423,8кг
| 6779,8 | 3. 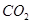
| 204,6 |
| Итого | 9651,8 | Итого | 9651,7 |
Таким образом, можно сделать вывод, что приведенное в методике [8] количество азотной кислоты недостаточно, так как в результате реакции остается значительное количество нераскисленных нитробензойных кислот.
Рассчитаем требующееся количество азотной кислоты для полного раскисления 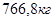 нитробензойных кислот:
нитробензойных кислот:
766,8
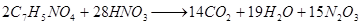
334,0 1764,0 616,0 342,0 1140,0
334 г/м НБК - 1764,0 г/м 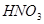
766,8кг НБК - 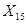 кг
кг 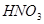
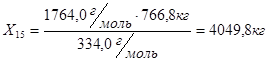
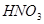
Азотная кислота, не вступившая в реакцию нитрования, частично остается в отработанной кислоте, частично расходуется в побочных реакциях, частично улетучивается в вентиляцию. Распределение азотной кислоты по этим статьям зависит от конкретных условий проведения реакции, то есть от температуры процесса, свойств и качества нитруемого соединения и т.д. На основании такого допущения определяем, что на раскисление пошло 20% моногидрата 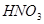 [9]:
[9]:
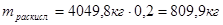
Следовательно, общая масса моногидрата:
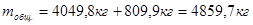
Для проведения реакции требуется 1002,1кг моногидрата азотной кислоты, тогда общее количество моногидрата азотной кислоты, необходимое для проведения реакции нитрования составит:
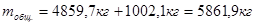
Следовательно, количество требующейся 98% азотной кислоты составит:
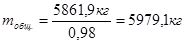
Рассчитаем количество газообразных продуктов и воды, выделившихся в результате реакции:
766,8 4049,8
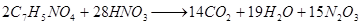
334,0 1764,0 616,0 342,0 1140,0
Из 1764,0 г/м 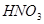 - 616,0 г/м
- 616,0 г/м 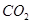
Из 4049,8 кг 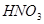 -
- 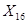 кг
кг 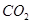
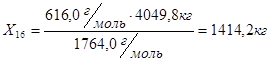
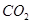
Из 1764,0 г/м 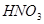 - 1140,0 г/м
- 1140,0 г/м 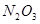
Из 4049,8 кг 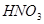 -
- 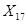 кг
кг 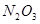
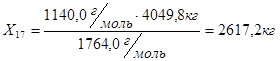
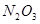
Из 1764,0 г/м 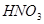 - 342,0 г/м
- 342,0 г/м 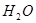
Из 4049,8 кг 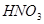 -
- 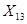 кг
кг 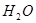
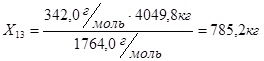
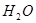
Для рассматриваемого процесса, можно принять, что 50 % оставшейся азотной кислоты расходуется на раскисление, 25 % - уносится в вентиляцию, а 25 % - остается в отработанной кислоте.
Рассчитаем количество продуктов, образующихся при раскислении 404,9 кг моногидрата азотной кислоты:
404,9
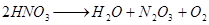
126 18 76 32
Из 126,0 г/м 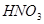 - 76,0 г/м
- 76,0 г/м 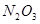
Из 404,9 кг 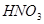 -
- 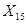 кг
кг 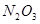
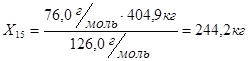
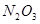
Из 126,0 г/м 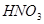 - 18,0 г/м
- 18,0 г/м 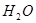
Из 404,9 кг 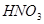 -
- 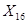 кг
кг 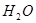
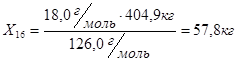
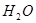
Из 126,0 г/м 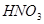 - 32,0 г/м
- 32,0 г/м 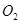
Из 404,9 кг 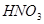 -
- 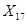 кг
кг 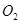
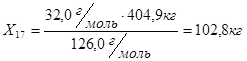
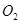
Следовательно, количество воды не вступившее в реакцию составит:
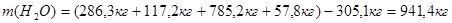
Таблица №4
Материальный баланс стадии нитрования
| Приход | кг | Расход | кг |
| 1. Бензойная кислота: ОВ 1250,4кг примеси 1,1кг | 1251,5 | 1. Суспензия ДНБК в отработанной кислоте:
ДНБК 1199,4 кг
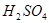 7084,8 кг 7084,8 кг
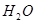 941,4 кг 941,4 кг
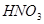 202,5кг
примеси 1,1кг 202,5кг
примеси 1,1кг
| 9429,2 |
| 2. Азотная кислота (98%): ОВ 5861,9 кг вода 117,2 кг | 5979,1 | 2. Газообразные продукты:
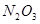 2861,4 кг 2861,4 кг
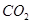 1414,2кг 1414,2кг
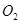 102,8кг
в вентиляцию 202,5 кг 102,8кг
в вентиляцию 202,5 кг
| 4580,9 |
3. Олеум (20%):
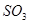 1355,9кг 1355,9кг
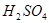 5423,8кг 5423,8кг
| 6779,8 | ||
| Итого | 14010,4 | Итого | 14010,1 |
2-я стадия - разбавление и фильтрация
В соответствии с методикой получения 3,5-динитробензойной кислоты необходимо снизить концентрацию серной кислоты в суспензии динитробензойной кислоты до 20%. Для этого рассчитаем необходимое количество воды, идущее на разбавление серной кислоты.
Массовая доля серной кислоты в исходной суспензии:
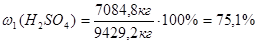
Требуемая массовая доля серной кислоты в суспензии:
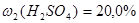
По правилу смешения запишем друг под другом массовые доли исходных растворов, а правее между ними - массовую долю раствора, который необходимо приготовить. При этом считаем, что вода - это раствор с массовой долей 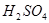 , равной нулю. Из большей массовой доли вычитаем заданную и записываем результат справа внизу, из заданной массовой доли вычитаем меньшую и записываем результат справа вверху [10].
, равной нулю. Из большей массовой доли вычитаем заданную и записываем результат справа внизу, из заданной массовой доли вычитаем меньшую и записываем результат справа вверху [10].
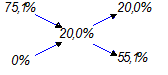
Затем вычисляем массу полученного раствора 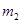 и массу воды
и массу воды 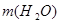 , которая потребуется для разбавления:
, которая потребуется для разбавления:
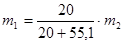 ,
,
где 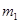 - масса суспензии, которая подается на разбавление.
- масса суспензии, которая подается на разбавление.
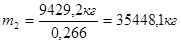 - масса полученного раствора
- масса полученного раствора
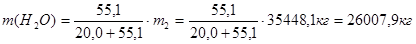
Динитробензойная кислота после фильтрации содержит 40% маточного раствора, образующегося в результате реакции:
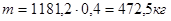
Рассчитаем процентное содержание компонентов в разбавленной суспензии:
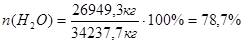
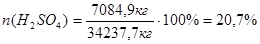
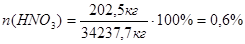
Следовательно, в 472,5 кг маточного раствора содержится пропорциональное количество компонентов:
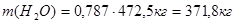
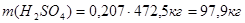
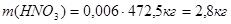
В результате, масса компонентов, содержащихся в отводимом маточном растворе уменьшится на соответствующее количество этих компонентов, содержащихся в динитробензойной кислоте:
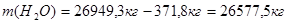
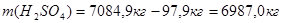
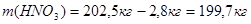
Рассчитаем потери динитробензойной кислоты с учетом выхода продукта:
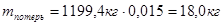
Таблица №5
Материальный баланс стадии разбавления и фильтрации
| Приход | кг | Расход | кг |
1. Суспензия ДНБК в отработанной кислоте:
ДНБК 1199,4 кг
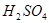 7084,8 кг 7084,8 кг
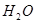 941,4 кг 941,4 кг
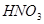 202,5кг
примеси 1,1кг 202,5кг
примеси 1,1кг
| 9429,2 | 1. Сырая ДНБК всего:
ДНБК 1181,2 кг
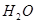 371,8 кг 371,8 кг
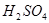 97,9 кг 97,9 кг
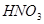 2,8 кг 2,8 кг
| 1653,7 |
| 2. Вода | 26007,9 | 2. Маточник всего:
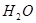 26577,5 кг 26577,5 кг
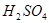 6987,0 кг 6987,0 кг
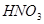 199,7 кг
примеси 1,1кг
ДНБК 18,0кг 199,7 кг
примеси 1,1кг
ДНБК 18,0кг
| 33783,3 |
| Итого | 35437,1 | Итого | 35437,0 |
Промывка
Зададимся модулем при промывке ДНБК 1 (1:
1), на 1 м. ч. ДНБК возьмем 1 м. ч. воды. Промывка осуществляется на вакуум-фильтре [9].
Динитробензойная кислота после промывки содержит 20% маточного раствора:
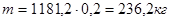
Рассчитаем процентное содержание компонентов в промытой ДНБК:
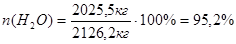
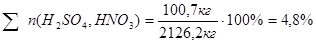
Следовательно, в 236,2 кг маточного раствора содержится пропорциональное количество компонентов:
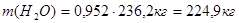
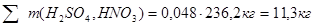
В результате, масса компонентов, содержащихся в отводимой промывной воде уменьшится на соответствующее количество этих компонентов, содержащихся в динитробензойной кислоте:
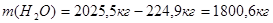
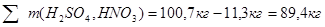
Таблица №6
Материальный баланс стадии промывки
| Приход | кг | Расход | кг |
1. Сырая ДНБК всего:
ДНБК 1181,2 кг
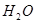 371,8 кг 371,8 кг
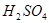 97,9 кг 97,9 кг
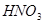 2,8 кг 2,8 кг
| 1653,7 | 1. Промытая ДНБК всего:
ДНБК 1181,2 кг
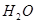 224,9 кг 224,9 кг
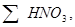 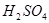 11,3 кг 11,3 кг
| 1417,4 |
| 2. Вода | 1653,7 | 2. Промывная вода всего:
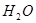 1800,6 кг 1800,6 кг
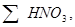 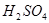 89,4 кг 89,4 кг
| 1890,0 |
| Итого | 3307,4 | Итого | 3307,4 |
Ориентировочно число промывок для жидких, веществ можно оценить по следующей формуле:
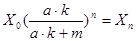
где 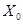 - начальная кислотность продукта;
- начальная кислотность продукта;
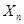 - кислотность продукта после n-ной промывки;
- кислотность продукта после n-ной промывки;
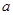 - количества жидкого вещества;
- количества жидкого вещества;
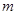 - количество промывной жидкости;
- количество промывной жидкости;


