 |
Главная |
Задание 28. Определение интенсивности фотосинтеза по накоплению углерода в листьях
|
из
5.00
|
Интенсивность фотосинтеза можно определять по различным параметрам - по поглощению углекислого газа, по выделению кислорода, по накоплению органического вещества в процессе фотоассимиляции. Методы последней группы наиболее просты, но требуют сложных приборов и могут быть использованы в лабораторных и полевых условиях.
Для определения органического вещества в листьях растений по количеству содержащегося в них углерода был предложен метод Ф.З.Бородулиной, принцип которого разработан ранее И.В.Тюриным для учета углерода в почве. Он основан на окислении органического вещества раствором калия двухромовокислого в смеси с концентрированной серной кислотой (хромовой смесью). При взаимодействии с углеродом бихромат разрушается, реакция идет по следующему уравнению:
2K2 Cr2 О7+8H2SO4+3С = 2К2SO4+2Cr2(SO4)3+2H2O+3CO2. (10)
Израсходованный на окисление углерода бихромат оттитровывается раствором соли Мора:
K2Cr7+6FeSO4+7H2SO4 = Cr2(SO4)3+3Fe2(SO4)3+K2S O4+7H2O. (11)
Ход работы. Для опыта использовать растения герани, предварительно выдержанные в темноте в течение суток для обеднения ассимилятами. У таких "голодных" растений на свету можно наблюдать более интенсивный фотосинтез.
Из листа герани пробочным сверлом высечь 3-4 диска. Лучше это сделать на одной половинке листа. Высечки использовать для анализа на содержание в них углерода. Лист поместить черенком в воду, выставить на свет, выдержать 1-2 часа, снова высечь 3-4 диска и определить в них количество углерода. Высечки до и после световой экспозиции следует брать одним и тем же сверлом с известным диаметром. Зная диаметр сверла, можно определить площадь высечек, взятых для анализа ( πr2 умножить на число дисков). Фотосинтез определять в двух - трех биологических повторностях, для чего до и после освещения листа при определении углерода брать 2-3 пробы. Это можно сделать на одном листе или использовать разные листья.
Чтобы определить углерод, диски из листьев нужно поместить в конические колбы на 100 мл. Туда же с помощью бюретки со стеклянным краном налить точно 10 мл 0,4 N раствора бихромата калия. Так как хромовая смесь является сильнейшим окислителем, то работать с ней надо очень осторожно. Недопустимо отмеривать её пипеткой!
Колбы закрыть стеклянными воронками и поместить на электрическую плитку для ускорения реакции окисления органического вещества. Нагревание следует вести строго определенное время - 5 минут (по песочным часам). Отсчет времени начать с момента появления пузырьков углекислого газа около дисков. Нагревание должно быть умеренным. Нельзя допускать бурного кипения смеси и выделения паров из воронки. При перегреве смесь может разрушиться.
При 5-минутном слабом кипении высечки должны полностью раствориться, окислиться. Колбы снять с плитки и охладить. Воронки снаружи и изнутри ополоснугь небольшим количеством воды (около 10 мл). В колбу добавить 5-6 капель индикатора (фенилантраниловую кислоту) и оттитровать содержимое 0,2 N раствором соли Мора. В присутствии хромовой смеси фенилантраниловая кислота дает бурую окраску раствора. По мере добавления соли Мора содержимое колбы светлеет, приобретает грязно-сиреневую окраску, которая от одной капли соли Мора может резко перейти в изумрудно-зеленую. Это конец титрования, важно его не пропустить, так как последующее прибавление соли Мора никаких изменений окраски не вызовет.
Иногда при титровании индикатор разрушается, особенно если раствор недостаточно охлажден. Поэтому целесообразно в середине титрования добавить еще 1-2 капли фенилантраниловой кислоты.
Параллельно с опытным титрованием провести контрольное (без высечек), чтобы найти соотношение 0,4 N раствора хромовой смеси и 0,2 N раствора cоли Мора. Методика титрования та же самая. Количество углерода определить по формуле:
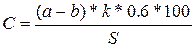 (12),
(12),
где С- количество углерода, мг/дм2
а - количество мл соли Мора при контрольном титровании;
b - количество мл соли Мора при титровании опытного образца;
к - поправка к титру соли Мора (ее можно не учитывать, если всю работу проводить с одним и тем же раствором соли Мора и бихромата);
0,6 - коэффициент пересчета количества соли Мора на количество углерода: 1 мл 0,2 N раствора соли Мора соответствует 0,6 мг углерода;
S – площадь высечек, см2.
Результаты оформить в виде таблицы (21).
Таблица 21.
Схема записи опыта
| Момент взятия проб | Пов-тор-ность | Взято K2Cr2O7, мл | Пошло на титрование соли Мора, мл | Площадь высечек, см2 | Кол-во углерода, мг/дм2 | Накопление углерода за время опыта 2 часа, мг/дм2 | Интенсив-ность фотосинтеза, мг С/ дм2/час | ||
| контроль | опыт | контроль | опыт | ||||||
| До освещения листа | 1 | ||||||||
| 2 | |||||||||
| средн. | |||||||||
| После освещения | 1 | ||||||||
| 2 | |||||||||
| средн. | |||||||||
По окончании работы рассчитать интенсивность фотосинтеза и сделать вывод.
МОДУЛЬ 3.
|
из
5.00
|
Обсуждение в статье: Задание 28. Определение интенсивности фотосинтеза по накоплению углерода в листьях |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

