 |
Главная |
Строение, физико-химические, электрические свойства.
|
из
5.00
|
Министерство образования и науки Украины
Харьковский национальный университет радиоэлектроники
Кафедра МЭПУ
Курсовая работа
По дисциплине «Материалы электронной техники»
На тему: Полупроводниковые материалы
Выполнил: Проверил:
Ст. гр. ЭЛ-05-2 Слипченко Н. И.
Сагитов А. А.
Харьков 2006
Реферат
Пояснительная записка содержит 36 стр., 8 рисунков, 1 таблицу, 8 используемых источников.
Объектом исследования является полупроводниковые материалы и твердые растворы, с целью рассмотрения сущности процессов, происходящих в материалах.
Введение
Научно-технический прогресс немыслим без электроники. Интенсивное развитие электроники связано с появлением новых разнообразных полупроводниковых приборов и интегральных микросхем, которые находят широкое применение в вычислительной технике, автоматике, радиотехнике и телевидении, в установках измерительной техники, медицины, биологии и т.д.
Полупроводники представляют собой обширную группу веществ, занимающих по величине удельного сопротивления промежуточное положение между диэлектриками и проводниками. Диапазон удельного сопротивления полупроводников при комнатной температуре условно ограничивают значениями 106-108Ом-м. Отличительным свойством полупроводников является сильная зависимость их удельного сопротивления от концентрации примесей. При введении примесей изменяется не только значение проводимости, но и характер ее температурной зависимости. У большинства полупроводников удельное сопротивление зависит также от температуры и других внешних энергетических воздействий (свет, электрическое и магнитное поле, ионизирующее излучение и т.д.). На управлении с помощью тепла, света, электрического поля, механических усилий электропроводностью полупроводников основана работа терморезисторов (термисторов), фоторезисторов, нелинейных резисторов (варисторов), тензорезисторов.
Полупроводниковые материалы по химическому составу можно разделить на простые и сложные.
Простыми (элементарными) полупроводниковыми материалами являются 12 химических элементов периодической системы: в III группе - В; в IV - С, Ge, Si. Sn (серое олово); в V - Р, As, Sb; в VI - S, Se, Те; в VII -I. В полупроводниковой электронике в основном применяют Ge и Si, а остальные используют в качестве легирующих добавок или компонентов сложных соединений.
Сложными полупроводниковыми материалами являются химические соединения, обладающие полупроводниковыми свойствами и включающие два, три и более элементов. Полупроводниковые соединения, состоящие из двух элементов, приято называть бинарными. Они обозначаются буквами латинского алфавита с цифровыми индексами (римские цифры над буквами обозначаются группу в периодической системе, а арабские цифры под буквами -стехиометрический коэффициент): АШВV (GaAs, JnSb), AIIBVI(CdS. ZnSe), AIVBVI(PbTe), AIVBIV(SiC), A2VB3VI(Bi2Te3) и т.д.
Твердые растворы полупроводниковых материалов обозначают символами
входящих в него элементов с индексами, которые указывают атомную долю этих элементов в растворе.
Для изготовления полупроводниковых приборов и устройств микроэлектроники используют как монокристаллы, так и поликристаллические материалы.
Ширина запрещенной зоны в полупроводниковых твердых растворах
Твердые растворы.
Признаком образования твердого раствора является сохранение типа решетки компонента—растворителя, но с иными размерами элементарной ячейки. Компоненты могут образовывать растворы неограниченной и ограниченной растворимости с разной степенью этого ограничения и разной температурной зависимостью предела насыщения раствора (предела растворимости).
Твердые растворы существенно расширили по сравнению с элементарными полупроводниками и полупроводниковыми соединениями набор электрофизических параметров, определяющих возможности применения материалов в конкретных полупроводниковых приборах.
Среди алмазоподобных полупроводников, в том числе соединений типа А В, распространены твердые растворы замещения. Необходимыми условиями образования твердых растворов являются кристаллохимическое подобие кристаллических решеток соединений-компонентов и близость их периодов идентичности. Наиболее хорошо изучены тройные твердые растворы, в которых замещение происходит лишь по узлам одной из подрешеток бинарного соединения (металлической или металлоидной). Состав таких твердых растворов принято характеризовать символами АхВ1-хС и АСуD1-у, где А и В обозначают элементы III группы, а С и D- элементы V группы. В формуле АхВ1-хС индекс х определяет мольную долю соединения АВ в твердом растворе. Если твердые растворы существуют во всем диапазоне концентраций, то х может изменяться от 0 до 1. В тройных твердых растворах имеет место статистически неупорядоченное распределение атомов замещаемых компонентов по узлам соответствующей подрешетки. С изменением состава твердого раствора наблюдается линейное изменение периода кристаллической решетки. Эта закономерность известна в кристаллохимии как закон Вегарда. Она позволяет определять состав твердого раствора по изменениям периода решетки с помощью дифракции рентгеновских лучей.
Как в бинарных соединениях АIIIВV, в твердых растворах не наблюдается существенных отклонений от стехиометрии, поэтому они просты по механизму легирования. Теми же методами, что и в бинарных соединениях, в них могут быть получены электронно-дырочные переходы. Температурные изменения электрических параметров также принципиально не отличаются от соответствующих зависимостей для соединений-партнеров.
1.2 Ширина запрещенной зоны
Особый интерес к твердым растворам обусловлен возможностью плавного управления шириной запрещенной зоны полупроводников путем изменения их компонентного состава. Возможные варианты этих зависимостей показаны на рис.1.1
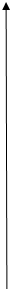 ΔЕ, эВ
ΔЕ, эВ

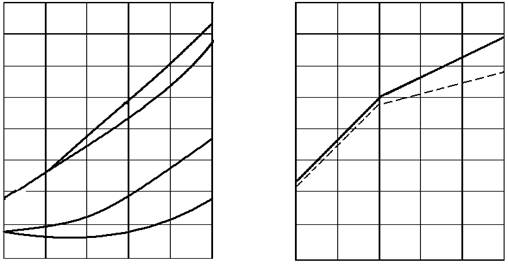
а) б)
Рис.1.1 Зависимость ширины запрещенной зоны от состава твердых растворов на основе соединений АIIIВV (Т=300К)
а-соединения-партнеры имеют одинаковую зонную структуру;
б-соединения-партнеры имеют различную зонную структуру
.Как видно из рисунка, зависимость ширины запрещенной зоны от состава в некоторых системах твердых растворов (Gaу In1-х As; InPу As1-у) очень близка к линейной, но может и существенно отличаться от нее, проявляя экстремум или излом при определенном соотношении между компонентами. Конкретный характер зависимости во многом определяется типом зонной структуры соединений-партнеров, т. е. положением
их энергетических долин в пространстве квазиимпульсов (k-пространстве).
В частности, излом зависимости ∆Э(х) аблюдается в тех системах твердых
растворах, в которых исходные бинарные соединения имеют зонные
структуры различных типов, т. е. различное расположение главных
энергетических минимумов зоны проводимости в k-пространстве.
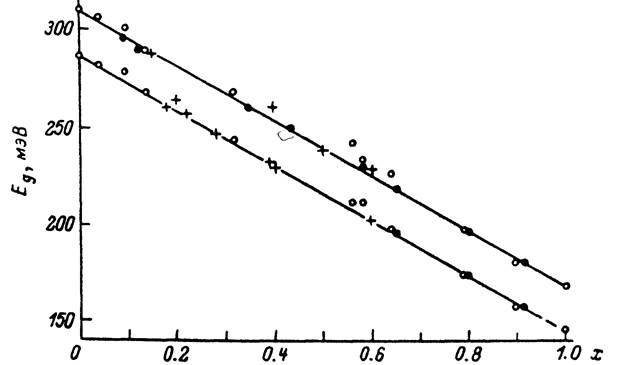
Рисунок 1.2 Зависимость Е g(х) для твердого раствора PbxS1-xSe
Вместе с тем, как и в металлических сплавах, эффекты статистического разупорядочения в кристаллической решетке оказывают сильное влияние на удельную теплопроводность полупроводников, которая у твердых растворах оказывается заметно ниже, чем у бинарных соединений. Например, у твердых растворов GaAs0,5P0,5 и Al0,5Ga0,5As значение удельной теплопроводности примерно на порядок меньше, чем у чистых кристаллов GaAs.
Изменение ширины запрещенной зоны у твердых растворов сопровождается соответствующим смещением спектров оптического поглощения и пропускания, люминесценции и фоточувствительности. С изменением состава твердого раствора изменяются значения диэлектрической проницаемости и показателя преломления, происходит смещение примесных энергетических уровней. В ряде систем при определенном соотношении между компонентами можно получить качественное новое сочетание свойств. Так, в твердых растворах GaAs1-уPу и AlхGa1-хAs (с х и у порядка 0,3 ÷ 0,4) сочетаются достаточно широкая запрещенная зона ( ∆Э>1,7эВ) с высоким квантовыми выходом межзонной излучательной рекомбинации. Такие материалы используют для создания эффективных электролюминесцентных источников красного излучения (светодиодов и лазеров). Твердые растворы
GaхIn1-хP c х=0,5-0,7 обладают эффективной люминесценцией в желто-зеленой области спектра.
Получение однородных твердых растворов заданного состава представляет собой весьма трудную технологическую задачу. Обычными методами кристаллизации из расплава в лучшем случае удается получать однородные поликристаллические слитки. Монокристаллические слои твердых растворов, используемых в приборных структурах, осаждают исключительно методами эпитаксии. Эпитаксию твердых растворов GaAs1-уPу осуществляют на подложках GaAs или GaP с помощью химических реакций, протекающих в газовой фазе. В то же время наиболее совершенные эпитаксиальные слои AlхGa1-хAs, AlхGa1-хSb,
GaхIn1-хAs, GaхIn1-хP получают методом жидкофазовой эпитаксии с использованием галлия или индия в качестве растворителя.
1.3Изопериодные гетероструктуры
Твердые растворы открывают широкие возможности создания гетеропереходов и приборов на их основе. Под гетеропереходом понимают контакт двух полупроводников с различной шириной запрещенной зоны. Для получения гетеропереходов со свойствами идеального контакта необходимо выполнить ряд условий совместимости материалов по механическим, кристаллохимическим и термическим свойствам. Решающим критерием при выборе материалов контактной пары является соответствие периодов их кристаллических решеток и температурных коэффициентов линейного расширения. Если компоненты гетеропары обладают взаимной растворимостью во всем интервале концентраций, то появляется уникальная возможность создавать гетеропереходы между химическим соединением АС и твердым раствором АхВ1-хС на его основе. Это обстоятельство позволяет плавно изменять свойства материалов на контактной границе, что важно при изготовлении ряда приборов оптоэлектроники и прежде всего – источников и приемников излучения. Среди полупроводников типа АIIIВVнаилучшими парами материалов для создания идеальных гетеропереходов являются системы GaAs-AlхGa1-хAs и GaSb-AlхGa1-хSb.
Преимущества указанных гетеропар заключаются в том, что период решетки твердых растворов AlхGa1-хAs и AlхGa1-х Sb слабо зависит от состава и близок к периоду решетки бинарного соединения (собственно GaAs и GaSb).
Дополнительные степени свободы для варьирования параметрами сопрягаемых полупроводниковых материалов при получении идеальных гетеропереходов возникают при использовании четырехкомпонентных твердых растворов типа АхВ1-хСуД1-у. Среди этой группы материалов наиболее интересными и изученными являются твердые растворы GaхIn1-хAs1-уPу, в которых имеет место замещение по обеим подрешеткам при сохранении общей стехиометрии, т. е. равенство суммарных количеств атомов металла и металлоида. В качестве исходных компонентов такого твердого раствора можно рассматривать четыре бинарных соединения: GaP, InP, GaAs и InAs. Особый интерес представляют твердые растворы GaхIn 1-хAs1-уPу с изопериодическим замещением по отношению к InP. В зависимости от состава их запрещенная зона может изменяться в пределах от 0,75 до 1,35 эВ.
Инжекционные лазеры на основе гетеропары InP- Ga In As P переспективны для применения в волоконно-оптических линиях связи, поскольку спектральный диапазон их излучения соответствует минимальным оптическим потерям кварцевого волокна.
Германий
Строение, физико-химические, электрические свойства.
Германий (лат. Germanium), Ge, химический элемент IV группы периодической системы Менделеева; порядковый номер 32, атомная масса 72,59; твёрдое вещество серо-белого цвета с металлическим блеском. Природный германий представляет собой смесь пяти стабильных изотопов с массовыми числами 70, 72, 73, 74 и 76.
Существование и свойства германия предсказал в 1871 Д. И. Менделеев и назвал этот неизвестный еще элемент «экасилицием» из-за близости свойств его с кремнием. В 1886 немецкий химик К. Винклер обнаружил в минерале аргиродите новый элемент, который назвал германий в честь своей страны; Германий оказался вполне тождествен «экасилицию». До 2-й половины 20 в. практическое применение германий оставалось весьма ограниченным. Промышленное производство германия возникло в связи с развитием полупроводниковой электроники.
Общее содержание германия в земной коре 7.10—4% по массе, т. е. больше, чем, например, сурьмы, серебра, висмута. Однако собственные минералы германия встречаются исключительно редко. Почти все они представляют собой сульфосоли: германит Cu2(Cu, Fe, Ge, Zn)2 (S, As)4, аргиродит Ag8GeS6, конфильдит Ag8(Sn, Ce) S6 и др. Основная масса германия рассеяна в земной коре в большом числе горных пород и минералов: в сульфидных рудах цветных металлов, в железных рудах, в некоторых окисных минералах (хромите, магнетите, рутиле и др.), в гранитах, диабазах и базальтах. Кроме того, германий присутствует почти во всех силикатах, в некоторых месторождениях каменного угля и нефти.
Германий кристаллизуется в кубической структуре типа алмаза, параметр элементарной ячейки а = 5, 6575. Плотность твёрдого германия 5,327 г/см3 (25°С); жидкого 5,557 (1000°С); tпл 937,5°С; tkип около 2700°С; коэффициент теплопроводности ~60 вт/(м (К), или 0,14 кал/(см (сек (град)при 25°С. Даже весьма чистый германий хрупок при обычной температуре, но выше 550°С поддаётся пластической деформации. Твёрдость германия по минералогической шкале 6—6,5; коэффициент сжимаемости (в интервале давлений 0—120 Гн/м2 или 0—12000 кгс/мм2) 1,4·10—7 м2/мн (1,4·10—6 см2/кгс); поверхностное натяжение 0,6 н/м (600 дин/см).Германий — типичный полупроводник с шириной запрещенной зоны 1,104·10—19, или 0,69 эв (25°С); удельное электросопротивление германия высокой чистоты 0,60 ом (м (60 ом (см) при 25°С; подвижность электронов 3900 и подвижность дырок 1900 см2/в. сек (25°С) (при содержании примесей менее 10—8%). Прозрачен для инфракрасных лучей с длиной волны больше 2 мкм.
Соединения германия
В химических соединениях германий обычно проявляет валентности 2 и 4, причём более стабильны соединения 4-валентного германия. При комнатной температуре германий устойчив к действию воздуха, воды, растворам щелочей и разбавленных соляной и серной кислот, но легко растворяется в царской водке и в щелочном растворе перекиси водорода. Азотной кислотой медленно окисляется. При нагревании на воздухе до 500—700°С германий окисляется до окиси GeO и двуокиси GeO2. Двуокись германия — белый порошок с tпл 1116°С; растворимость в воде 4,3 г/л (20°С). По химическим свойствам амфотерна, растворяется в щелочах и с трудом в минеральных кислотах. Получается прокаливанием гидратного осадка (GeO2. nH2O), выделяемого при гидролизе тетрахлорида GeCl4. Сплавлением GeO2 с др. окислами могут быть получены производные германиевой кислоты — германаты металлов (In2CeO3, Na2Ge О3 и др.) — твёрдые вещества с высокими температурами плавления.
При взаимодействии Г. с галогенами образуются соответствующие тетрагалогениды. Наиболее легко реакция протекает с фтором и хлором (уже при комнатной температуре), затем с бромом (слабое нагревание) и с иодом (при 700—800°С в присутствии CO). Одно из наиболее важных соединений германия тетрахлорид GeCl4 — бесцветная жидкость; tпл —49,5°С; tkип 83,1°С; плотность 1,84 г/см3 (20°С). Водой сильно гидролизуется с выделением осадка гидратированной двуокиси. Получается хлорированием металлического германия или взаимодействием GeO2 с концентрированной НС1. Известны также дигалогениды Г. общей формулы GeX2, монохлорид GeCl, гексахлордигерман Ge2Cl6 и оксихлориды Г. (например, GeOCl2).
Сера энергично взаимодействует с германием при 900—1000°С с образованием дисульфида GeS2 — белого твёрдого вещества, tпл 825°С. Описаны также моносульфид GeS и аналогичные соединения германия с селеном и теллуром, которые являются полупроводниками. Водород незначительно реагирует с Г. при 1000—1100°С с образованием гермина (GeH) x — малоустойчивого и легко летучего соединения. Взаимодействием германидов с разбавленной соляной кислотой могут быть получены германоводороды ряда GenH2n+2 вплоть до Ge9H20. Известен также гермилен состава GeH2. С азотом германий непосредственно не реагирует, однако существует нитрид Ge3N4, получающийся при действии аммиака на германий при 700—800°С. С углеродом германий не взаимодействует. Германий образует соединения со многими металлами — германиды.
Известны многочисленные комплексные соединения германия, которые приобретают всё большее значение как в аналитической химии германия, так и в процессах его получения. Германий образует комплексные соединения с органическими гидроксилсодержащими молекулами (многоатомными спиртами, многоосновными кислотами и др.). Получены гетерополикислоты германия. Так же, как и для других элементов IV группы, для германия характерно образование металлорганических соединений, примером которых служит тетраэтилгерман (C2H5)4 Ge3.
Получение германия.
В промышленной практике германий получают преимущественно из побочных продуктов переработки руд цветных металлов (цинковой обманки, цинково-медно-свинцовых полиметаллических концентратов), содержащих 0,001—0,1% германия. В качестве сырья используют также золы от сжигания угля, пыль газогенераторов и отходы коксохимических заводов. Первоначально из перечисленных источников различными способами, зависящими от состава сырья, получают германиевый концентрат (2—10% германия). Извлечение германия из концентрата обычно включает следующие стадии:
1) хлорирование концентрата соляной кислотой, смесью её с хлором в водной среде или др. хлорирующими агентами с получением технического GeCl4. Эти процессы можно представить уравнениями реакций:
GeO2+4HCl=GeCl4+2H2O.
2) Гидролиз GeCl4 и прокаливание продуктов гидролиза до получения GeO2. Температура кипения полученного тетрахлорида германия 83° C. Так как вместе с ним в сконденсированной жидкости имеются и другие соединения, то его подвергают ректификации и экстракции примесей концентрированной HCl. После этого тетрахлорид германия переводят в двуокись по уравнению
GeCl4+(x+2)H2O=GeO2xH2O+4HCl.
3) Восстановление GeO водородом или аммиаком до металла. Полученную чистую двуокись германия восстанавливают в трубчатой электрической печи водородом. Восстановление протекает по реакции
GeO2+2H2=Ge+2H2O,
При температуре 600°C, в течение 20-50 мин, после чего лодочка с восстановленным германием передвигается в зону более высоких температур и при 1000-1100°C происходит сплавление.
Для выделения очень чистого германия, используемого в полупроводниковых приборах, проводится зонная плавка металла. Необходимый для полупроводниковой промышленности монокристаллический германий получают обычно зонной плавкой или методом Чохральского.
2.4 Применение германия
Германий — один из наиболее ценных материалов в современной полупроводниковой технике. Он используется для изготовления диодов, триодов, кристаллических детекторов и силовых выпрямителей.Германиевые диоды и триоды нашли широкое применение в радиоприемниках и телевизорах, счетно-решающих устройствах и в разнообразной измерительной аппаратуре.Германий применяют и в других первостепенно важных областях современной техники: для измерения низких температур.
Монокристаллический германий применяется также в дозиметрических приборах и приборах, измеряющих напряжённость постоянных и переменных магнитных полей. Важной областью применения германия является инфракрасная техника, в частности производство детекторов инфракрасного излучения, работающих в области 8—14 мк. Перспективны для практического использования многие сплавы, в состав которых входят германий, стекла на основе GeO2 и др. соединения германия.
Полупроводник германий нашел применение при решении другой важной проблемы – созданию сверхпроводящих материалов, работающих при температуре жидкого водорода, а не жидкого гелия. Водород, как известно, переходит из газообразного в жидкое состояние при температуре – 252,6°C, или 20,5°К. В начале 70-х годов была получена пленка из сплава германия с ниобием толщиной всего в несколько тысяч атомов. Эта пленка сохраняет сверхпроводимость при температуре 23,2°К и ниже.
2.5 Заменители германия
Более дешевый кремнии и сплавы Ga, In,Se,. Те могут заменить германий в некоторых электронных применениях. Замена металлического германия подложками из стекла в инфракрасных системах не всегда эффективна.
Исследуются возможности использования новых катализаторов для замены германия при получении пластиков. Тенденция к обесцвечиванию пластиков способствует появлению катализаторов на алюминиевой и титановой основе, при этом также снижаются затраты на производство пластиков.
|
из
5.00
|
Обсуждение в статье: Строение, физико-химические, электрические свойства. |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

