 |
Главная |
Квалификация функционирования
|
из
5.00
|
(OPERATIONAL QUALIFICATION - OQ)
8.1. OQ проводится после IQ. Проверяется и оценивается работоспособность объекта квалификации (технологическое и лабораторное оборудование, инженерные системы, оснащенные (чистые( помещения и др.) путем тестирования функций и параметров оборудования/систем с использованием, при необходимости, средств измерений.
8.2. На стадии OQ уточняются стандартные операционные процедуры, проекты которых были разработаны на стадии IQ.
8.3. При OQ определяются критические условия/параметры оборудования/систем. На стадии OQ допускается, там, при необходимости, использование имитатора продукта. При изучении критических параметров следует учесть случаи, когда значения параметров равны верхним или нижним допустимым пределам в эксплуатации. Обычно это относится к "наихудшему случаю".
8.4. При проведении валидации/квалификации оснащенных (чистых( помещений и зон (производственных и лабораторных) измеряются и определяются необходимые параметры воздушной среды в порядке, установленном действующими нормативными документами. На стадии OQ не проводится микробиологический контроль воздушной среды (чистых( помещений и зон.
8.5. На стадии OQ важно доказать, что все контрольные эксплуатационные функции/параметры соответствуют критериям приемки, оборудование/системы работают правильно и надежно при нормальных и наихудших условиях.
Для сложного или объемного оборудования допускается проведение проверки/приемки на сборочной площадке поставщика, но это не заменяет выполнение стадии OQ на предприятии.
8.6. В случае невыполнения критериев/требований IQ, необходимо установить дальнейший порядок корректирующих действий и сроки их выполнения.
Квалификация эксплуатации
(Performance Qualification - PQ).
9.1. PQ проводится после IQ и OQ. Проверяется и оценивается надежность и эффективность эксплуатационных параметров объекта квалификации (технологическое оборудование, инженерные системы, функционирующие (чистые( помещения и др.) путем тестирования функций и параметров оборудования/систем с использованием имитатора препарата или образцов одной серии реального продукта, а также необходимых средств измерений.
9.2. Квалификацию каждой единицы технологического оборудования целесообразно завершать стадией PQ, чтобы перейти к валидации процессов (PV), по следующим причинам:
9.2.1. Одна единица оборудования часто используется для производства нескольких видов/наименований продукции.
9.2.2. В одном технологическом процессе, как правило, используется значительное количество оборудования разных типов.
9.3. Стадия PQ является конечной при валидации инженерных систем (обеспечение чистым воздухом, водой, паром, инертным газом, сжатым воздухом и др.), так как каждая из них вырабатывает свой конечный (продукт(. В этом случае, стадия PQ в отношении систем, по сути, тождественна валидации процесса (PV).
9.4. При проведении валидации/квалификации функционирующих (чистых( помещений (производственных и лабораторных) оценивается соответствие фактического значения концентрации жизнеспособных (колониеобразующих) микроорганизмов в 1 м3 воздуха нормам, установленным Стандартом отрасли ОСТ 42-510 (GMP) для помещений и зон всех классов чистоты (А, В, С, D).
9.5. В случае невыполнения критериев/требований PQ, необходимо установить причины отклонений и принять меры по их корректировке (с документальным подтверждением) до начала валидации процессов (PV).
Валидация процессов
(Process Validation - PV)
10.1. PV проводится после стадий квалификации в зависимости от вида валидации.
10.2. Валидация технологических процессов проводится с использованием образцов не менее трех серий реального продукта с целью доказательство и предоставление документального свидетельства, что процесс (в пределах установленных параметров) обладает повторяемостью и приводит к ожидаемым результатам при производстве полупродукта или готового продукта требуемого качества.
10.3. При PV проводится валидация аналитических методов, используемых для контроля процессов.
Валидация аналитических методов состоит в определении: точности, воспроизводимости, чувствительности, устойчивости (межлабораторная воспроизводимость), линейности и других метрологических характеристик. В данном документе валидация аналитических методов подробно не рассматривается
10.4. Валидация вспомогательных процессов (очистки, санитарной обработки и др.) проводится после проведения валидации аналитических методов.
10.5. В случае отрицательных результатов, полученных на стадии PV, необходимо устранить отклонения до начала производства продукции.
Приложение А. Примерное содержание отчета о проведении валидации
(Рекомендуемое)
Отчет о проведении валидации включает в себя следующие положения, информацию, документы:
1. Объект валидации и его идентификация, дата (период) и место проведения.
2. Цель и вид валидации.
3. Идентификация валидаторов (ФИО, должность, подпись, дата);
4. Исходная информация:
4.1. Общая характеристика объекта, включая критические параметры.
4.2. Перечень документации (регламенты, фармстатьи, проектная документации, инструкции, спецификации, сертификаты, паспорта и др.).
4.3. Перечень методик проведения испытаний (измерений, отбора проб и др.) и критериев оценки результатов.
4.4. Сведения о привлеченных организациях или экспертах.
5. Сведения о калибровке/поверке:
5.1. Средств измерений (приборы, датчики, весы и др.), установленных в оборудовании, инженерных системах, помещениях и др.
5.2. Средств измерений, используемых при проведении валидации/ квалификации.
6. Документы:
6.1. Валидационные протоколы всех стадий квалификации (DQ,IQ,OQ,PQ) и валидации процессов (PV), или ссылка на них с указанием места хранения.
6.2. Протоколы (отчеты и др.) с данными и результатами испытаний, отбора проб и т.п.
7. Анализ полученных результатов, в т.ч. по:
7.1. Проверке критических условий и параметров.
7.2. Выявленным отклонениям (изменениям), требующим действий по корректировке.
7.3. Условиям охраны труда и технике безопасности.
8. Вывод по результатам валидации.
9. Сроки проведения повторной плановой валидации.
Приложение Б. Схема этапов валидации
(Информационное)
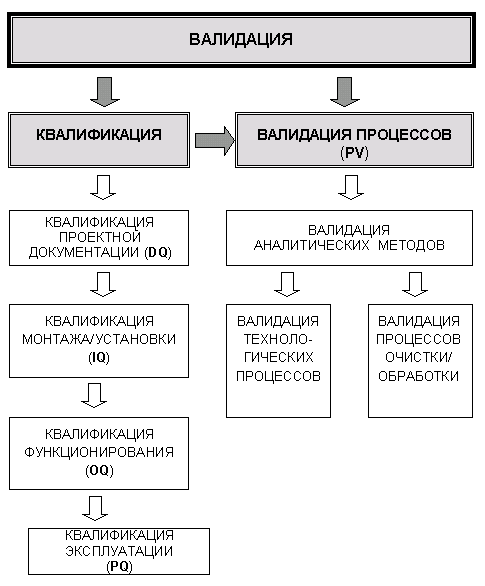
Примечание: Валидация компьютерных систем, при необходимости, проводится на разных этапах с учетом их специфики. В данном документе валидация компьютерных систем подробно не рассматривается
Приложение В. Примерное содержание валидационного протокола
(Рекомендуемое)
Валидационные протоколы включают в себя следующие положения, информацию, документы:
1. Объект валидации/квалификации и его идентификация, дата(период) и место проведения.
2. Вид, стадия и этап валидации/квалификации.
3. Идентификация валидаторов (ФИО, должность, подпись, дата), сведения о привлеченных организациях или экспертах.
4. Распределение ответственности за подготовку, согласование, утверждение и хранение протокола.
5. Термины и определения.
6. Процедуры и методы валидации/квалификации (применительно к объекту).
7. Критерии оценки условий параметров.
8. Нормативная документация (ГОСТы, ОСТы, регламент, МУ и др.).
9. Сведения о калибровке/поверке средств измерений, используемых при проведении квалификации и валидации.
10. Сведения о калибровке/поверке средств измерений (приборы, датчики и др.), установленных в оборудовании, инженерных системах, помещениях и др.;
11. Результаты проверки и оценки тестов (испытаний, измерений, отбора проб и др.).
12. Выявленные отклонения/изменения и меры по их корректировке.
13. Комментарии и рекомендации (в т.ч. по срокам проведения повторной плановой валидации/квалификации).
14. Вывод по результатам валидации/квалификации.
Примечание:
На каждой странице валидационного протокола рекомендуется приводить краткую информацию (название предприятия, наименование протокола, этап/вид/стадия, код, страница ... из ...).
Приложение Г. Примерное содержание валидационного плана
(Рекомендуемое)
Валидационный план включает в себя следующие положения, информацию, документы:
1. Цели и задачи валидации (политика предприятия в отношении проведения валидации).
2. Распределение ответственности за проведение валидации/квалификации, написание и утверждение валидационных протоколов, и др.
3. Термины и определения.
4. Нормативные ссылки.
5. Организационная структура (сценарий) валидации, включая:
5.1. Вид, стадии и этапы валидации/квалификации.
5.2. Место и время проведения работ. Привлекаемые сторонние организации и/или эксперты.
5.3. Формы валидационных протоколов, отчетов, сводных таблиц и др.
5.4. Калибровка/поверка средств измерений.
5.5. Перечень работ по валидации процессов и квалификация условий производства (технологическое и лабораторное оборудование, инженерные системы, "чистые" помещения и др.). При этом обосновывается исключение отдельных объектов/процедур валидации.
5.6. Требования к персоналу, учесть в проведении валидации/квалификации.
5.7. Условия периодической корректировки валидационного плана.
6. Описание предприятия, производства/участка, процесса, оборудования, инженерных систем, продукта и др. (в т.ч. даются ссылки на другие документы).
7. Перечень методик проведения испытаний (измерений, отбора проб и др.). Критерии оценки результатов, критические условия/параметры.
8. График проведения работ рекомендуется оформить в виде таблицы с указанием наименования объекта валидации/квалификации, стадии/этапов, валидаторов, ответственных за согласование/утверждение протоколов, времени и места, идентификация СОПов, стоимости и т.п.
9. Необходимые приложения (чертежи, схемы и др.).
Приложение Д. Библиография
(Информационное)
1. ИСО 9001 : 2000 Система менеджмента качества. Требования.
2. Надлежащая производственная практика лекарственных средств. Киев, "Морион" 1999.
3. Нормирование фармацевтического производства. Обеспечение качества продукции. Москва, "Ремедиум" 2001г.
|
из
5.00
|
Обсуждение в статье: Квалификация функционирования |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

