 |
Главная |
Расчет кривой титрования слабой кислоты сильным основание.
|
из
5.00
|
Содержание.
1.Задание.
2.Расчет кривой титрования сильной кислоты сильным основанием.
3. Определение индикатора и индикаторной ошибки.
4 Расчет кривой титрования слабой кислоты сильным основанием.
5. Определение индикатора и индикаторной ошибки.
Задание: расчитать и построить кривые титрования в 100 мл. 0,1 молярного раствора HCl 100 мл. 0,1 молярного раствора бензойной кислоты (К 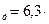 10-5). Выбрать индикатор и рассчитать индикаторную ошибку. При расчете кривой титрования необходимо рассчитать начальную точку; 90; 99; 99,9; точку эквивалентности и после точки эквивалентности (101; 110). Кривые титрования строят в одной системе координат.
10-5). Выбрать индикатор и рассчитать индикаторную ошибку. При расчете кривой титрования необходимо рассчитать начальную точку; 90; 99; 99,9; точку эквивалентности и после точки эквивалентности (101; 110). Кривые титрования строят в одной системе координат.
Расчет кривой титрования сильной кислоты сильным основание.
HCl- сильная кислота;
NaOH- сильное основание.
1.При вычислении значение pH в растворах сильных кислот и оснований, являющихся сильными электролитами, концентрацию ионов Н+ или ОН- принимают практически равной общей концетрации кислот или оснований .
Тогда значение рН в исходном растворе кислоты определяется
рН=-lg 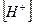

pH=-lg0,1=1
2.Концентрация остаточной кислоты, а, следовательно, и концентрацию ионов водорода в промежуточных точках титрования (до точки эквивалентности) рассчитывается по формуле:
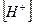 =
=  ; рН=-lg
; рН=-lg 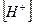
50%: 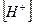 =
= 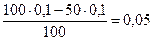
рН=-lg 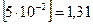
90%: 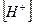 =
= 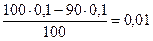
pH=-lg10-2=2
99%: 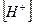 =
= 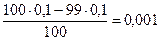
рН=-lg10-3=3
99,9%: 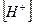 =
= 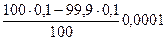
рН=-lg10-4=4
2.В точке эквивалентности.
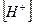 =
= 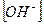 =10-7
=10-7
рН=7
3. После точки эквивалентности.
Теперь проводят расчет концентрации избытка реагента (щелочи):
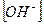 =
= 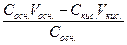 ; рОН=-lg10-4; рН=14-рОН
; рОН=-lg10-4; рН=14-рОН
100,1%: 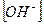 =
= 
pOH=-lg10-4=4
pH=14-4=10
101%: 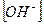 =
= 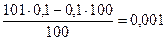
рОН=-lg10-3=3
pH=14-3=11
110%: 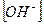 =
= 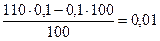
рОН=-lg10-2=2
pH=14-2=12
Определение индикатора и индикаторной ошибки.
При титровании сильной кислоты сильным основание скачек титрования определяется в 6 единиц рН, от 4 до 9. В этих границах рН свою окраску изменяют многие индикаторы., например, метиловый красный (4,4-6,2). Значит, рТ будет находиться по формуле:
рТ= 
Проанализировав значения в точке эквивалентности (рН=7) и значение рТ=5,3, можно сделать вывод что мы не до титровали, поэтому мы находим кислотную ошибку.
∆НА  ; ∆ОН=
; ∆ОН= 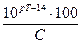
∆НА= 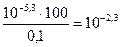
∆ОН= 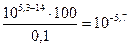
Расчет кривой титрования слабой кислоты сильным основание.
1.До начала титрования, т.е. в чистом растворе одноосновной слабой кислоты концентрации 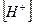 и
и  равны между собой, а концентрация
равны между собой, а концентрация 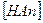 практически равна концентрации исходной кислоты при условии, что степень диссоциации достаточно мала.
практически равна концентрации исходной кислоты при условии, что степень диссоциации достаточно мала.
В соответствии с этим константа диссоциации представлена в виде:
Кк-ты= 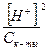
рН= 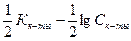
рК=-lgKд
рК=-lg6,3 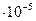 =4,21
=4,21
pH= 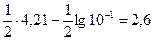
2.В промежуточных точках титрования слабой кислоты сильным основание образуется буферный раствор, содержащий одновременно свободную слабую кислоту и соль этой кислоты.
Расчет величины рН в этом случае так же рассчитывается из Кк-ты, которая в присутствии соли может быть представлена в виде:
К= 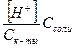
рН=рКт-ты-lg 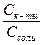
50%: 4,21-lg 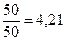
90%: 4,21-lg 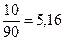
99%: 4,21-lg 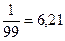
99,9%: 4,21-lg 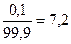
3.В точке эквивалентности.
Образуется соль, гидролиз которой обуславливает щелочную реакцию среды. Значит
рН=7+ 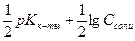
рН=7+ 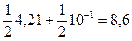
4.После точки эквивалентности концентрацию избытка рабочего раствора (щелочи) рассчитывают аналогично расчету точек при f>1 для титрования сильной кислоты сильным основанием, т.к. присутствие сильной щелочи подавляет гидролиз соли, что определяет величину рН в этом случае присутствующей в растворе свободной щелочью.
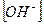 =
= 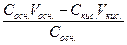 ; рОН=-lg10-4; рН=14-рОН
; рОН=-lg10-4; рН=14-рОН
100,1%: 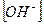 =
= 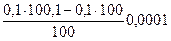
pOH=-lg10-4=4
pH=14-4=10
101%: 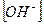 =
= 
рОН=-lg10-3=3
pH=14-3=11
110%: 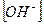 =
= 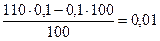
рОН=-lg10-2=2
pH=14-2=12
|
из
5.00
|
Обсуждение в статье: Расчет кривой титрования слабой кислоты сильным основание. |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

