 |
Главная |
Равновесные диаграммы потенциал- pH (диаграммы Пурбе или диаграммы электрохимического равновесия). Принципы построения. Использование диаграмм Пурбе
|
из
5.00
|
Одним из наиболее значительных достижений электрохимии 60-х годов является построение диаграмм pH-потенциал для всех важных металлов, названных в честь автора диаграммами Пурбе.
Диаграммы характеризуют, прежде всего, состав водного раствора и термодинамическую устойчивость твердой фазы (металла, оксидов, гидрооксидов и других соединений) в зависимости от двух переменных – электродного потенциала φ и pH. Каждая диаграмма построена в предположении, что все другие переменные заданы, но изменение состава водного раствора по еще одной переменной, например по концентрации иона металла, можно отобразить семейством линий. На полных диаграммах pH-потенциал наносят семейства линий при активностях ионов в растворе, равных 100, 10-2, 10-4, 10-6М. Эти линии обозначают соответственно числами 0, -2, -4 и -6. Для характеристики коррозионных процессов используют упрощенные диаграммы Ph=-потенциал. Для этого или объединяют кривые, соответствующие разным активностям ионов в водном растворе, проводя усредненную кривую, или строят диаграмму только при  =10-6М.
=10-6М.
Для расчета и построения диаграмм pH-потенциал необходимо располагать сведениями о химических и электрохимических реакциях, возможных в данной системе, об их количественных термодинамических характеристиках (энергиях Гиббса, стандартных электродных потенциалах, их температурных коэффициентах).
В области низких температур (0 – 100°С) энергию Гиббса реакции достаточно рассчитывать в приближении Улига:
 (1.3.1)
(1.3.1)
Величину стандартного электродного потенциала можно определить по уравнению
 (1.3.2)
(1.3.2)
В справочной литературе стандартные потенциалы отнесены к температуре 298К, их величины при других температурах могут быть найдены из уравнения (1.3.2) или по соответствующим изотермическим температурным коэффициентам. Первый изотермический коэффициент отражает изменение стандартной энтропии электродной реакции:
 (1.3.3)
(1.3.3)
а второй – изменение изобарных теплоемкостей
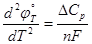 (1.3.4)
(1.3.4)
Если известны температурные коэффициенты, то стандартный потенциал любого электрода по температуре, отличной от 298К, можно рассчитать по уравнению
 (1.3.5)
(1.3.5)
Приближение Улига ( 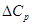 =0) соответствует уравнению (1.3.5) с учетом лишь первого температурного коэффициента.
=0) соответствует уравнению (1.3.5) с учетом лишь первого температурного коэффициента.
Линии на диаграммах pH-потенциал рассчитывают по равновесию, представленному в общем виде:
 (1.3.6)
(1.3.6)
для которого можно записать уравнение равновесного потенциала
 (1.3.7)
(1.3.7)
Где  - активности компонентов в конденсированных фазах. Если один из реагентов или продуктов реакции (1.3.6) находится в газовой фазе, то вместо термодинамической активности в уравнение (1.3.7) подставляется соответствующее парциальное давление (летучесть). Вводя общепринятое обозначение
- активности компонентов в конденсированных фазах. Если один из реагентов или продуктов реакции (1.3.6) находится в газовой фазе, то вместо термодинамической активности в уравнение (1.3.7) подставляется соответствующее парциальное давление (летучесть). Вводя общепринятое обозначение  ,получим
,получим
 (1.3.8)
(1.3.8)
Для того, чтобы по уравнению (1.3.8) построить линию на диаграмме pH-потенциал, из условий равновесия устанавливают значения 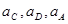 и
и  так, чтобы последний член имел определенную величину. Затем строят прямую линию с ординатой
так, чтобы последний член имел определенную величину. Затем строят прямую линию с ординатой 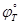 при pH=0 и наклоном
при pH=0 и наклоном  . При 298К значение
. При 298К значение 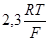 равно 0,0591 В, тогда наклон составит
равно 0,0591 В, тогда наклон составит  .
.
Наклонные линии (m≠0, n≠0) отображают равновесия, в которых участвуют ионы H+ или OH- совместно с электронами; горизонтальные линии (m=0, n≠0) – равновесия, в которых участвуют электроны, но не принимают участия ионы H+ и OH-; вертикальные линии (m≠0, n=0) – равновесия, в которых принимают участие ионы H+ и OH-, но не участвуют электроны. Последнее равновесие является химическим, поэтому не может быть рассчитано по формуле (1.3.7). Вместо него применяют
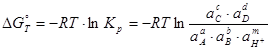 (1.3.9)
(1.3.9)
Затем определяют pH для вертикальной линии:
 (1.3.10)
(1.3.10)
М. Пурбе описал пять основных приложений равновесных диаграмм pH-потенциал чистых металлов:
1) теоретическое обоснование областей или условий коррозии (самопроизвольного растворения), иммунности (термодинамической устойчивости) и пассивации (условий, при которых термодинамически неустойчивые металлы практически не подвергаются растворению вследствие кинетических затруднений);
2) оценка стойкости металлов в воде;
3) установление металлов, которые находятся в активном или пассивном состоянии в определенной коррозионной среде;
4) оценка возможностей использования окисляющих ингибиторов коррозии (хроматов, молибдатов и т.д.);
5) классификация металлов по степени их благородности (термодинамической устойчивости) [3].
Вследствие диссоциации воды в водных растворах всегда присутствуют ионы водорода и гидроксила. Поэтому на всех электродах может протекать не только собственно электродная реакция, но и реакции, проходящие на водородном и кислородном электродах. Таким образом, теоретически в водных растворах электроды всегда рассматриваются как смешанные.
Диаграмма равновесия воды.
На простейшей, но, как указано выше, очень важной в практическом отношении диаграмме равновесия потенциалы электродных реакций, протекающих на водородном [εР(Н+/H2)] и кислородном [εР(О2/ОН-)] электродах, приведены в и зависимости от рН раствора. Эта диаграмма, кроме того, дает сведения об электрохимической устойчивости воды.
Потенциал реакции водородного электрода при 25°С можно представить в виде
 (1.3.11)
(1.3.11)
учитывая, что -lg 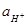 = pH. В этом уравнении
= pH. В этом уравнении  =
=  /
/  , где
, где 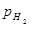 - давление газообразного водорода в системе, а
- давление газообразного водорода в системе, а  - давление газа, выбранное в качестве стандартной величины (1,01325·105 Па).
- давление газа, выбранное в качестве стандартной величины (1,01325·105 Па).
На кислородном электроде реализуется следующая реакция:
O2 + 2H2O + 4ē = 4OH- (1.3.12)
Потенциал электродной реакции равен
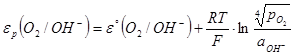 (1.3.13)
(1.3.13)
где 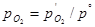 (
(  – давление газообразного кислорода в системе); εР (O2/OH-) – стандартный потенциал электродной реакции (1.3.12), равный 0,401 В при 25°С.
– давление газообразного кислорода в системе); εР (O2/OH-) – стандартный потенциал электродной реакции (1.3.12), равный 0,401 В при 25°С.
С учетом ионного произведения воды 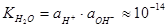 получаем выражение
получаем выражение
 (1.3.14)
(1.3.14)

Рис. 1.3.1 - Диаграмма равновесия воды
На рис. 1.3.1. величины  и
и  , рассчитанные по уравнениям (1.3.11) и (1.3.14), приведены как функции pH. Сплошные прямые отвечают
, рассчитанные по уравнениям (1.3.11) и (1.3.14), приведены как функции pH. Сплошные прямые отвечают  . При уменьшении pH на единицу потенциалы обоих электродов уменьшаются на 0,0591 В. Штриховые линии получают при уменьшении и увеличении давления водорода и кислорода на два порядка. В этом случае потенциал реакции водородного электрода (при постоянном pH) изменяется на 0,0591 В, а потенциал кислородного электрода – на 0,0295В. Следовательно, если построить график зависимости величин
. При уменьшении pH на единицу потенциалы обоих электродов уменьшаются на 0,0591 В. Штриховые линии получают при уменьшении и увеличении давления водорода и кислорода на два порядка. В этом случае потенциал реакции водородного электрода (при постоянном pH) изменяется на 0,0591 В, а потенциал кислородного электрода – на 0,0295В. Следовательно, если построить график зависимости величин  и
и  от pH, то получаются две параллельные прямые, причем их истинное расположение зависит от давления газа. В интервале между двумя прямыми вода устойчива, т.е. при обычных условиях на электродах, работающих при потенциалах в пределах указанного интервала, не происходит выделения водорода или кислорода (это «интервал устойчивости» воды). За пределами этого интервала (т.е. при электродных потенциалах более отрицательных, чем
от pH, то получаются две параллельные прямые, причем их истинное расположение зависит от давления газа. В интервале между двумя прямыми вода устойчива, т.е. при обычных условиях на электродах, работающих при потенциалах в пределах указанного интервала, не происходит выделения водорода или кислорода (это «интервал устойчивости» воды). За пределами этого интервала (т.е. при электродных потенциалах более отрицательных, чем  , и более положительных, чем
, и более положительных, чем  ) вода разлагается соответственно с выделением водорода и кислорода.
) вода разлагается соответственно с выделением водорода и кислорода.
Поэтому в водных растворах можно достаточно надежно изучать равновесие и электродную реакцию на простых электродах, если потенциал данной реакции находится в пределах интервала устойчивости воды, а электролит не содержит растворенных газов H2 и O2. Если потенциал электродной реакции находится за пределами интервала устойчивости воды, то нельзя достичь равновесия исследуемой реакции [4].
|
из
5.00
|
Обсуждение в статье: Равновесные диаграммы потенциал- pH (диаграммы Пурбе или диаграммы электрохимического равновесия). Принципы построения. Использование диаграмм Пурбе |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

