 |
Главная |
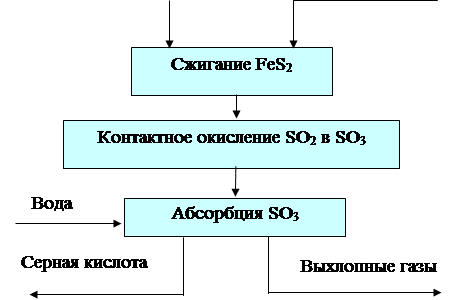
Блок-схема производства
|
из
5.00
|
 |
| ||||
 | |||||
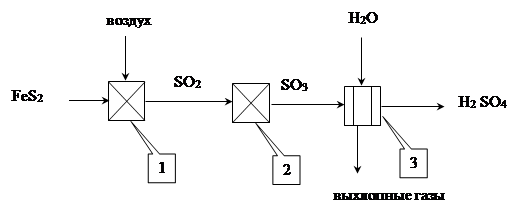 |
Операторная схема процесса
1 - печь, 2- контактный аппарат, 3- абсорбер
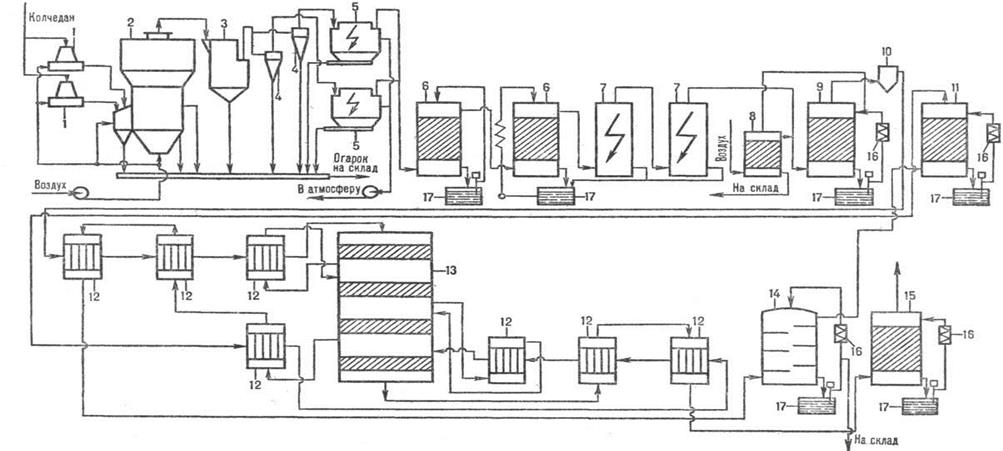
Рисунок 3.1.– Схема производства серной кислоты из колчедана
1 – тарельчатый питатель; 2 – печь; 3 – котел-утилизатор; 4 – циклоны; 5 – электрофильтры; 6 – промывные башни; 7 – мокрые электрофильтры; 8 – отдувочная башня; 9 – сушильнаябашня; 10 – брызгоуловитель; 11, 15 – моногидратные абсорберы; 12 – теплообменники; 13 – контактный аппарат; 14 – олеумный абсорбер; 16 – холодильники.
Расчет материального баланса
Расчет материального баланса является основным этапом. На основе материального баланса определяется целый ряд важнейших техноэкономических показателей: расход сырья и вспомогательных материалов для обеспечения заданной производительности; тепловой баланс и, соответственно, расход энергии, и теплообменную аппаратуру; экономический баланс производства, себестоимость продукции и, следовательно, рентабельность производства.
Исходные данные:
1. В печь поступает колчедан 40 т/сут.
2. Состав колчедана, % масс:
FeS2 – 70%;
песок (глина) –25%;
влага – 5%.
3. Содержание FeS2 в огарке – 2 %.
4. Коэффициент избытка воздуха α = 1,5. Состав воздуха кислород-21%об., азот-79%об..
Решение:
4FeS2 + 11O2→8SO2 +2Fe2O3
1. Рассчитаем, сколько пирита содержится в колчедане:
40 · 0,7 = 28 т/сут
2. Рассчитаем, сколько песка содержится в колчедане:
40 · 0,25 = 10 т/сут
3. Рассчитаем, сколько влаги содержится в колчедане:
40 · 0,05 = 2 т/сут
4. Молярная масса компонентов реакционной смеси : Mr(FeS2) = 120 кг/кмоль, Mr(O2) = 32 кг/кмоль, Mr(Fe2O3) = 160 кг/кмоль, Mr(SO2) = 64 кг/кмоль.
5. Рассчитаем, сколько диоксида серы по массе получится при обжиге 40 т колчедана, содержащего 28 т пирита:
(28 т/сут · 8 · 64 кг/кмоль) /(4 · 120 кг/кмоль) = 29,87 т/сут
6. Рассчитаем массу образовавшегося огарка:
(28 т/сут · 160 кг/кмоль · 2)/(4 · 120 кг/кмоль) = 18,67 т/сут.
7. Рассчитаем содержание FeS2 в огарке:
18,67 т/сут · 0,02 = 0,37 т/сут
8. Рассчитаем содержание Fe2O3:
18,67 т/сут – 0,37 т/сут = 18,3 т/сут
9. Рассчитаем массу кислорода, израсходованного на получение 29,87 т/сут SO2:
(29,87 т/сут · 11 · 32 кг/кмоль) /(8 · 64 кг/кмоль) = 20,54 т/сут
10. Рассчитаем массу кислорода с учетом коэффициента избытка воздуха
α =1,5:
20,54 т/сут · 1,5 = 30,81 т/сут
11. Рассчитаем объем кислорода:
(20,54 т/сут · 22,4 м3/кмоль) / 0,032 т/кмоль =14378 м3/сут
12. Рассчитаем объем кислорода с учетом коэффициента избытка воздуха
α =1,5:
14378 м3/сут · 1,5 = 21567 м3/сут
13. Рассчитаем объем воздуха, поступившего на окисление:
21567 м3/сут / 0,21 = 102700 м3/сут.
14. Рассчитаем массу воздуха, поступившего на окисление:
(102700 м3/сут · 0,02884 т/кмоль) / 22,4 м3/кмоль = 132,23 т/сут.
15. Рассчитаем массу отработанного воздуха:
(132,23 т/сут – 30,81 т/сут) + (30,81 т/сут – 20,54 т/сут) = 111,7 т/сут.
16. Рассчитаем массу вышедшего кислорода:
30,81 т/сут. – 20,54 т/сут. = 10,27 т/сут.
Таблица 3.1 – Материальный баланс процесса окисления пирита (FeS2) кислородом воздуха
| Приход | |||||
| Исходное вещество | кг/ч | т/сут. | т/мес. | т/год | %масс |
| Колчедан, в т.ч.: | 1666,7 | 40,0 | 1200,0 | 14400 | 23,22 |
| - пирит | 1166,7 | 28,0 | 840,0 | 10080,0 | |
| - влага | 83,3 | 2,0 | 60,0 | 720,0 | |
| - песок (глина) | 416,7 | 10,0 | 300,0 | 3600,0 | |
| Воздух, в т.ч.: | 5509,6 | 132,23 | 3966,9 | 47602,8 | 76,78 |
| - О2 | 1283,8 | 30,81 | 924,3 | 11091,6 | |
| - N2 | 4225,8 | 101,42 | 3042,6 | 36511,2 | |
| Всего | 7176,3 | 172,23 | 5166,9 | 62002,8 | 100 |
| Расход | |||||
| продукт | кг/ч | т/сут | т/мес. | т/год | %масс |
| SO2 | 1244,6 | 29,87 | 896,1 | 10753,2 | 17,34 |
| Пиритный огарок, в т.ч.: | 1277,9 | 30,67 | 920,1 | 11041,2 | 17,81 |
| - Fe2O3 | 762,5 | 18,3 | 549 | 6588 | |
| - пирит | 15,4 | 0,37 | 11,1 | 133,2 | |
| - песок (глина) | 416,7 | 10,0 | 300,0 | 3600,0 | |
| - влага | 83,3 | 2,0 | 60,0 | 720,0 | |
| Отработанный воздух, в т.ч.: | 4653,75 | 111,69 | 3350,7 | 40208,4 | 64,85 |
| - О2 | 427,9 | 10,27 | 308,1 | 3697,2 | |
| - N2 | 4226,3 | 101,42 | 3042,9 | 36514,8 | |
| Всего | 7176,3 | 172,23 | 5166,9 | 62002,8 | 100 |
Рассчитано, что для получения 1т сернистого ангидрида нужно затратить 1,3391 т. сырья; при использовании 1т сырья выход диоксида серы составляет 0,7467 т.
|
из
5.00
|
Обсуждение в статье: Блок-схема производства |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

