 |
Главная |
II. Решение задач по методу Вант – Гоффа
Метод Вант - Гоффа . Этот метод основан на изучении зависимости скорости реакции от концентрации одного из реагентов.
r = k*СА nA
Логарифмируя это выражение, получим
ln r = ln k + nAln CA (4)
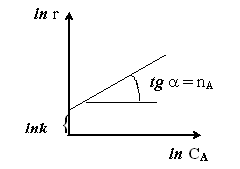
Чтобы найти кинетические параметры уравнения скорости реакции по данному уравнению (4) необходимо определить скорость реакции для нескольких кинетических кривых при различных концентрациях реагента и построить график прямой линия в координатах ln r = f(lnCA ). Тангенс угла наклона этой прямой равен порядку реакции по реагенту, а отрезок, отсекаемый этой прямой на оси ординат при ln CA = 0, равен ln k.
1. Метод Вант-Гоффа можно применять аналитически, рассчитывая порядок реакции по формуле: 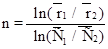 (5)
(5)
Пример 3. Вычислите порядок реакции пиролиза А при 10оС из следующих данных:
А0*102 , моль/л 2,0 0,51
r*104 , моль/ л,час 6,4 1,63
Решение: n = ln(r’/r”)/ln(Co’/Co”) = ln(6,4/1,63)/ln(2,0/0,51) = 1,02
Константа скорости : Для n = 1 r = k* CA , отсюда k = r/CA = 6,4*10-4/2,0*10-2 = 3,2*10-2 л/ моль*ч.
2. При наличии нескольких исходных реагентов порядки реакции по каждому из них можно определить при условии изменения скорости от концентрации одного реагента при постоянстве концентраций других реагентов.
Пример 4. В реакции А + В à Пр получены следующие начальные скорости при различных начальных концентрациях реагентов :
| [А]0, моль/л | 1,0 | 0,1 | 1,0 |
| [В]0, моль/л | 1,0 | 1,0 | 0,0086 |
| r0, моль/(л ,с) | 0,025 | 0,0025 | 0,00025 |
Напишите кинетическое уравнение реакции? Определите константу скорости.
Решение: Запишем выражение скорости с неизвестными порядками по реагентам:
r = k*CAnACBnB
Сначала выберем 1 и 3 колонки при постоянной концентрации [А]0 :
r = k”CBnB , где k”= k*CAnA тогда порядок по В можно определить как:
nВ = ln(r’/r”)/ln(Co’/Co”) = ln(0,025/0,00025)/ln(1/0,025) = 0,96 » 1
Аналогично. Выберем 1 и 2 колонки при постоянной концентрации [В]0 :
r = k”” CAnA , где k”’= k* CBnB тогда порядок по A можно определить как:
nA = ln(r’/r”)/ln(Co’/Co”) = ln(0,025/0,0025)/ln(1/0,1) = 1
Окончательно: nВ =1 и nA = 1 и r = k*CA1CB1
Проверка: r = k*CA1CB1 и k = r /CA1CB1
Получим значения k для трех колонок: k1 = 0,025; k2= 0,025 ; k3= 0,030 л/моль*c.
3. Метод Вант – Гоффа можно применить и при наличии только одной кинетической кривой. Для этого определим скорость реакции по касательным проведенным через точки с различным значением времени. Такая процедура достаточно трудоемкая и мало применяется.
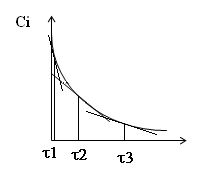
Рис. 2. Определение порядка реакции методом Вант-Гоффа.
Наиболее часто, когда не известен порядок реакции пользуются средними скоростями реакции ~ Dci/Dt вместо истинных скоростей ~ dci/dt. Определённая таким образом скорость, называется средней скоростью реакции.
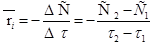 - средняя скорость (6)
- средняя скорость (6)
при 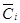 =
= 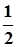 (С1 + С2 ) - средняя концентрация (7)
(С1 + С2 ) - средняя концентрация (7)
Пример 5. Нитрование толуола (т) в избытке азотной кислотой идёт как реакция псевдопервого порядка. Концентрация п-нитротолуола изменялась следующим образом:
| t, мин, | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| Ст,104,моль/л | 3,0 | 2,837 | 2,684 | 2,538 | 2,401 | 2,271 | 2,148 | 2,031 | 1,921 |
Методом Вант – Гоффа подтвердите первый порядок реакции и определите константу скорости реакции и время полупревращения,
Рассчитываем несколько значений средних скоростей и средних концентраций:
t =0 и t = 10 ; r1 =-(2,837-3,0)/(10-0)=0,0163 моль/л*мин; с1=(2,837+3,0)/2= 2,919 моль/л
t=10 и t=20; r2=-(2,684-2,837)/(20-10)=0,0153моль/л*мин;
с2=(2,837+2,684)/2 = 2,761 моль/л и т.д. для других пар точек.
n = ln(r’/r”)/ln(Co’/Co”) = ln(0,0163/0,0153)/ln(2,919/2,761) = 1,14 »1

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

