 |
Главная |
Общий механизм реакций электрофильного присоединения
|
из
5.00
|
 Любой полярный реагент в принципе может быть представлен как результат взаимодействия электрофила E+ и нуклеофила Nu-:
Любой полярный реагент в принципе может быть представлен как результат взаимодействия электрофила E+ и нуклеофила Nu-:
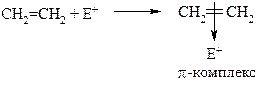 На первой стадии реакции электрофил подходит к электронному облаку π-связи и они притягиваются друг к другу. Образуется так называемый π-комплекс:
На первой стадии реакции электрофил подходит к электронному облаку π-связи и они притягиваются друг к другу. Образуется так называемый π-комплекс:
Затем электрофил образует новую σ-связь с одним из атомов углерода. Для этого он использует оба электрона бывшей π-связи. Образуется так называемый σ-комплекс, или карбкатион:
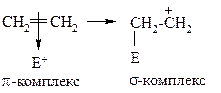 |
Так как электрофил использовал на образование новой связи электроны π-связи, соседний углерод приобретает полный положительный заряд.
 σ-Комплекс затем реагирует с оставшимся нуклеофилом, который предоставляет свои электроны для образования новой связи:
σ-Комплекс затем реагирует с оставшимся нуклеофилом, который предоставляет свои электроны для образования новой связи:
Стадия образования карбкатиона является самой медленной (старая π-связь должна разорваться, это требует затрат энергии). Скорость этой стадии определяет скорость реакции в целом. Её называют лимитирующей стадией реакции.
Теперь рассмотрим конкретные примеры реакций электрофильного присоединения.
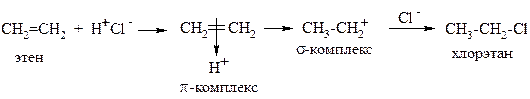 Реакция гидрогалогенирования (гидрохлорирования, гидробромирования).Эта реакция протекает полностью в соответствии с общим механизмом AE:
Реакция гидрогалогенирования (гидрохлорирования, гидробромирования).Эта реакция протекает полностью в соответствии с общим механизмом AE:
В результате реакции образуются галогеналканы.
Реакция гидратации– присоединение воды. Эта реакция возможна только в присутствии сильных минеральных кислот (серной или фосфорной). Чтобы объяснить роль кислоты, необходимо рассмотреть механизм этой реакции.
Молекула воды – плохой источник электрофильных частиц (H+), т.к. степень её диссоциации очень низкая. Фактически роль электрофилов в реакции гидратации играют протоны, полученные не от молекул воды, а от молекул минеральной кислоты. Именно они и начинают реакцию.
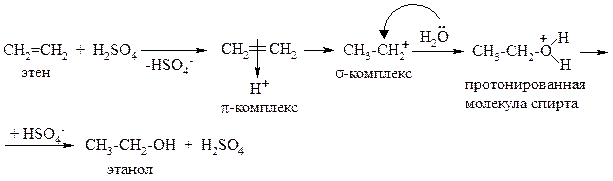 |
На первой стадии реакции протон кислоты образует π-комплекс с электронным облаком π-связи. Затем протон водорода присоединяется к одному из атомов углерода, при этом на соседнем атоме углерода возникает полный положительный заряд. Образуется σ-комплекс (карбкатион). Вы видите, что эти две стадии протекают в соответствии с общим механизмом реакций AE. А вот над следующей стадией этой реакции надо подумать: σ-комплекс должен прореагировать с нуклеофилом (см. общий механизм), а в реакционной среде есть два вида нуклеофилов – анионы кислоты HSO4- и нейтральные молекулы воды с неподелённой электронной парой на кислороде. В общем, анионы – более сильные нуклеофилы, но в этой реакции кислота используется в каталитических количествах (анионов мало), в то время как воду используют в избытке. Вот почему в этом «соревновании нуклеофилов» побеждают молекулы воды.
Итак, на следующей стадии реакции молекула воды как нуклеофил атакует карбкатион, и по донорно-акцепторному механизму образуется новая σ-связь. Так как атом кислорода затратил на образование новой связи два своих электрона (как донор), на нём образовался полный положительный заряд. Получилась протонированная молекула спирта – нестабильная заряженная частица. Для стабилизации ей необходимо отщепить протон, что и делает анион серной кислоты. В результате этой реакции образовались молекулы спирта и серной кислоты. То, что серная кислота в результате реакции не расходуется, подтверждает, что она является катализатором этой реакции. Итак, роль серной кислоты в реакции гидратации алкенов – это роль катализатора, источника электрофильных частиц (H+).
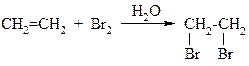 Реакция галогенирования (хлорирования, бромирования).Алкены в обычных условиях легко присоединяют галогены, например, в реакции бромирования этена образуется 1,2-дибромэтан:
Реакция галогенирования (хлорирования, бромирования).Алкены в обычных условиях легко присоединяют галогены, например, в реакции бромирования этена образуется 1,2-дибромэтан:
Эта реакция протекает с водным раствором брома, так называемой бромной водой. Под действием полярных молекул воды неполярная связь в молекуле брома поляризуется:
 |
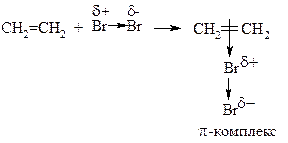 Затем эта поляризованная молекула брома взаимодействует с π-электронным облаком этена, образуя π-комплекс:
Затем эта поляризованная молекула брома взаимодействует с π-электронным облаком этена, образуя π-комплекс:
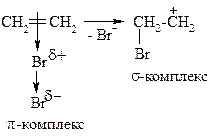 Под действием электронов π-облака происходит ещё большая поляризация связи Br-Br, она разрывается гетеролитически, и Br+ участвует в образовании σ-комплекса:
Под действием электронов π-облака происходит ещё большая поляризация связи Br-Br, она разрывается гетеролитически, и Br+ участвует в образовании σ-комплекса:
У положительно заряженного атома углерода σ-комплекса есть вакантная p-орбиталь, а у атома брома – неподелённая электронная пара. Они взаимодействуют по донорно-акцепторному механизму, образуется циклический катион бромония:
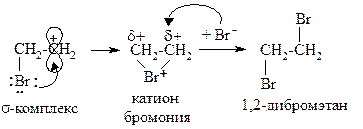 |
Катион бромония подвергается атаке нуклеофила (Br-), и образуется 1,2-дибромэтан. Поскольку подход Br- со стороны первого брома затруднён стерически, его атака происходит с противоположной стороны (так называемое транс-присоединение).
В случае образования 1,2-дибромэтана это не столь важно, т.к. конформеры свободно переходят друг в друга, но при присоединении к циклоалкенам нужно обращать внимание именно на транс-присоединение, например, при бромировании циклопентена образуется транс-1,2-дибромциклопентан:
 |
Реакцию бромирования используют как качественную реакцию на непредельность (на двойную и тройную связь). Качественными называют реакции, результат которых хорошо виден, например, выпадение или растворение осадка, изменение окраски, выделение пузырьков газа, появление характерного запаха. В реакции бромирования алкенов можно наблюдать обесцвечивание бромной воды (исчезновение оранжевой или жёлто-оранжевой окраски).
Реакции электрофильного присоединения
к несимметричным алкенам
Когда мы рассматривали реакцию гидрогалогенирования или гидратации на примере этена, у нас не возникало вопроса к какому из атомов углерода при двойной связи присоединится протон водорода на стадии образования σ-комплекса: в молекуле этена (и других симметричных алкенов) оба углерода при двойной связи равноценны. В случае же этих реакций в несимметричных алкенах возможно образование двух продуктов присоединения, а значит, возникает проблема: какой из них будет преобладающим. Рассмотрим это на примере гидрохлорирования пропена:
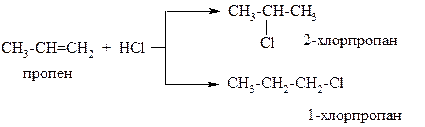 |
Теоретически, в реакции гидрохлорирования пропена могут образоваться 1-хлорпропан и 2-хлорпропан, однако на практике в основном получается 2-хлорпропан. Эта реакция протекает по правилу Марковникова: при присоединении реагентов типа H+X- (например, HCl, HBr, HOH) к несимметричным алкенам протон водорода присоединяется к более гидрогенизированному атому углерода при двойной связи.
Чтобы объяснить такой порядок присоединения, необходимо рассмотреть статический и динамический факторы.
Статический фактор – это распределение электронной плотности в нереагирующей молекуле.
 Атом углерода при двойной связи sp2-гибридизован, он более электроотрицателен, чем sp3-гибридизованный углерод метильной группы. Поэтому электронная плотность связи CH3-CH= смещена к углероду с двойной связью. Так как π-связь поляризуется легче, чем σ-связь, электроны π-связи смещаются к соседнему атому углерода, т.е. происходит её поляризация. В конечном итоге на первом атоме углерода возникает частичный отрицательный заряд (δ-), а на втором – частичный положительный (δ+). Конечно же, протон водорода (положительно заряженная частица) будет направляться к тому углероду, где есть избыток электронной плотности, а он и есть более гидрогенизированный атом углерода при двойной связи.
Атом углерода при двойной связи sp2-гибридизован, он более электроотрицателен, чем sp3-гибридизованный углерод метильной группы. Поэтому электронная плотность связи CH3-CH= смещена к углероду с двойной связью. Так как π-связь поляризуется легче, чем σ-связь, электроны π-связи смещаются к соседнему атому углерода, т.е. происходит её поляризация. В конечном итоге на первом атоме углерода возникает частичный отрицательный заряд (δ-), а на втором – частичный положительный (δ+). Конечно же, протон водорода (положительно заряженная частица) будет направляться к тому углероду, где есть избыток электронной плотности, а он и есть более гидрогенизированный атом углерода при двойной связи.
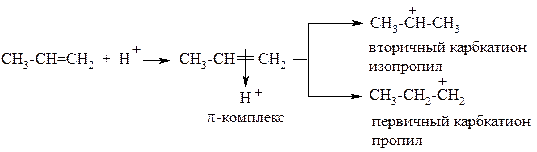 Теперь рассмотрим динамический фактор – сравним стабильность промежуточных частиц (карбкатионов). Вы уже знаете: чем стабильнее промежуточная частица (интермедиат), тем больше вероятность её образования.
Теперь рассмотрим динамический фактор – сравним стабильность промежуточных частиц (карбкатионов). Вы уже знаете: чем стабильнее промежуточная частица (интермедиат), тем больше вероятность её образования.
На стадии образования σ-комплекса теоретически могут образоваться два карбкатиона – пропил (первичный) и изопропил (вторичный). Атом углерода с полным положительным зарядом смещает к себе электронную плотность соседней (или соседних) C-C σ-связи, уменьшая собственный недостаток электронной плотности. Вторичный карбкатион более стабилен из-за большей компенсации положительного заряда на углероде:
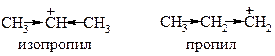 |
Если рассуждать о стабильности карбкатионов вообще, то самыми стабильными являются третичные, затем – вторичные, первичные, а самым нестабильным – катион метил:
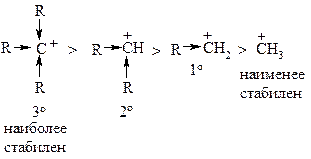 |
 Так как в рассматриваемом примере более стабильным является изопропил-катион, именно он в первую очередь сможет провзаимодействовать с анионом хлора, а значит преобладающим продуктом этой реакции является 2-хлорпропан (т.е. протон водорода присоединился к более гидрогенизированному атому углерода):
Так как в рассматриваемом примере более стабильным является изопропил-катион, именно он в первую очередь сможет провзаимодействовать с анионом хлора, а значит преобладающим продуктом этой реакции является 2-хлорпропан (т.е. протон водорода присоединился к более гидрогенизированному атому углерода):
Классическое правило Марковникова можно без оговорок применять только к самим алкенам. В случае их производных нужно обязательно рассматривать статический и динамический факторы, влияющие на ход реакции (например, позже мы будем рассматривать реакции электрофильного присоединения в акриловой кислоте, которые протекают против правила Марковникова).
В современной интерпретации правило Марковникова формулируется так: направление присоединения реагентов типа HX к производным алкенов определяется относительной устойчивостью промежуточных карбкатионов.
Реакция гидрирования алкенов протекает по механизму радикального присоединения в присутствии катализаторов (никель, платина), на поверхности которых происходит гомолитический разрыв молекулы водорода. В результате гидрирования алкенов образуются алканы:
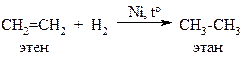 |
Реакции окисления алкенов протекают с образованием различных продуктов в зависимости от условий. Мы рассмотрим только так называемое мягкое окисление алкенов. Его проводят разбавленным раствором перманганата калия при комнатной температуре (реакция Вагнера).
В результате реакции образуются гликоль (двухатомный спирт) и диоксид марганца:
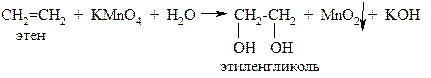 |
Эту реакцию используют как качественную на наличие двойной связи: в результате исчезает малиновое окрашивание перманганата калия и появляется бурый осадок диоксида марганца.
|
из
5.00
|
Обсуждение в статье: Общий механизм реакций электрофильного присоединения |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

