 |
Главная |
РАСКИСЛЕНИЕ МЕТАЛЛИЧЕСКИХ РАСПЛАВОВ
|
из
5.00
|
Под раскислением понимают комплекс операций по снижению содержания кислорода в жидкой стали.
Основными задачами раскисления являются:
– снижение содержания кислорода в жидком железе присадками элементов с большим сродством к кислороду, чем у железа, до уровня, обеспечивающего получение плотного металла;
– создание условий для более полного удаления из жидкой стали продуктов раскисления.
Если первая задача рассматривается с использованием законов химической термодинамики, то вторая решается при помощи аппарата химической кинетики.
Термодинамический подход позволяет выявить связь между содержанием кислорода в жидкой стали и содержанием элемента-раскислителя R, определить степень влияния температуры на характер этой связи, а также рассчитать минимальное содержание кислорода в металлическом расплаве при раскислении его элементом R.
Рассмотрим случай, когда при раскислении металлического расплава каким-либо элементом Rпроисходит образование твердой конденсированной фазы  в соответствии с реакцией вида [4]
в соответствии с реакцией вида [4]
 . (46)
. (46)
При условии  =1 константа равновесия данной реакции примет вид
=1 константа равновесия данной реакции примет вид
 , (47)
, (47)
где 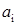 – активность
– активность 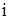 -го компонента в расплаве.
-го компонента в расплаве.
Для расчета активностей компонентов расплава за стандартное состояние целесообразно принять 1%-ный разбавленный раствор.
Значение константы равновесия KRможно определить по изменению свободной энергии реакции (46):
 . (48)
. (48)
Значение  , в свою очередь, определяется из анализа реакции образования оксида
, в свою очередь, определяется из анализа реакции образования оксида  из чистого компонента R икислорода при
из чистого компонента R икислорода при 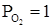 атм, а также реакций растворения в металле кислорода и элемента R:
атм, а также реакций растворения в металле кислорода и элемента R:
 ;
;
 ;
;
 ;
;
 ;
;
 . (49)
. (49)
С учетом уравнения (49) в выражении (48) константу равновесия можно записать как функцию температуры:
 ,
,
где А и В – постоянные для данной химической реакции.
Чтобы рассчитать равновесные концентрации кислорода и элемента R, в уравнении (46) активности компонентов выражают через их концентрации и коэффициенты активности:
 . (50)
. (50)
Коэффициенты активности fR и fO можно оценить при помощи параметров взаимодействия первого порядка с учетом принятого стандартного состояния:
 ; (51)
; (51)
 ; (52)
; (52)
Прологарифмировав уравнение (50) и выразив концентрацию кислорода через остальные члены суммы, определим раскислительную способность элемента R по равновесной концентрации кислорода:
 . (53)
. (53)
Чтобы рассчитать минимальную концентрацию кислорода в металлическом расплаве, раскисляемом элементом R, необходимо продифференцировать уравнение (53) по концентрации этого элемента и приравнять к нулю:
 . (54)
. (54)
Приравнивая правую часть уравнения (54) к нулю и решая его относительно R, находим концентрацию раскислителя R, соответствующую минимальному содержанию кислорода в металле; при этом значение коэффициентов активности компонентов находим по соотношениям (51) и (52):
 ; (55)
; (55)
 . (56)
. (56)
Подставляя значение [R] из соотношения (56) в уравнение (53), определяем минимальную концентрацию кислорода в металлическом расплаве, раскисляемом элементом R:
 . (57)
. (57)
Задание
Рассчитать равновесную концентрацию кислорода в жидком железе (никеле) при раскислении его элементом R в присутствии хрома при температуре 1600 °С.
Построить и проанализировать зависимости  и
и  .
.
Определить минимальное содержание кислорода в металле. Необходимые данные взять в табл. 18–20 (в железе  , в никеле
, в никеле 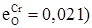 .
.
Таблица 18
| № | R | % (пределы изменения) | Значение 
| 
| |||||
| в железе | в никеле | ||||||||

| 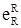
| 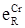
| 
| 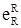
| 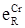
| ||||
| Mn | 0,5–3,5 | –0,021 | –0,35 | 0,01 | 1; 3; 5 |
При взаимодействий марганца с растворенным в железе кислородом происходит образование твердого оксида в соответствии с реакцией вида
 ; (58)
; (58)
при этом  и константа равновесия выражается уравнением
и константа равновесия выражается уравнением
 . (59)
. (59)
Константа равновесия данной реакции связана с изменением свободной энергии образования оксида известным соотношением
 . (60)
. (60)
Значение  можно определить из анализа реакции образования оксида
можно определить из анализа реакции образования оксида  из чистого
из чистого 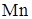 и кислорода при
и кислорода при 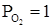 атм, при этом будем учитывать реакцию растворения в железе кислорода и марганца:
атм, при этом будем учитывать реакцию растворения в железе кислорода и марганца:
 ; (61)
; (61)
 ; (62)
; (62)
 . (63)
. (63)
Комбинируя реакции (61) – (63) (вычитая из первой две оставшиеся), получаем исходную реакцию (58). Соответственно для нее изменение свободной энергии будет иметь значение
 = –95 400 + 19,70Т – 1320 + 9,35Т + 28 000+ 0,69Т = –68720 + 29,74Т. (64)
= –95 400 + 19,70Т – 1320 + 9,35Т + 28 000+ 0,69Т = –68720 + 29,74Т. (64)
В соответствии с уравнением (60) константа равновесия будет иметь вид
 . (65)
. (65)
Активности компонентов  ] и
] и  выразим через их концентрации (в %) и коэффициенты активности:
выразим через их концентрации (в %) и коэффициенты активности:
 . (66)
. (66)
Коэффициенты активности рассчитаем с помощью параметров, взаимодействия:
 . (67)
. (67)
В растворах Fe–Mn–O концентрация кислорода мала, поэтому в соотношениях (67) произведениями  и
и  можно пренебречь. Кроме того, параметр взаимодействия
можно пренебречь. Кроме того, параметр взаимодействия  . Следовательно,
. Следовательно,  , а
, а  .
.
С учетом этого, константа равновесия реакции раскисления марганца будет иметь вид
 . (68)
. (68)
откуда можно выразить равновесную концентрацию кислорода:
 . (69)
. (69)
Значение  определим из (21):
определим из (21):
при Т=1873 К  .
.
При содержании марганца  , соответственно
, соответственно 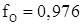 .
.
Подставляя полученные значения  и
и  в формулу (69), определяем равновесную концентрацию кислорода при содержании марганца 0,5%:
в формулу (69), определяем равновесную концентрацию кислорода при содержании марганца 0,5%:
 .
.
Активность кислорода будет 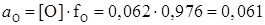 .
.
Аналогичным образом рассчитываем содержание кислорода в железе при содержании марганца от 0,4 до 1,2%, результаты расчета приведены в табл. 17.
Таблица 17
 % %
|  % %
| 
| 
|
| 0,5 | 0,062 | 0,976 | 0,061 |
| 0,032 | 0,953 | 0,030 | |
| 1,5 | 0,022 | 0,930 | 0,020 |
| 0,017 | 0,908 | 0,015 | |
| 2,5 | 0,014 | 0,886 | 0,012 |
| 0,012 | 0,865 | 0,010 | |
Как видно из представленных данных, по мере увеличения концентрации марганца в железе равновесное содержание кислорода снижается. Уменьшается с ростом содержания марганца и активность кислорода.
Для определения минимальной концентрации кислорода в железе, раскисляемом марганцем, необходимо прологарифмировать соотношение (69),а затем продифференцировать полученное уравнение по концентрации марганца и найти экстремум функции, приравняв ее к нулю. В результате определим концентрацию марганца, соответствующую минимальному содержанию кислорода:
 .
.
Значение  определим по соотношению (55),предварительно рассчитав
определим по соотношению (55),предварительно рассчитав  :
:
 .
.
Зависимость 

Зависимость 

|
из
5.00
|
Обсуждение в статье: РАСКИСЛЕНИЕ МЕТАЛЛИЧЕСКИХ РАСПЛАВОВ |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

