 |
Главная |
Диазо- и азосоединения. Реакции солей диазония без выделения азота. Азосочетание. Получение азосоединений. Азокрасители
|
из
5.00
|
Реакции ароматических солей диазония без выделения азота
Востановление солей арендиазония до арилгидразинов.
Реакция азосочетания.
Азосочетание.
АЗОСОЧЕТАНИЕ,
Азосочетание включает две стадии-присоединение катиона диазония к азосоставляющей и отщепление протона, напр.:
Медленной (лимитирующей) стадией часто является первая.
К т. наз. окислительному азосочетанию относят взаимод. ароматич. гидразинов или гидразонов с азосоставляющими в присут. окислителей. Эта р-ция используется гл. обр. при получении азосоединений на основе гетероароматич. компонентов, напр.:
Билет № 26 Альдегиды и кетоны. Номенклатура. Реакции нуклеофильного присоединения, механизм. Влияние радикала на реакционную способность карбонильной группы. Присоединение спиртов, гидросульфита натрия, циановодорода, металлорганических соединений.
Альдегиды и кетоны кислородсодержащие органические соединения, содержа-щие карбонильную группу (-С=О).
Общая формула карбонильных соединений:
В альдегидах Х = Н (исключением является формальдегид (R = Х = H); в кетонах Х = R, R' – алкильные радикалы (СН3-. С2Н5-)
Для альдегидов используется тривиальная, рациональная номенклатура и номенклатура ИЮПАК (систематическая).
Тривиальные названия альдегидов производят от тривиальных названий тех кислот, в которые альдегиды превращаются при окислении.
Реакции нуклеофильного присоединения альдегидов и кетонов.
Альдегиды и кетоны легко присоединяют нуклеофильные реагенты по С=О связи:
Электронодонорные и объемистые заместители затрудняют реакцию, электроноакцепторные заместители повышают реакционную способность карбонильного соединения. Поэтому альдегиды в AdN–реакциях активнее, чем кетоны.
Активность карбонильных соединений повышается в присутствии кислотных катализаторов, которые увеличивают положительный заряд на карбонильном атоме углерода:
Присоединение воды.
Присоединение спиртов и тиолов.
Альдегиды присоединяют спирты с образованием полуацеталей. При избытке спирта и в присутствии кислотного катализатора реакция идет дальше – до образования ацеталей
Реакция образования полуацеталя протекает как нуклеофильное присоединение и ускоряется в присутствии кислот или оснований.
Процесс образования ацеталя идет как нуклеофильное замещение ОН группы в полуацетале и возможен только в условиях кислотного катализа, когда группа ОН превращается в хорошую уходящую группу (H2O)
Присоединение гидросульфита натрия.
Альдегиды и метилкетоны присоединяют гидросульфит натрия NaHSO3 c образованием бисульфитных производных.
Бисульфитные производные карбонильных соединений – кристаллические вещества, не растворимые в избытке раствора бисульфита натрия. Реакция используется выделения карбонильных соединений из смесей. Карбонильное соединение может быть легко регенерировано обработкой бисульфитного производного кислотой или щелочью.
Взаимодействие с соединениями общей формулы NH2X.
.
Полимеризация альдегидов. Реакции присоединения – отщепления: образование иминов (оснований Шиффа), оксимов, гидразонов, арилгидразонов, семикарбазонов. Взаимодействие альдегидов с аммиаком (гексаметилентетрамин).
образуются амины. Процесс используется для синтеза аминов из альдегидов и кетонов и называется восстановительным аминированием. С карбонильными соединениями семикарбазид образует продукты конденсации по гидразинной аминогруппе — семикарбазоны. Реакция идет через промежуточное образование α-аминоспирта: 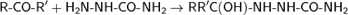
Взаимодействие с соединениями общей формулы NH2X.
Реакции протекают по общей схеме как процесс присоединения-отщепления. Образующийся на первой стадии продукт присоединения не устойчив и легко отщепляет воду.
По приведенной схеме с карбонильными соединениями реагируют аммиак, первичные амины, гидразин, замещенные гидразины, гидроксиламин.
Образующиеся производные представляют собой кристаллические вещества, которые используют для выделения и идентификации карбонильных соединений.
Имины (основания Шиффа) являются промежуточными продуктами во многих ферментативных процессах (трансаминирование под действием кофермента пиридоксальфосфата; восстановительное аминирование кетокислот при участии кофермента НАД Н). При каталитическом гидрировании иминов
31. Сложные эфиры. Реакция этерификации. Кислотный и щелочной гидролиз сложных эфиров. Переэтерификация. Аммонолиз сложных эфиров.
Сложными эфирами называются функциональные производные карбоновых кислот обшей формулы RC(O)OR’,в которых гидроксильная группа, входящая в состав карбоксильной группы, замещена на остаток спирта или фенола —OR. Обычно сложные эфиры называют по исходным кислоте и спирту или фенолу. По заместительной номенклатуре IUPAC их названия образуют из названия углеводородного радикала спирта или фенола и систематического названия карбоновой кислоты, в котором суффикс -овая кислота заменяется суффиксом -оат:
Сложные эфиры низших спиртов и карбоновых кислот представляют собой летучие жидкости, с приятным запахом, плохо растворимые в воде и хорошо — в большинстве органических растворителей.
Реакция этерификации.
Механизм.
|
из
5.00
|
Обсуждение в статье: Диазо- и азосоединения. Реакции солей диазония без выделения азота. Азосочетание. Получение азосоединений. Азокрасители |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

