 |
Главная |
Фракционная перегонка и перегонка с дефлегматором
|
из
5.00
|
Возможности разделения веществ с помощью простой перегонки весьма ограничены. Фактически она позволяет отделить летучие соединения от нелетучих, например, диэтиловый эфир (Ткип = 36 °С) отогнать от анилина (Ткип = 184 °C). Если температуры кипения неограниченно смешивающихся жидкостей различаются менее, чем на 50° С, дистиллат – продукт перегонки – обязательно содержит компонент с высокой температурой кипения (даже если это первые капли дистиллата), а остаток в перегонной колбе (кубовый остаток) – компонент с низкой температурой кипения. Правда его содержание будет значительно меньше, чем в исходной смеси. Поэтому если перегонку повторить несколько раз, можно получить достаточно чистые вещества.
Практически при дробной перегонке поступают следующим образом. Смесь перегоняют, собирая три фракции, обычно в заранее выбранных температурных интервалах. Например, если перегоняется смесь метилового спирта (Ткип = 64 °С) и воды, температурный интервал, в котором может кипеть такая смесь, равен 100 – 64 = 36 °С. Этот интервал делят на три части. Первую фракцию собирают в пределах 64 – 76 °С, вторую – 76 – 88 °С и третью – 88 – 100 °С. Первая фракция содержит преимущественно (но не исключительно) метиловый спирт, а последняя – преимущественно воду. Чем больше разнятся температуры кипения компонентов, тем больше объемы первой и последней фракций и тем меньше объем промежуточной.
Далее вновь перегоняют первую фракцию. После того, как температура повторной перегонки поднимется до 76 °С, к кубовому остатку прибавляют вторую фракцию первой перегонки. Может это покажется странным, хотя удивительного здесь ничего нет, но полученная смесь закипает при температуре ниже 76 °С. Поэтому приемник дистиллата меняют только тогда, когда температура вновь не достигнет 76 °С. Затем собирают фракцию с температурой кипения до 88 °С и к кубовому остатку прибавляют третью фракцию, полученную при первой перегонке. Вновь жидкость закипает при температуре несколько ниже 88 °С, поэтому приемник пока остается прежним. Третью фракцию собирают, как и первый раз в интервале температур 88 – 100 °С. Если промежуточная фракция в результате повторной перегонки остается большой по объему, ректификацию повторяют еще и еще раз. В конечном счете путем больших затрат времени и труда с помощью фракционной перегонки можно получить практически чистые вещества, даже если они очень близки по температурам кипения. К счастью, существует более приемлемый вариант разделения смесей компонентов с близкими температурами кипения – ректификация.
Самым простым вариантом ректификации является перегонка с дефлегматором (рис. 8).
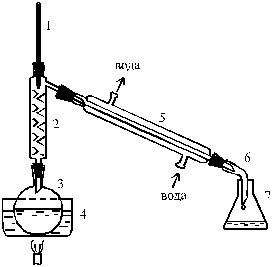
Рис. 8. Схема установки для перегонки с дефлегматором: 1 – термометр, 2 – дефлегматор, 3 – перегонная колба, 4 – водяная баня , 5 – прямой холодильник, 6 – алонж, 7 – приемная колба
Дефлегматор (2) – это стеклянная трубка, внутренняя поверхность которой сплошь покрыта выступами для увеличения площади контакта паров жидкости, поднимающихся из колбы (3), с конденсатом, стекающим обратно. (Конденсат в данном случае называется флегмой, откуда и название “дефлегматор”). В дефлегматоре горячие пары (предпочтительно компонент с высокой температурой кипения) конденсируются в более холодной жидкости. При этом выделяется теплота, которая расходуется на повторное испарение конденсата, причем предпочтительно его компонента с меньшей температурой кипения. Этот процесс конденсации – испарения многократно повторяется, и из дефлегматора в холодильник (5) поступает пар, обогащенный легко летучим компонентом.
Следует отметить, что эффективность работы дефлегматора тем выше, чем он длиннее, лучше термоизолирован и чем медленнее осуществляется перегонка. Установлено, что перегонка с дефлегматором длиной 1 м соответствует обычной двукратной перегонке. Практически используемые дефлегматоры в два – три раза короче, поэтому для более менее удовлетворительного разделения компонентов жидкости перегонку приходится повторять.
Очень простой по конструкции и эффективной в работе является лабораторная ректификационная колонка, представляющая собой стеклянную трубку диаметром 35 – 40 мм длиной 70 – 80 см, заполненную стеклянными колечками диаметром 4 – 5 мм или обрезками трубочек диаметром 2 – 2,5 мм длиной 6 – 7 мм. Такую колонку, как и дефлегматор, следует хорошо термоизолировать. Примерно половину выходящих из нее паров следует сконденсировать в обратном холодильнике и вернуть назад в колонку в виде флегмы. Вторая половина направляется в прямой холодильник и далее через алонж в приемную колбу. Перегонка с такой колонкой в 5 –10 раз более эффективна, чем обычная.
Существуют смеси, которые при определенном составе дают пар, не отличающийся по составу от жидкости. Они называются азеотропными (постояннокипящими) и разделить их никакой перегонкой невозможно. Примером азеотропа может служить смесь 95,57 % этилового спирта и 4,43 % воды. Эта смесь, подобно чистому веществу, вся выкипает при постоянной температуре (78,15° С).
Дополнительные сведения по технике лабораторных работ см. в [5, 6].
Контрольные вопросы
1. Какие типы перегонки применяют для разделения и очистки органических жидкостей?
2. Изобразите схему установки для простой перегонки.
3. Какова темературная зависимость давления насыщенных паров органических жидкостей?
4. Что называется кипением? При каких условиях жидкость закипает?
5. В чем особенности перегонки жидкостей под вакуумом?
6. В каких случаях применяют перегонку с водяным паром? Какими свойствами должна обладать органическая жидкость, чтобы она перегонялась с паром?
7. В чем суть фракционной перегонки?
8. Для чего применяют дефлегматор и ректификационные колонки? Каковы принципы их работы?
9. Что такое азеотропные смеси?
Хроматография
Хроматография – это метод разделения, качественного и количественного анализа смесей веществ, основанный на распределении вещества между двумя фазами – подвижной и неподвижной. Подвижная фаза в большинстве случаев – растворитель или газ, неподвижная – сорбент с высокоразвитой поверхностью. Примеры неподвижной фазы – фильтровальная бумага (есть специальная бумага для хроматографии), тонкие порошки оксида алюминия, диоксида кремния, талька, сахара и т.д.
Вариантов хроматографии много, но наибольшее распространение получили адсорбционная, открытая российским ученым М. С. Цветом, газо-жидкостная, тонкослойная и бумажная. Все они используются в студенческом лабораторном практикуме.
По назначению хроматографию подразделяют на аналитическую – качественный и количественный анализ – и препаративную. В аналитических целях используют и адсобционную, и газо-жидкостную хроматографию. В препаративных, для получения индивидуальных веществ, – в основном адсорбционную. Для анализа качественного и количественного состава смесей веществ относительно небольшой молекулярной массы применяют газо-жидкостную хроматографию.
|
из
5.00
|
Обсуждение в статье: Фракционная перегонка и перегонка с дефлегматором |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

