 |
Главная |
Влияние природы реагирующих веществ
|
из
5.00
|
Реакция протекает в направлении разрушения менее прочных связей и образования веществ с более прочными связями.
Реакция водорода  с фтором
с фтором  при комнатной температуре протекает практически мгновенно с взрывом
при комнатной температуре протекает практически мгновенно с взрывом  , с бромом
, с бромом  медленно даже при нагревании
медленно даже при нагревании  , c кислородом (О2) – при комнатной температуре не протекает, а при 7000С проходит быстро с взрывом (2Н2+О2=2Н2О).
, c кислородом (О2) – при комнатной температуре не протекает, а при 7000С проходит быстро с взрывом (2Н2+О2=2Н2О).
Влияние концентрации.
С увеличением концентрации чаще происходят столкновения молекул реагирующих веществ – скорость возрастает. Эта зависимость описывается основным кинетическим уравнением. Для гомогенной системы скорость необратимой реакции аА+вВ®сС+dД равна:
 ,
,
где СА и СВ – молярные концентрации взаимодействующих веществ; k – константа скорости прямой реакции;  и
и  – коэффициенты, называемые порядком реакции по веществам А и В.
– коэффициенты, называемые порядком реакции по веществам А и В.
Общий порядок реакции (n) определяется как сумма порядков реакции по каждому реагенту:

Для простых гомогенных реакций, протекающих в однородной среде в одну стадию, порядок реакции по компонентам совпадает со стехиометрическими коэффициентами в уравнении реакции. Зависимость скорости реакции от концентрации в этом случае выражается законом действующих масс, по которому скорость реакции пропорциональна произведению концентраций реагирующих веществ в степенях их стехиометрических коэффициентов.
 .
.
Физический смысл константы скорости химической реакции в том, что она численно равна скорости реакции при концентрации реагирующих веществ 1 моль/л. Константа скорости реакции зависит от природы реагирующих веществ, температуры и катализатора, но не зависит от концентрации реагентов.
Для гетерогенных реакций (протекающих на границе раздела фаз) концентрация твердой фазы, как величина постоянная, в выражение скорости реакции не входит.
Например, для реакции S(T) + O2(Г) = SO2(Г) закон действующих масс для прямой реакции запишется так:
 .
.
Влияние температуры.
Необходимым условием взаимодействия молекул является их столкновение. Но не все столкновения молекул эффективны и приводят к образованию продуктов реакции. Среди всех молекул, имеющихся в системе, можно выделить активные молекулы. Эти молекулы обладают определенной энергией, достаточной для того, чтобы их столкновения были эффективными. Поскольку кинетическая энергия молекулы растет с повышением температуры (следствие увеличения скорости теплового движения молекулы), число активных молекул в общей их массе возрастает при возрастании температуры.
Правило Вант–Гоффа: скорость большинства химических реакций при увеличении на 10 К увеличивается в 2–4 раза.
 , где
, где  и
и  – скорости реакции при температурах
– скорости реакции при температурах  – температурный коэффициент, значение которого для многих реакций лежит в пределах 2-4.
– температурный коэффициент, значение которого для многих реакций лежит в пределах 2-4.
Это уравнение можно записать и через константы скоростей химических реакций:

где  и
и  – константы скоростей реакции при температурах
– константы скоростей реакции при температурах  и
и 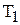 .
.
Уравнение Аррениуса устанавливает более точную зависимость константы скорости химической реакции от температуры:

где  – константа скорости реакции;
– константа скорости реакции;  – предэкспоненциальный множитель, учитывающей вероятность столкновения частиц; е–основание натурального логарифма; R–универсальная газовая постоянная; Т–температура;
– предэкспоненциальный множитель, учитывающей вероятность столкновения частиц; е–основание натурального логарифма; R–универсальная газовая постоянная; Т–температура;  – энергия активации.
– энергия активации.
Энергия активации – это тот избыток энергии по сравнению со средней энергией молекул при данной температуре, которым должны обладать молекулы реагирующих веществ, чтобы они могли вступить в химическую реакцию.
Энергия активациитратится на преодоление межмолекулярных взаимодействий, на преодоление сил отталкивании между электронными оболочками реагирующих частиц при их сближении, на ослабление химических связей внутри реагирующих частиц и т.д.
Чем больше величина энергии активации реакции, тем сильнее зависит скорость этой реакции от температуры.
После математических преобразований уравнение Аррениуса принимает вид:

где  и
и  – константы скоростей химических реакций при температурах
– константы скоростей химических реакций при температурах  и
и 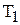 .
.
|
из
5.00
|
Обсуждение в статье: Влияние природы реагирующих веществ |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

