 |
Главная |
КОРПУСКУЛЯРНО-ВОЛНОВОЙ ДУАЛИЗМ
|
из
5.00
|
ЗАДАНИЕ № 29
Два источника излучают свет с длиной волны 375 и 750 нм. Отношение импульсов фотонов, излучаемых первым и вторым источником равно …
ВАРИАНТЫ ОТВЕТОВ:
1) 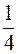 ; 2)
; 2)  ; 3) 2 ; 4) 4 .
; 3) 2 ; 4) 4 .
ЗАДАНИЕ № 30
Если скорость частиц одинакова, то наименьшей длиной волны обладает …
ВАРИАНТЫ ОТВЕТОВ:
1)  -частица ; 2) нейтрон ; 3) электрон ; 4) протон .
-частица ; 2) нейтрон ; 3) электрон ; 4) протон .
ЗАДАНИЕ № 31
Если частицы имеют одинаковую длину волны де Бройля, то наименьшей скоростью обладает …
ВАРИАНТЫ ОТВЕТОВ:
1)  -частица; 2) нейтрон; 3) позитрон; 4) протон.
-частица; 2) нейтрон; 3) позитрон; 4) протон.
ЗАДАНИЕ № 32
Если частицы имеют одинаковую скорость, то наибольшей длиной волны де Бройля обладает …
ВАРИАНТЫ ОТВЕТОВ:
1) электрон; 2) нейтрон; 3) протон; 4)  -частица.
-частица.
ЗАДАНИЕ № 33
Отношение длин волн де Бройля электрона и протона  , имеющих одинаковую скорость, составляет величину порядка…
, имеющих одинаковую скорость, составляет величину порядка…
ВАРИАНТЫ ОТВЕТОВ:
1)103; 2) 1; 3) 10;4)10–3 .
---------------------------
Указание к заданиям № 29 – 33
Связь между длиной волны де Бройля (  ) и импульсом (p) частицы:
) и импульсом (p) частицы:
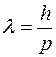 (h – постоянная Планка).
(h – постоянная Планка).
Для нерелятивистской частицы ( 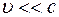 ) справедливо:
) справедливо:  ,
,
где m – масса частицы, а  – её скорость.
– её скорость.
ПОСТУЛАТЫ БОРА. СПЕКТР АТОМА ВОДОРОДА
ЗАДАНИЕ № 34
Электрон в атоме водорода перешёл из основного состояния в возбужденное с n=3 . Радиус его боровской орбиты …
ВАРИАНТЫ ОТВЕТОВ:
1) увеличился в 2 раза;
2) увеличился в 3 раза;
3) увеличился в 9 раз;
4) уменьшился в 3 раза;
5) не изменился.
ЗАДАНИЕ № 35
Схемаэнергетических уровней атома водорода показана на рисунке …
ВАРИАНТЫ ОТВЕТА:

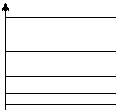
 1) 2) 3)
1) 2) 3)
ЗАДАНИЕ № 36
На рисунке представлена диаграмма энергетических уровней атома. Переход с поглощениемфотона наибольшей частоты обозначен цифрой …
 |
ВАРИАНТЫ ОТВЕТА:
1) 1 ; 2) 2 ; 3) 3 ; 4) 4 ; 5) 5 .
ЗАДАНИЕ № 37
Видимой части спектра излучения атома водорода соответствует формула …
ВАРИАНТЫ ОТВЕТА:
1)  , n = 2 , 3 , 4 …
, n = 2 , 3 , 4 …
2)  , n = 3 , 4 , 5 …
, n = 3 , 4 , 5 …
3)  , n = 4 , 5 , 6 …
, n = 4 , 5 , 6 …
4)  , n = 5 , 6 , 7 …
, n = 5 , 6 , 7 …
ЗАДАНИЕ № 38
На рисунке изображены стационарные орбиты атома водорода согласно модели Бора, а также условно изображены переходы электронов с одной стационарной орбиты на другую, сопровождающиеся излучением кванта энергии. В ультра фиолетовой области спектра эти переходы дают серию Лаймана, в видимой – серию Бальмера, и инфракрасной – серию Пашена.
Наименьшей частоте кванта в серии Бальмерасоответствует переход …
 |
ВАРИАНТЫ ОТВЕТОВ:
1) n = 2 → n = 1
2) n = 3 → n = 2
3) n = 4 → n = 3
4) n = 5 → n = 2
ЗАДАНИЕ № 39
На рисунке изображены стационарные орбиты атома водорода согласно модели Бора, а также условно изображены переходы электронов с одной стационарной орбиты на другую, сопровождающиеся излучением кванта энергии. В ультра фиолетовой области спектра эти переходы дают серию Лаймана, в видимой – серию Бальмера, и инфракрасной – серию Пашена.
Наименьшей частоте кванта в серии Лайманасоответствует переход …
 |
ВАРИАНТЫ ОТВЕТОВ:
1) n = 5 → n = 1
2) n = 5 → n = 2
3) n = 5 → n = 3
ЗАДАНИЕ № 40
На рисунке изображены стационарные орбиты атома водорода согласно модели Бора, а также условно изображены переходы электронов с одной стационарной орбиты на другую, сопровождающиеся излучением кванта энергии. В ультра фиолетовой области спектра эти переходы дают серию Лаймана, в видимой – серию Бальмера, и инфракрасной – серию Пашена.
Наименьшей частоте кванта в серии Пашенасоответствует переход …

ВАРИАНТЫ ОТВЕТОВ:
1) n = 2 → n = 1
2) n = 4 → n = 3
3) n = 5 → n = 1
4) n = 5 → n = 3
ЗАДАНИЕ № 41
В атоме водорода электрон переходит с одного энергетического уровня на другой, как показано на рисунке.
Чему равно изменение его главного Dn и орбитального Dl квантовых чисел?
 |
ВАРИАНТЫ ОТВЕТОВ:
1) Δn = –2; Δl = +1
2) Δn = +2; Δl = –1
3) Δn = –1; Δl = 0
4) Δn = +1; Δl = +1
5) Δn = +2; Δl = +1
ЗАДАНИЕ № 42
В атоме водорода электрон переходит с одного энергетического уровня на другой, как показано на рисунке.
Чему равно изменение его главного Dn и орбитального Dl квантовых чисел?
 |
ВАРИАНТЫ ОТВЕТОВ:
1) Δn = +2; Δl = –1
2) Δn = +2; Δl = +1
3) Δn = –2; Δl = +1
4) Δn = –1; Δl = 0
5) Δn = –2; Δl = –1
ЗАДАНИЕ № 43
При переходах электрона в атоме с одного уровня на другой закон сохранения момента импульса накладывает определённые ограничения (правила отбора). В энергетическом спектре атома водорода запрещённым переходом является …
ВАРИАНТЫ ОТВЕТОВ:
1) 4f – 3d ; 2) 4s – 3p ; 3) 3s – 2s ; 4) 3p – 2s .
ЗАДАНИЕ № 44
При переходах электрона в атоме с одного уровня на другой закон сохранения момента импульса накладывает определённые ограничения (правила отбора).
 |
Если система энергетических уровней атома водорода имеет вид, представленный на рисунке, то запрещёнными переходами являются …
А) 5p-2s; B) 3s-2s; C) 4s-3p; D) 4f-3p.
ВАРИАНТЫ ОТВЕТОВ:
1) A, C ; 2) B, C ; 3) A, D ; 4) B, D .
ЗАДАНИЕ № 45
Закон сохранения момента импульса накладывает ограничения на возможные переходы электрона в атоме водорода с одного уровня на другой (правила отбора). В энергетическом спектре атома водорода (рисунок) запрещённым переходом является …
ВАРИАНТЫ ОТВЕТОВ:
 1) 3s – 2p
1) 3s – 2p
2) 4s – 3p
3) 4s – 3d
4) 2p – 1s
---------------------------
Указание к заданиям № 34 - 45
ПОСТУЛАТЫ БОРА
Первый постулат. В атоме существуют стационарные (не изменяющиеся со временем) состояния, характеризующиеся определенными дискретными значениями энергии. Стационарным состояниям атома соответствуют стационарные op6иты, на которых находятся электроны. В соответствии с первым постулатом Бора электрон, двигаясь по круговой стационарной орбите обладает определенным значением момента импульса, удовлетворяющем условию:
 ,
,
где me –масса электрона,
υn – скорость электрона на n-й орбите радиуса rn,
ħ=h/2π (h – постоянная Планка).
Радиус n-ой орбиты для атома водорода:

где e – заряд электрона, εо – электрическая постоянная.
По теории Бора полная энергия электрона в атоме водорода может принимать дискретный ряд значений:

где n – номер орбиты электрона (номер стационарного состояния атома).
Второй постулат. При переходе электрона с одной орбиты на другую излучается фотон с энергией hν, равной разности энергий соответствующих стационарных состояний En и Еm :
hν= En– Em.
Наборвозможных дискретных частот ν переходов атома между стационарными состояниями атома определяет линейчатый спектр атома.
В спектре атома водорода частота квантового перехода:

где R – постоянная Ридберга, m = 1, 2, 3, …; n = m+1, m+2, m+3, …
Эта обобщенная формула Бальмера описывает серии линий в спектре атома водорода, где m определяет серию (m = 1, 2, 3…), а n определяет отдельные линии соответствующей серии (n = m+1, m+2, …).
В ультрафиолетовой области спектра атома водорода наблюдается

В видимой области спектра атома водорода наблюдается

В инфракрасной области спектра атома водорода наблюдаются




В квантовой механике считается, что электрон при своем движении как бы «размазан» по всему объему, образуя электронное облако, плотность (густота) которого характеризует вероятность нахождения электрона в различных точках объема. Размер, форму и ориентацию электронного облака в пространстве характеризуют, соответственно, квантовые числа n, l и ml .
n (главное квантовое число) определяет энергетические уровни электрона в атоме, принимая следующие значения: п = 1,2,3,... ;
l (орбитальное квантовое число) определяет форму электронного облака, принимая следующие значения: l = 0, 1, 2, ... n–1;
ml (магнитное квантовое число определяет ориентацию электронного облака в пространстве, принимая следующие значения: ml=0, ±1, ±2, …±l .
Состояние электрона в атоме водорода определяется набором квантовых чисел.
При l = 0 состояние электрона называется s-состоянием, при l=1состояние электрона соответствует р-состоянию, при l = 2 – d-состоянию и т. д.
При записи состояния электрона значение n указывается перед условным обозначением орбитального квантового числа, например, 2s (n = 2, l = 0).
Правила, ограничивающие число возможных переходов электронов при испусканием или при поглощением света, называются правилами отбора.
Правила отбора для орбитального и магнитного квантовых чисел:
∆l = ±1; ∆ml = 0, ±1.
С учетом этих правил отбора спектральной серии Лаймана соответствуют переходы: np → 1s (n = 2, 3, 4, ...), а для серии Бальмера соответствуют переходы np → 2s, ns → 2p, nd → 2p (n = 3, 4, ...) и т. д.
УРАВНЕНИЕ ШРЕДИНГЕРА
|
из
5.00
|
Обсуждение в статье: КОРПУСКУЛЯРНО-ВОЛНОВОЙ ДУАЛИЗМ |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

