 |
Главная |
Правила составления уравнения реакции горения
|
из
5.00
|
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ «ИВАНОВСКИЙ ИНСТИТУТ ГОСУДАРСТВЕННОЙ ПРОТИВОПОЖАРНОЙ СЛУЖБЫ МИНИСТЕРСТВА РОССИЙСКОЙ ФЕДЕРАЦИИ ПО ДЕЛАМ ГРАЖДАНСКОЙ ОБОРОНЫ, ЧРЕЗВЫЧАЙНЫМ СИТУАЦИЯМ И ЛИКВИДАЦИИ ПОСЛЕДСТВИЙ СТИХИЙНЫХ БЕДСТВИЙ»
Кафедра химии, теории горения и взрыва
Т.А Мочалова, Д.В. Батов, А.В. Петров
Теория горения и взрыва
Задания и методические указания по выполнению
Расчетно-графической работы
Иваново
УДК 536+54.01+544.4+547
Мочалова Т.А, Батов Д.В., Петров А.В. Теория горения и взрыва. Задания и методические рекомендации по выполнению расчетно-графической работы. Учебное пособие. Иваново: ООНИ ИвИ ГПС МЧС России, 2012.- 38 с.
Учебное пособие предназначено для обучающихся по специальности 280705 Пожарная безопасность и направлению подготовки 280700 Техносферная безопасность. Учебное пособие охватывает основные темы дисциплины «Теория горения и взрыва» и рассчитано на более глубокое ее усвоение. Пособие содержит варианты контрольных заданий и методические рекомендации по выполнению расчетно-графической работы по дисциплине «Теория горения и взрыва».
Печатается по решению Редакционно-издательского совета института
Рассмотрено и рекомендовано к публикации кафедрой химии, теории горения и взрыва, протокол № 7 от 22 декабря 2011 года.
Рецензенты:
Ведущий научный сотрудник ФГБУН
Институт химии растворов им. Г.А.Крестова РАН
доктор химических наук П.Р.Смирнов
Старший преподаватель
кафедры физики и теплотехники
Ивановского института ГПС МЧС России
кандидат химических наук О.Е.Сторонкина
© Ивановский институт ГПС МЧС России, 2012
содержание
| Стр. | ||
| Список используемых сокращений | ||
| ВВЕДЕНИЕ | ||
| Общие указания по выполнению расчетно-графической работы | ||
| Правила составления уравнения реакции горения | ||
| Пример решения задач | ||
| Задачи для самостоятельного решения | ||
| Список рекомендуемой литературы | ||
| Приложения |
Список используемых сокращений
КПР – концентрационные пределы распространения пламени
НКПР – нижний концентрационный предел распространения пламени
ВКПР - верхний концентрационный предел распространения пламени
ТПР – температурные пределы распространения пламени
ПГ – продукты горения
ГВ – горючее вещество
ТНТ - тринитротолуол
Введение
В результате изучения дисциплины «Теория горения и взрыва» у обучающихся формируется теоретический фундамент для глубокого осмысления всей системы показателей пожарной опасности веществ и материалов как совокупности предельных условий и параметров возникновения и прекращения горения.
Овладение методами расчета показателей пожарной опасности веществ необходимо, прежде всего, для будущей практической деятельности: для решения вопросов обеспечения безопасности технологических процессов, зданий и сооружений, а также обеспечения пожарной безопасности людей во время пожаров.
Использование знаний о механизмах протекания горения дает возможность управлять горением на пожаре, организовывать профилактические меры против возникновения самовоспламенения, самовозгорания, воспламенения, меры по снижению интенсивности горения на пожаре, его локализации и тушению.
1. Общие указания по выполнению расчетно-графической работы
В соответствие с учебным планом обучающиеся по дисциплине «Теория горения и взрыва» обязаны выполнить расчетно-графическую работу. Расчетно-графическая работа выполняется по индивидуальному заданию.
Вариант задания выбирается по двум последним цифрам номера зачётной книжки (Приложение 1).
При необходимости преподаватель имеет право изменить вариант расчетно-графической работы обучающегося.
Расчетно-графические работы могут быть оформлены как в ученических тетрадях в объеме не более 18 листов рукописного текста, так и на листах формата А-4, в объеме не более 15 листов, компьютерным набором, ориентация книжная.
При выполнении расчетно-графической работы в ученической тетради с полями, содержащей не менее 18 листов, на титульном листе тетради должны быть указаны звание, фамилия, имя, отчество, номер зачётной книжки и номер учебной группы обучающегося. Работа выполняется аккуратно, разборчивым почерком через строчку, графики вычерчиваются при помощи линейки и карандаша. В задании должны быть представлены номер и полный текст задачи.
При выполнении расчетно-графической работы на компьютере необходимо учитывать следующие требования:
- ориентация страниц – книжная;
- на титульном листе указывается министерство, название кафедры, фамилия, инициалы обучающегося, номер учебной группы, номер варианта, должность, фамилия, инициалы преподавателя (приложение 3);
- поля: верхнее – 1 см, левое – 2 см, нижнее – 1 см, правое – 1 см;
- интервал между строками- одинарный;
- красная строка 1,5 см от левой границы текста;
- нумерация по центру листа внизу;
- шрифт Times New Roman, размер шрифта 14;
- работа скрепляется в папку-скоросшиватель.
Задание должно быть оформлено в соответствии со следующей схемой: формулировка задачи, дано, найти, решение, ответ.
При решении задач даются ссылки на использованные справочные данные и соответствующий литературный источник. Литература, используемая в процессе выполнения задания, приводится в конце работы. Список литературы составляется с учетом правил оформления библиографии (Приложение 1).
Выполненная и правильно оформленная расчетно-графическая работа сдается преподавателю. Работа, выполненная не по своему варианту, к зачету не принимается. Такая работа должна быть выполнена повторно.
Правила составления уравнения реакции горения
При решении практически всех задач по дисциплине "Теория горения и взрыва" необходимо составить уравнение реакции горения. Поэтому очень важно научиться делать это правильно. Изучите изложенные ниже правила составления уравнений реакции горения, разберите примеры.
Правило № 1. В левой части уравнения записываем горючее вещество и окислитель [воздух в виде(O2 + 3,76N2)].
Правило № 2.В правой части уравнения записываем продукты реакции горения, учитывая, что:
углерод (С), содержащийся в горючем веществе, превращается в CO2,
сера (S), содержащаяся в горючем веществе, превращается в SO2,
фосфор (Р), содержащийся в горючем веществе, превращается в P2O5,
водород (Н), содержащийся в горючем веществе, превращается в H2O,
хлор (Cl), содержащийся в горючем веществе, превращается в HCl,
фтор (F), содержащийся в горючем веществе, превращается в HF,
бром (Br), содержащийся в горючем веществе, превращается в HBr,
йод (I), содержащийся в горючем веществе, превращается в HI,
кислород (О), содержащийся в горючем веществе, входит в состав образующихся оксидов (CO2, SO2, H2O) как и кислород воздуха.
азот (N), при температуре горения ниже 2000 оС не вступает в реакцию. Поскольку, в условиях реального пожара температура не превышает значения 1500 – 1600 оС, то принимают, что азот выделяется в свободном виде (N2). Следовательно, 3,76 молей N2 из воздуха переходят в неизменном виде в продукты горения.
Если горючее вещество содержит другие элементы, то они переходят в высшие оксиды.
Правило № 3. Атомы кислорода, входящие в состав молекул горючего вещества (например, C2H6OS - 2-тиолэтанол), участвуют в реакции горения в качестве окислителя, как кислород воздуха.
Правило № 4.Расставляем коэффициенты в схеме реакции горения для того, чтобы в исходных веществах (левая часть уравнения) и получившихся из них продуктах реакции (правая часть уравнения) содержалось одинаковое количество атомов данного вида. При подсчете количества атомов данного вида стехиометрические коэффициенты и индексы, указывающие количество атомов в молекуле, перемножаются.
Рекомендуется придерживаться следующей последовательности действий.
Перед формулой горючего вещества всегда ставится коэффициент 1, так как все расчеты ведут на 1 моль горючего вещества.
Перед формулой углекислого газа ставится коэффициент равный количеству атомов углерода в молекуле горючего вещества.
Уравниваем число атомов элементов, входящих в состав молекул горючего вещества, за исключением Н, О и N.
Уравниваем число атомов водорода, учитывая их содержание в молекулах галогеноуглеводородов и воды.
Уравниваем число атомов кислорода, рассчитав их количество в правой части уравнения и учитывая атомы кислорода, содержащиеся в молекуле горючего вещества.
Коэффициент, поставленный перед молекулой кислорода, переносим в правую часть уравнения и ставим перед 3,76N2. Уравниваем число атомов азота, содержащиеся в молекуле горючего вещества.
Рассмотрим несколько примеров составления реакций горения веществ в воздухе, в которых использованы описанные выше правила.
Пример 1. Составить уравнение реакции горения С6Н4N2О4 в воздухе.
Решение.
1. В левой части уравнения записываем формулу горючего вещества плюс воздух:
С6Н4N2О4 + (О2 + 3,76 N2)
2. В правой части уравнения записываем продукты реакции горения, основываясь на составе молекулы горючего вещества (правило 2):
С6Н4N2О4 + (О2 + 3,76 N2) → СО2 + Н2О + N2 + 3,76 N2
Таким образом, углерод (С), содержащийся в горючем веществе, перешел в СО2, водород превратился в воду, кислород вошел в состав воды и углекислого газа, азот выделился в свободном виде - N2. Азот, содержащийся в воздухе, также не участвует в реакции горения и выделяется в неизменном виде – 3,76 N2.
3. Расставляем коэффициенты в схеме реакции горения.
а) Перед формулой горючего вещества всегда ставится коэффициент 1:
1С6Н4N2О4 + (О2 + 3,76 N2) → СО2 + Н2О + N2 + 3,76 N2
б) Перед формулой углекислого газа ставим коэффициент 6, равный количеству атомов углерода в молекуле горючего вещества:
1С6Н4N2О4 + (О2 + 3,76 N2) → 6СО2 + Н2О + N2 + 3,76 N2
в) Уравниваем число атомов элементов, входящих в состав молекулы горючего вещества, за исключением Н и О. В данном случае уравниваем число атомов азота. В состав горючего вещества входят два атома азота. В составе выделившейся молекулы азота тоже два атома, поэтому перед молекулой азота в продуктах реакции ставим коэффициент 1:
1С6Н4N2О4 + (О2 + 3,76 N2) → 6СО2 + Н2О + 1N2 + 3,76 N2
г) Уравниваем число атомов водорода. В составе молекулы горючего вещества четыре атома водорода. В состав молекулы воды входит только два атома. Следовательно, перед формулой воды ставим коэффициент 2:
1С6Н4N2О4 + (О2 + 3,76 N2) → 6СО2 + 2Н2О + 1N2 + 3,76 N2
д) Уравниваем число атомов кислорода. Для этого рассчитываем число атомов кислорода в правой части уравнения:
в составе шести молекул углекислого газа: 6 ∙ 2 = 12;
в составе двух молекул воды: 2 ∙ 1 = 2;
итого: 12 + 2 = 14 атомов кислорода.
Рассчитываем число атомов кислорода в левой части уравнения. В составе молекулы горючего вещества имеется 4 атома кислорода. Вычитаем это число из количества атомов кислорода в правой части уравнения (14 – 4 = 10). Затем делим полученное число на 2 (количество атомов водорода в Н2О) (10/2 = 5) и ставим полученный коэффициент перед воздухом:
1С6Н4N2О4 + 5(О2 + 3,76 N2) → 6СО2 + 2Н2О + 1N2 + 3,76 N2
е) коэффициент 5, поставленный перед воздухом, ставим перед 3,76N2 в правой части уравнения:
1С6Н4N2О4 + 5(О2 + 3,76 N2) = 6СО2 + 2Н2О + 1N2 + 5 ∙ 3,76 N2
Чтобы убедиться в правильности составленного уравнения реакции горения, рассчитаем количество атомов одних и тех же элементов в его правой и левой частях:
С – слева 6, справа 6 ∙ 1 = 6;
Н – слева 4, справа 2 ∙ 2 = 4;
N – слева: в горючем веществе 2, в воздухе 5∙ 3,76 = 18,8, итого 20,8;
справа 2 + 5∙ 3,76 = 20,8;
О - слева: в горючем веществе 4, в воздухе 5 ∙ 2 = 10, итого 14;
справа: в углекислом газе 6 ∙ 2 = 12, в воде 2 ∙ 1 = 2, итого 14.
Вывод: уравнение реакции горения составлено верно.
Пример 2. Составить уравнение реакции горения п-дихлорбензола (С4Н4Сl2) в воздухе.
Решение.
1. В левой части уравнения записываем формулу горючего вещества плюс воздух:
С4Н4Сl2 + (О2 + 3,76 N2)
2. В правой части уравнения записываем продукты реакции горения, основываясь на составе молекулы горючего вещества (правило 2):
С4Н4Сl2 + (О2 + 3,76 N2) → СО2 + Н2О + HCl + 3,76 N2
Таким образом, углерод (С), содержащийся в горючем веществе, перешел в СО2, водород превратился в воду, хлор превратился в хлороводород. Азот, содержащийся в воздухе, не участвует в реакции горения и выделяется в неизменном виде – 3,76 N2.
3. Расставляем коэффициенты в схеме реакции горения.
а) Перед формулой горючего вещества всегда ставится коэффициент 1:
1 С4Н4Сl2 + (О2 + 3,76 N2) → СО2 + Н2О + HCl+ 3,76 N2
б) Перед формулой углекислого газа ставим коэффициент 4, равный количеству атомов углерода в молекуле горючего вещества:
1С4Н4Сl2 + (О2 + 3,76 N2) → 4СО2 + Н2О + HCl+ 3,76 N2
в) Уравниваем число атомов элементов, входящих в состав горючего вещества, за исключением Н, О, N. В данном случае уравниваем число атомов хлора. В состав горючего вещества входят два атома хлора. В составе выделившейся молекулы хлороводорода один атом Cl, поэтому перед молекулой хлороводорода в продуктах реакции ставим коэффициент 2:
1С4Н4Сl2 + (О2 + 3,76 N2) → 4СО2 + Н2О + 2HCl+ 3,76 N2
г) Уравниваем число атомов водорода. В составе молекулы горючего вещества четыре атома водорода. Из них два атома водорода уже вошли в состав двух молекул хлороводорода. Оставшиеся два атома водорода перейдут в состав молекулы Н2О. Следовательно, перед молекулой воды ставим коэффициент 1:
1С4Н4Сl2 + (О2 + 3,76 N2) → 4СО2 + 1Н2О + 2HCl+ 3,76 N2
д) Уравниваем число атомов кислорода. Для этого рассчитываем число атомов кислорода в правой части уравнения:
в составе четырех молекул углекислого газа: 4 ∙ 2 = 8;
в составе одной молекулы воды: 1 ∙ 1 = 1;
итого: 8 + 1 = 9 атомов кислорода.
Рассчитываем число атомов кислорода в левой части уравнения. В составе молекулы горючего вещества нет атомов кислорода. Следовательно, делим количество атомов кислорода в правой части уравнения на 2 (9 /2 = 4,5) и ставим полученный коэффициент перед воздухом:
1С4Н4Сl2 + 4,5(О2 + 3,76 N2) → 4СО2 + 1Н2О + 2HCl+ 3,76 N2
е) коэффициент 4,5, поставленный перед воздухом, ставим перед 3,76N2 в правой части уравнения:
1С4Н4Сl2 + 4,5(О2 + 3,76 N2) = 4СО2 + 1Н2О + 2HCl+ 4,5 ∙3,76 N2
Пример 3. Составить уравнение реакции горения ацетилена (С2Н2) в воздухе.
Решение.
1. В левой части уравнения записываем формулу горючего вещества плюс воздух:
С2Н2 + (О2 + 3,76 N2)
2. В правой части уравнения записываем продукты реакции горения, основываясь на составе молекулы горючего вещества (правило 2):
С2Н2 + (О2 + 3,76 N2) → СО2 + Н2О + 3,76 N2
Таким образом, углерод (С), содержащийся в горючем веществе, перешел в СО2, водород превратился в воду. Азот, содержащийся в воздухе, не участвует в реакции горения и выделяется в неизменном виде – 3,76 N2.
3. Расставляем коэффициенты в схеме реакции горения.
а) Перед формулой горючего вещества всегда ставится коэффициент 1:
1 С2Н2 + (О2 + 3,76 N2) → СО2 + Н2О + 3,76 N2
б) Перед формулой углекислого газа ставим коэффициент 2, равный количеству атомов углерода в молекуле ацетилена:
1 С2Н2 + (О2 + 3,76 N2) → 2СО2 + Н2О + 3,76 N2
в) Уравниваем число атомов элементов, входящих в состав горючего вещества, за исключением Н, О и N. В данном случае таких элементов нет.
г) Уравниваем число атомов водорода. В составе молекулы горючего вещества - два атома водорода. В состав молекулы воды входит также два атома водорода. Следовательно, перед молекулой воды ставим коэффициент 1:
1 С2Н2 + (О2 + 3,76 N2) → 2СО2 + 1Н2О + 3,76 N2
д) Уравниваем число атомов кислорода. Для этого рассчитываем число атомов кислорода в правой части уравнения:
в составе двух молекул углекислого газа: 2 ∙ 2 = 4;
в составе одной молекулы воды: 1 ∙ 1 = 1;
итого: 4 + 1 = 5 атомов кислорода.
Рассчитываем число атомов кислорода в левой части уравнения. В составе молекулы горючего вещества нет атомов кислорода, следовательно, делим количество атомов кислорода в правой части уравнения на 2 (5/2 = 2,5) и ставим данный коэффициент перед воздухом:
1 С2Н2 + 2,5(О2 + 3,76 N2) → 2СО2 + 1Н2О + 3,76 N2
е) коэффициент 2,5, поставленный перед воздухом, ставим перед 3,76N2 в правой части уравнения:
1 С2Н2 + 2,5(О2 + 3,76 N2) = 2СО2 + 1Н2О + 2,5 ∙ 3,76 N2
Пример 4. Составить уравнение реакции горения C6Н8SО3 в воздухе.
Решение.
1.В левой части уравнения записываем формулу горючего вещества плюс воздух:
C6Н8SО3+ (О2 + 3,76 N2)
2. В правой части уравнения записываем продукты реакции горения, основываясь на составе молекулы горючего вещества (правило 2):
C6Н8SО3 + (О2 + 3,76 N2) → СО2 + Н2О + SO2 + 3,76 N2
Таким образом, углерод (С), содержащийся в горючем веществе, перешел в СО2, водород превратился в воду, кислород вошел в состав воды и углекислого газа, сера образовала оксид SO2. Азот воздуха не участвует в реакции горения и выделяется в неизменном виде – 3,76 N2.
3. Расставляем коэффициенты в схеме реакции горения.
а) Перед формулой горючего вещества всегда ставится коэффициент 1:
1 C6Н8SО3 + (О2 + 3,76 N2) → СО2 + Н2О + SO2 + 3,76 N2
б) Перед формулой углекислого газа ставим коэффициент 6, равный количеству атомов углерода в молекуле горючего вещества:
1 C6Н8SО3 + (О2 + 3,76 N2) → 6СО2 + Н2О + SO2 + 3,76 N2
в) Уравниваем число атомов элементов, входящих в состав горючего вещества, за исключением Н, О и N. В данном случае уравниваем число атомов серы. В состав молекулы горючего вещества входит один атом серы. В составе выделившейся молекулы SO2 тоже один атом, поэтому перед молекулой SO2 в продуктах реакции ставим коэффициент 1:
1 C6Н8SО3 + (О2 + 3,76 N2) → 6СО2 + Н2О + 1SO2 + 3,76 N2
г) Уравниваем число атомов водорода. В составе молекулы горючего вещества восемь атомов водорода, а в состав молекулы воды входит только два атома. Следовательно, перед молекулой воды ставим коэффициент 4:
1 C6Н8SО3 + (О2 + 3,76 N2) → 6СО2 + 4Н2О + 1SO2 + 3,76 N2
д) Уравниваем число атомов кислорода. Для этого рассчитываем число атомов кислорода в правой части уравнения:
в составе шести молекул углекислого газа: 6 ∙ 2 = 12;
в составе четырех молекул воды: 4 ∙ 1 = 4;
в составе одной молекулы оксида серы: 1∙ 2 = 2
итого: 12 + 4 + 2 = 18 атомов кислорода.
Рассчитываем число атомов кислорода в левой части уравнения. В составе молекулы горючего вещества имеется 3 атома кислорода. Вычитаем это число из количества атомов кислорода в правой части уравнения (18 – 3 = 15). Делим полученное число на 2 (15 /2 = 7,5) и ставим данный коэффициент перед воздухом:
1 C6Н8SО3 + 7,5(О2 + 3,76 N2) → 6СО2 + 4Н2О + 1SO2 + 3,76 N2
е) коэффициент 7,5, поставленный перед воздухом, ставим перед 3,76N2 в правой части уравнения:
1 C6Н8SО3 + 7,5(О2 + 3,76 N2) = 6СО2 + 4Н2О + 1SO2 +7,5 ∙3,76 N2
Многообразие реакций горения не исчерпывается рассмотренными в данном разделе примерами. Однако, используя описанные правила, можно самостоятельно составить реакцию горения многих других горючих веществ. Написание уравнений реакций горения является важной составной частью при решении многих задач в курсе «Теория горения и взрыва».
Пример решения задач
Задача. Используя данные таблицы, определить показатели пожарной опасности толуола: группу горючести, температуру вспышки; концентрационные пределы распространения пламени (в % и г/м3) при t = 25, 45 и 65 oC, построить график зависимости КПР от температуры; температурные пределы распространения пламени, низшую теплоту сгорания по следствию из закона Гесса; максимальное давление взрыва, тротиловый эквивалент возможного аварийного взрыва при взрыве в технологическом оборудовании. Рассчитать объем воздуха, объем и процентный состав компонентов продуктов горения.
| Начальное давление, Па | Начальная температура, 0С | Температура взрыва, 0С. | Масса вещества, кг | Коэффициент избытка воздуха |
| 101 300 | 1,3 |
Дано:
С7Н8
m = 10 кг;
α = 1,3;
Рн = 0,1 МПа;
tн = 23 0С;
tВЗР = 2678 0С.
Найти: группу горючести, tВСП., КПР, ТПР, QН, РВЗР, VВ, VПГ, φПГ.
Решение:
1. Составляем уравнение реакции горения толуола в воздухе (см. правила составления уравнения реакции горения) и определяем стехиометрический коэффициент β (коэффициент перед кислородом):
1C7Н8 + 9(О2 + 3,76 N2) → 7СО2 + 4Н2О + 9 ∙ 3,76 N2
β = 9
2. Рассчитываем объём, занимаемый 1 кмоль воздуха при заданных условиях.


3. Рассчитываем молярную массу толуола.
М (C7H8) = 12 × 7 + 1 × 8 = 92 (кг/кмоль)
4. Рассчитываем объём воздуха, необходимого для полного сгорания заданной массы толуола.

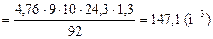
5. Определяем избыточное количество вещества кислорода и азота.
 = b(a - 1), кмоль;
= b(a - 1), кмоль;  = 9(1,3 - 1) = 2,7 (кмоль)
= 9(1,3 - 1) = 2,7 (кмоль)
 =3,76 × b(a - 1), кмоль;
=3,76 × b(a - 1), кмоль;  =3,76 × 9(1,3 - 1) = 10,2 (кмоль)
=3,76 × 9(1,3 - 1) = 10,2 (кмоль)
6. Рассчитываем общее количество вещества продуктов горения.
ånпг =  , кмоль;
, кмоль;
ånпг = 7 + 4 + 33,84 + 2,7 + 10,2 = 57,74 (кмоль)
7. Определяем общий объём образующихся продуктов горения.
 , м3;
, м3;

8. Определяем мольный процентный состав компонентов продуктов горения. Принимаем общее количество вещества продуктов горения за 100%, а количество вещества конкретного продукта реакции за  %:
%:
Для СО2 получаем следующую пропорцию.
ånпг = 57,74 кмоль – 100%
 = 7 кмоль –
= 7 кмоль –  %,
%,
отсюда 
Аналогично находим процентное содержание оставшихся продуктов горения:

При расчете процентного содержания азота суммируем его количество перешедшее в продукты горения в результате реакции и из избытка воздуха.


9. Определяем группу горючести толуола. Для этого рассчитываем его коэффициент горючести по формуле:
К = 4nC + 4nS + nH + nN - 2nO - 2nCl - 3nF - 5nBr
где: nC, nS, nH, nN, nO, nCl, nF, nBr- соответственно число атомов углерода, серы, водорода, азота, кислорода, хлора, фтора, брома в молекуле вещества.
Если расчётное значение К £ 0 – вещество негорючее, 0 < К £ 2 – вещество трудногорючее, К > 2 – вещество является горючим.
Записываем количество атомов составляющих толуол (С7Н8): nC= 7; nH= 8;
Рассчитываем коэффициент горючести:
К = 4nC + 4nS + nH + nN - 2nO -2nCl -3nF - 5nBr = 4 × 7 + 8 = 36
Вывод: К > 2, следовательно, толуол – горючее вещество.
10. Определяем температуру вспышки. Для этого по справочнику [4] находим температуру кипения толуола:
tкип = 110,6 0С.
Определяем температуру вспышки по формуле Элея:
 .
.
Справочное значение 7 0С [4].
11. Рассчитываем нижний и верхний концентрационный пределы распространения пламени толуола при стандартных условиях по формуле:
 , об. %
, об. %
где
 - нижний (верхний) концентрационные пределы распространения пламени, % об.;
- нижний (верхний) концентрационные пределы распространения пламени, % об.;
b - число молекул кислорода, необходимое для полного окисления молекулы горючего;
a и b - константы определяемые по табл. 2 приложения 2.
Концентрационные пределы распространения пламени при заданных условиях рассчитываются по формулам:


где
 и
и  - концентрационные пределы распространения пламени при стандартных условиях (Р = 101325 Па, Т = 298 К);
- концентрационные пределы распространения пламени при стандартных условиях (Р = 101325 Па, Т = 298 К);
 и
и  - концентрационные пределы распространения пламени при заданной температуре Т;
- концентрационные пределы распространения пламени при заданной температуре Т;
1550 К и 1110 К - температура горения соответственно на нижнем и верхнем концентрационных пределах распространения пламени.
Рассчитываем КПР при температуре 298 К.
Для расчета  выбираем из табл. 2 Приложения 2: a = 8.64, b = 4.679.
выбираем из табл. 2 Приложения 2: a = 8.64, b = 4.679.

Для расчета  при b > 7.5 a = 0.768, b = 6.554.
при b > 7.5 a = 0.768, b = 6.554.

Рассчитываем КПР при температуре Т = 273,15 + 45 = 318,15 К.


Рассчитываем КПР при температуре Т = 273,15 + 65 = 338,15 К.


Строим графики зависимостей КПР от температуры.

Из графика делаем вывод, что с увеличением температуры НКПР толуола незначительно уменьшается, ВКПР – сильно возрастает. Изменение ВКПР приблизительно в 10 раз превышает изменение НКПР. Таким образом, с ростом температуры область воспламенения паров толуола расширяется.
12. Рассчитываем концентрационные пределы распространения пламени толуола в граммах на кубометр (j/н или j/в):
 , г/м3
, г/м3
где
Vt – объем занимаемый 1 кмоль газа при заданной температуре и давлении, м3/кмоль;
М – молярная масса, кг/кмоль.
Определяем мольный объем паров толуола при заданных температурах:
При Т = 298.15 К 

При Т = 318.15 К 

При Т = 338.15 К 

Рассчитываем КПР паров толуола при заданных температурах:
При Т = 298.15 К  г/м3;
г/м3;  (г/м3)
(г/м3)
При Т = 318.15 К  г/м3;
г/м3;  (г/м3)
(г/м3)
При Т = 338.15 К 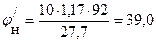 г/м3;
г/м3;  (г/м3)
(г/м3)
13. Определяем температурные пределы распространения пламени по уравнению Антуана:
 ,
,
где
tН(В) – нижний (верхний) температурные пределы распространения пламени;
 - давление насыщенного пара на нижнем (верхнем) температурном пределе распространения пламени, мм.рт.ст.;
- давление насыщенного пара на нижнем (верхнем) температурном пределе распространения пламени, мм.рт.ст.;
А, В, С – константы, определяемые по таблице 10 Приложения 2.
Определяем давление насыщенного пара на нижнем и верхнем температурных пределах распространения пламени по формуле:



Из табл. 10 приложения 2 находим значения констант А, В и С для толуола:
А = 6,95508, В = 1345,087, С = 219,516
Подставляем значения в уравнение Антуана и определяем температурные пределы распространения пламени:
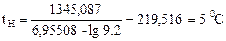

Справочные значения tн = 6 оС, tв = 37 оС [4].
14. Рассчитываем низшую теплоту сгорания толуола, используя следствие из закона Гесса.
Qн = [S(ni×  )ПГ - S(nj×
)ПГ - S(nj×  )ГВ], кДж/моль.
)ГВ], кДж/моль.
Здесь ni×и  - число молей и стандартные энтальпии образования компонентов продуктов горения (ПГ), nj и
- число молей и стандартные энтальпии образования компонентов продуктов горения (ПГ), nj и  - число молей и стандартные энтальпии образования компонентов горючей смеси (ГВ).
- число молей и стандартные энтальпии образования компонентов горючей смеси (ГВ).
По уравнению реакции находим, что при сгорании 1 моль толуола выделяется 7 моль углекислого газа и 4 моль воды:
 ,
,  ,
, 
Определяем по табл. 3 приложения 2 значения стандартных теплот образования горючего вещества и продуктов горения, учитывая при этом, что теплоты образования простых веществ (О2, N2) равны нулю.
Df 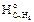 = 50,02 кДж/моль;
= 50,02 кДж/моль;
Df  = -393,65 кДж/моль;
= -393,65 кДж/моль;
Df  = -241,91 кДж/моль
= -241,91 кДж/моль
Следует иметь в виду, что существует две шкалы тепловых эффектов. В термодинамической шкале экзотермическому процессу соответствует знак минус, эндотермическому – знак плюс. В термохимической шкале знаки изменяются на противоположные. В справочной литературе используется в основном термодинамическая шкала. Однако для расчетов в курсе «Теории горения и взрыва» применяют термохимическую шкалу. Поэтому значения стандартных энтальпий образования веществ нужно подставлять в уравнение с обратным знаком.
Qн =  = 7×393,65 + 4×241,91 – 1∙(-50,02) = 3773,21 (кДж/моль)
= 7×393,65 + 4×241,91 – 1∙(-50,02) = 3773,21 (кДж/моль)
15. Рассчитываем максимальное давление взрыва паров толуола при заданных условиях по формуле:

где
Рн – давление паровоздушной смеси до взрыва, Па;
ТВЗР – температура взрыва, К;
Тн - температура паровоздушной смеси до взрыва, К;
Snпг - число моль продуктов горения, моль;
Sncм - число моль исходной газовоздушной смеси, моль.
По уравнению реакции горения определяем число моль газов в горючей смеси до взрыва и число моль продуктов горения.
Sncм =  = 1 + 9 + 9∙3,76 = 43,84 моль
= 1 + 9 + 9∙3,76 = 43,84 моль
ånп.г=  =7 + 4 + 33,84 + 2,7 + 10,2=57,74 (моль)
=7 + 4 + 33,84 + 2,7 + 10,2=57,74 (моль)
Переводим начальную температуру и температуру взрыва из шкалы Цельсия в шкалу Кельвина:
Тн = 273 + 23 = 296 К
ТВЗР = 273 + 2678 = 2951 К
Рассчитываем давление взрыва паров толуола при заданных условиях.

16. Рассчитываем тротиловый эквивалент возможного аварийного взрыва паров толуола при взрыве в технологическом оборудовании по формуле:

где
QН - низшая теплота сгорания взрывчатого вещества, Дж/кг;
mВВ – масса горючего вещества в смеси, кг;
4520×103 – низшая теплота сгорания тринитротолуола (ТНТ, тротил), Дж/кг.
Согласно расчету, проведенному в п.14, низшая теплота сгорания толуола равна Qн = 3773,21 кДж/моль. Переводим ее в кДж/кг, разделив на молярную массу (92∙10-3 кг/моль):

Рассчитываем тротиловый эквивалент возможного аварийного взрыва при взрыве в технологическом оборудовании:
 (кг тротила)
(кг тротила)
Ответ: объем воздуха, необходимый для сгорания 10 кг толуола равен 147,1 м3, объем выделившихся в результате горения продуктов равен 152,5 м3, процентное содержание углекислого газа равно 12,1%, воды – 6,9%, азота – 76,3%, избыточного кислорода – 4,7%; температура вспышки толуола равн
|
из
5.00
|
Обсуждение в статье: Правила составления уравнения реакции горения |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

