 |
Главная |
Свойства кальция и его соединений
|
из
5.00
|
ГЛАВА 16. ЭЛЕКТРОМЕТАЛЛУРГИЯ
КАРБИДА КАЛЬЦИЯ И СИЛИКОКАЛЬЦИЯ
Свойства кальция и его соединений
Кальций представитель группы щелочных металлов Периодической системы элементов Д.И.Менделеева. Порядковый номер кальция 20, атомная масса 40,08.
Конфигурация внешней электронной оболочки атома 2s22p1, температура плавления 839оС, температура кипения 1495оС. Кальций аллотропный металл: до 443оС устойчива модификация a–Са с кубической гранецентрированной решеткой (ГКЦ) (а = 0,558 нм), в интервале 443–842оС – b–Са с ОЦК решеткой (а = 0,448 нм). Плотность кальция 1,54 г/см3.
Система Са–С. При взаимодействии Са с углеродом образуется карбид кальция СаС2 (62,54% Са, 37,46% С). Термодинамические константы карбида кальция: стандартная теплота образования ∆Н 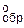 = –58,49 кДж/моль, энтропия S
= –58,49 кДж/моль, энтропия S 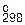 = 69,8 Дж/(моль×K), теплоемкость С
= 69,8 Дж/(моль×K), теплоемкость С  = 62,6 кДж/(моль×K), изменение энергии Гиббса ∆G
= 62,6 кДж/(моль×K), изменение энергии Гиббса ∆G 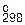 = –64,8 кДж/моль, температура плавления СаС2 равна 2430 K, плотность 2,204 г/см3, зависимость ∆G
= –64,8 кДж/моль, температура плавления СаС2 равна 2430 K, плотность 2,204 г/см3, зависимость ∆G 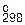 (Т) реакции образования СаС2 из элементов имеет вид:
(Т) реакции образования СаС2 из элементов имеет вид:
Саж + 2Ст = СаС2т; ∆G 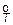 = –60250 – 26,28Т Дж/моль.
= –60250 – 26,28Т Дж/моль.
Система Са–Si (рис. 16.1). Кальций с кремнием образует силициды: Са2Si (25,95% Si) ∆Н 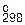 = –209 кДж/моль, Са5Si3 (28,31% Si), СаSi (41,20% Si, ∆Н
= –209 кДж/моль, Са5Si3 (28,31% Si), СаSi (41,20% Si, ∆Н 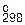 = -150,5 кДж/моль), Ca3Si4 (48,3% Si) и СаSi2 (58,36% Si, ∆Н
= -150,5 кДж/моль), Ca3Si4 (48,3% Si) и СаSi2 (58,36% Si, ∆Н 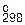 = –150,7 кДж/моль).
= –150,7 кДж/моль).
Cоединения CaSi и CaSi2 плавятся конгруэнтно при 1245 и 1000оС, соединения Ca2Si и Ca3Si4 образуются по перитектическим реакциям при температурах 900 и 1020оС, соответственно.
Зависимости ∆G 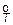 (Т) реакций образования силицида кальция описываются следующими уравнениями (в Дж/моль):
(Т) реакций образования силицида кальция описываются следующими уравнениями (в Дж/моль):
2Саж + Siж = Са2Siж; ∆G 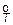 = –217169 + 4,77Т;
= –217169 + 4,77Т;
Саж + Siж = СаSiж ∆G 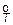 = –146622 + 3,31Т;
= –146622 + 3,31Т;
Саж + 2Siж = СаSi2ж ∆G 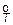 = –18084 – 2,05Т.
= –18084 – 2,05Т.
Рис. 16.1. Диаграмма состояния системы Ca–Si
Система Са–О (рис.16.2). В системе известны оксиды СаО, СаО2 (пероксид), СаО4 (гипероксид), СаО6 (озоид). Наиболее устойчивым является СаО (71,42% Са, 28-58% О). Температура плавления СаО 2613°С, температура кипения свыше 3000°С, плотность 3,37 г/см3, стандартная энтальпия ∆Н 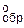 = –635,09 кДж/моль, энтропия S
= –635,09 кДж/моль, энтропия S 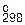 = 38,10 Дж/(моль×K).
= 38,10 Дж/(моль×K).
Типы фазовых превращений, температуры и составы приведены в табл. 16.1.
Температурные зависимости изменения энергии Гиббса реакций образования СаО с учетом агрегатного состояния кальция имеют вид (в Дж/моль):
2Сат + О2 = 2СаОт; ∆G  =–1268600 + 198Т; (А)
=–1268600 + 198Т; (А)
2Саж + О2 = 2СаОт; ∆G  = –1283700 + 215Т; (Б)
= –1283700 + 215Т; (Б)
2Саг + О2 = 2СаОт; ∆G  = –1591900 + 390Т. (С)
= –1591900 + 390Т. (С)
Рис. 16.2. Диаграмма равновесного состояния системы Са–О с указанием предположительного положения линии ликвидуса (Р = 0,1 МПа)
Таблица 16.1. Фазовые превращения в системе Са–О (конденсированное состояние)
| Превращения | Состав, ат.% О | Темпера-тура, оС | Тип превращения | ||
| L®(bCa)+CaO | 0,3 | –839 | эвтектика | ||
| L1®L2+CaO | |||||
| (bCa)®(aCa) | -0 | –443 | эвтектоидное | ||
| (bCa)®(aCa) | 443±3 | аллотропное | |||
| L®(bCa) | 842±3 | плавление | |||
| L®CaO | –50 | 2613±25 | плавление |
Температура начала термической диссоциации СаО (условие ∆G 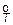 = 0, Р
= 0, Р  = 101 кПа) по реакции (А) равна 6400 K, по реакции (Б) 5970 K.
= 101 кПа) по реакции (А) равна 6400 K, по реакции (Б) 5970 K.
Оксид СаО является основным компонентом ферроплавной извести, которую получают на заводах обжигом известняка (СаСО3). Химизм термической диссоциации СаСО3 описывается реакцией
СаСО3(т) – СаОт + СО2; ∆G 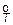 = 170648 – 144,2Т Дж/моль.
= 170648 – 144,2Т Дж/моль.
Зависимость логарифма упругости диссоциации СаСО3 (кПа) от температуры следующая:
lgP  = –37300/T + 36,6.
= –37300/T + 36,6.
Давление P  = 101,3 кПа достигается при 1183 K (910°С).
= 101,3 кПа достигается при 1183 K (910°С).
Система СаО–SiO2 (рис. 16.3). Как следует из диаграммы состояния этой системы, при взаимодействии СаО с SiO2 образуется ряд силикатов 3СаО×SiO2, 2СаО×SiO2, 3СаО×2SiO2 и СаО×SiO2, которые характеризуются относительно высокой термодинамической прочностью (табл. 16.2).
Рис. 16.3. Диаграмма состояния системы СаО–SiO2
Таблица 16.2. Термодинамические свойства силикатов кальция
| Силикат кальция | ∆Н 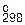 ,
кДж/моль ,
кДж/моль
| ∆G 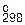 ,
кДж/моль ,
кДж/моль
| S 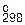 ,
кДж/(моль×K) ,
кДж/(моль×K)
| C  ,
кДж/(моль×K) ,
кДж/(моль×K)
| tпл., оС |
| CaO×SiO2 | –1633 | –1548 | 80,67 | 85,18 | |
| 2CaO×SiO2 | –2312 | –2198 | 120,67 | 126,7 | |
| 3CaO×SiO2 | –2198 | –2189 | 127,5 | 128,5 |
Температурные зависимости изменения энергии Гиббса реакций образование силикатов кальция приведены ниже (Дж/моль):
СаOт + SiO2(т) = a–CaO×SiO2;
∆G  = –89200 + 0,50T;
= –89200 + 0,50T;
СаOт + SiO2(т) = b–CaO×SiO2;
∆G 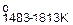 = –83300 – 3,40T;
= –83300 – 3,40T;
2СаOт + SiO2(т) = 2CaO×SiO2;
∆G  = –126236 + 5,02T;
= –126236 + 5,02T;
3СаOт + SiO2(т) = 3CaO×SiO2;
∆G  = –101753 + 16,64T.
= –101753 + 16,64T.
Ортосиликат 2СаО×SiO2 плавится конгруэнтно при 2130°С, моносиликат СаО×SiO2 – конгруэнтно при относительно низкой температуре 1544°С. Ортосиликат 2СаО×SiO2 обладает полиморфизмом. Температуры полиморфных (фазовых) превращений его приведены ниже:

 a-2СаО×SiO2
a-2СаО×SiO2 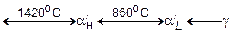
670°С b 405°С
Из приведенной схемы последовательности фазовых превращений 2СаО×SiO2 следует, что переходы a ® 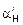 и
и  относятся к энантиотропным, т.е. проходящими в прямом и обратном направлениях, тогда как b ® g и g ®
относятся к энантиотропным, т.е. проходящими в прямом и обратном направлениях, тогда как b ® g и g ®  относятся к монотропным, т.е. проходящими только в одном направлении. Превращение b-2СаО×SiO2 ® g-2СаО×SiO2 сопровождается увеличением объема на 12%, что приводит к рассыпанию ортосиликата и высокоосновных шлаков производства металлического марганца, низкоуглеродистого феррохрома.
относятся к монотропным, т.е. проходящими только в одном направлении. Превращение b-2СаО×SiO2 ® g-2СаО×SiO2 сопровождается увеличением объема на 12%, что приводит к рассыпанию ортосиликата и высокоосновных шлаков производства металлического марганца, низкоуглеродистого феррохрома.
|
из
5.00
|
Обсуждение в статье: Свойства кальция и его соединений |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

