 |
Главная |
Электрометаллургия ферросиликостронция
|
из
5.00
|
Физико-химические свойства стронция и его соединений. Стронций* – химический элемент ІІ группы Периодической системы элементов Д.И.Менделеева, атомный номер 38, атомная масса 87,62, конфигурация внешней электронной оболочки атома 5s2, относится к группе щелочно-земельных металлов. Природный стронций состоит из четырех стабильных изотопов:  (82,56%),
(82,56%),  (9,86%),
(9,86%), 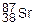 (7,02%) и
(7,02%) и  (0,56%). Степень окисления стронция 2, очень редко 1. Металл существует в трех аллотропных модификациях, превращение которых проходит при следующих температурах:
(0,56%). Степень окисления стронция 2, очень редко 1. Металл существует в трех аллотропных модификациях, превращение которых проходит при следующих температурах:
a-Sr  bSr
bSr  g-Sr
g-Sr  Srж
Srж  Srпар
Srпар
(ГЦК) (гексаг.) (ОЦК)
Энтальпия плавления стронция ∆Нпл= 8,2 кДж/моль, энтальпия испарения ∆Нисп = 133,8 кДж/моль, энтропия ∆S  = 55,70 Дж/(моль×K).
= 55,70 Дж/(моль×K).
Система Sr–O. В системе Sr–O образуется оксид SrO, представляющий собой бесцветные кристаллы плотностью 4,7 г/см3. Температура плавления SrO 2660°С, ∆Н  = –590,5 кДж/моль, энтропия S
= –590,5 кДж/моль, энтропия S  = 55,44 Дж/(моль×K). При прокаливании SrO в среде О2 при высоком давлении образуется переоксид SrO2. При взаимодействии SrO с Н2О образуется гидрооксид Sr(OН)2 – бесцветные гигроскопичные кристаллы, температура плавления 535°С, плотность 3,632 г/см3, ∆С
= 55,44 Дж/(моль×K). При прокаливании SrO в среде О2 при высоком давлении образуется переоксид SrO2. При взаимодействии SrO с Н2О образуется гидрооксид Sr(OН)2 – бесцветные гигроскопичные кристаллы, температура плавления 535°С, плотность 3,632 г/см3, ∆С  = 92,06 Дж/(моль×K); ∆Н
= 92,06 Дж/(моль×K); ∆Н  = –965
= –965
_______________________
* Свойства стронция приведены по данным «Химической энциклопедии». - М.: БСЭ. 1995. т. 4. С. 441.
кДж/моль, S  = 94 Дж/(моль×K).
= 94 Дж/(моль×K).
Зависимости изменения энергии Гиббса реакций образования оксида SrO при взаимодействии стронция различного агрегатного состояния с молекулярным кислородом от температуры имеют вид (в Дж/моль):
2Srтв + О2 = 2SrОтв; ∆G 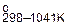 = –1177700+194,1Т;
= –1177700+194,1Т;
2Srж + О2 = 2SrОтв; ∆G  = –1191800+206,5Т;
= –1191800+206,5Т;
2Srг + О2 = 2SrОтв; ∆G 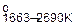 = –1442100+359,9Т.
= –1442100+359,9Т.
Температурная зависимость давления пара над SrO в предположении, что диссоциация SrO не имеет места, описывается уравнением
lgPобщ(атм) = 1,44 + 1,908lgT – 25950/Т (700–1600 K).
Система SrO–СО2. Карбонат стронция SrСО3 – бесцветные кристаллы, существуют в нескольких полиморфных модификациях:
a-SrСО3  bSrСО3
bSrСО3  g-SrСО3
g-SrСО3
(ромб.решетка, (гексагональная (кубическая
пл.3,785 г/см3) решетка) решетка)
Температура плавления SrСО3 1494°С, ∆Н  = –1227,0 кДж/моль, энтропия S
= –1227,0 кДж/моль, энтропия S  = 97,2 Дж/(моль×K). При нагревании SrСО3 диссоциирует по реакции
= 97,2 Дж/(моль×K). При нагревании SrСО3 диссоциирует по реакции
SrСО3 ® SrО + СО2.
Уравнения температурной зависимости давления термической диссоциации SrСО3 имеют вид
lg  (Па) = 12,767 – 11549/Т (1093 – 1193 K);
(Па) = 12,767 – 11549/Т (1093 – 1193 K);
lg  (Па) = 11,942 – 10579/Т (1203 – 1323 K).
(Па) = 11,942 – 10579/Т (1203 – 1323 K).
Система Sr–C. В системе Sr–C образуется термодинамически прочный карбид SrC2 (∆Н  = –81,43 кДж/моль, S
= –81,43 кДж/моль, S  = 75,5 Дж/(моль×K). Изменение энергии Гиббса реакций образования карбида с участием стронция в различном агрегатном состоянии в зависимости от температуры описывается уравнениями (в Дж/моль):
= 75,5 Дж/(моль×K). Изменение энергии Гиббса реакций образования карбида с участием стронция в различном агрегатном состоянии в зависимости от температуры описывается уравнениями (в Дж/моль):
Srт + 2Cт = SrC2(т); ∆G 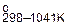 = –81646 – 7,45Т;
= –81646 – 7,45Т;
Srж + 2Cт = SrC2(т); ∆G  = –87927 – 5,27Т;
= –87927 – 5,27Т;
Srг + 2Cт = SrC2(т); ∆G 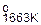 = –221752 + 76,55Т.
= –221752 + 76,55Т.
Давление паров стронция над карбидом SrC2 в зависимости от температуры представлено уравнением
lgPSr(ат) =  + 3,74 (1200 – 1500 K).
+ 3,74 (1200 – 1500 K).
Система Sr–Si (рис. 18.6). В системе Sr–Si образуются силициды SrSi (75,77% Sr, 24,23% Si) и SrSi2 (61,01% Sr, 38,99% Si). Силициды SrSi и SrSi2 плавятся конгруэнтно при 1140 и 1150°С соответственно. В системе имеются три эвтектики с температурами ~ 700, 1044 и 1000°С. Сообщается также о существовании соединения Sr2Si.
Рис. 18.6.Диаграмма равновесного состояния системы Sr–Si
Система SrO–SiO2 (рис. 18.7). В системе существуют кристаллические фазы (силикаты) 2SrO×SiO2, SrO×SiO2. Температура плавления 2SrO×SiO2 точно не установлена, но она выше 1700°С. Соединение SrO×SiO2 плавится конгруэнтно при 1580°С. Наиболее низкая эвтектическая температура 1358°С. Силикаты стронция характеризуются сравнительно высокой термодинамической прочностью, что подтверждается приведенным ниже изменением энергии Гиббса реакций их образования из компонентов, Дж/моль:
SrO + SiO2 = SrO×SiO2; ∆G  = –148049 + 7,86T;
= –148049 + 7,86T;
2SrO + SiO2 = 2SrO×SiO2; ∆G  = –214347 + 38,91T;
= –214347 + 38,91T;
3SrO + SiO2 = 3SrO×SiO2; ∆G  = –246686 + 49541T.
= –246686 + 49541T.
Рис. 18.7.Диаграмма равновесного состояния системы SrO–SiO2
Система SrO–Al2O3 (рис. 18.8). В этой системе установлено существование соединений 4SrO×Al2O3, 3SrO×Al2O3 (tпл = 1660°С), SrO×Al2O3 (tпл = 1790°С), SrO×2Al2O3 (tпл = 1820°С) и SrO×6Al2O3 (tпл = 1900°С). Соединение 4SrO×Al2O3 имеет две модификации: высокотемпературную (a-4SrO×Al2O3), устойчивую в области 1320–1690°С, и низкотемпературную (b-4SrO×Al2O3), устойчивую в области 1125–1320°С. Наиболее низкая эвтектическая температура 1505°С.
Сводные термодинамические свойства ряда соединений стронция обобщены в табл. 18.3
Таблица 18.3. Физико-химические свойства некоторых соединений стронция
| Соеди- нения | –∆Н  ,
кДж
моль ,
кДж
моль
| –∆G  ,
кДж
моль ,
кДж
моль
| S  ,
Дж
(моль×К) ,
Дж
(моль×К)
| CP  ,
Дж
(моль×К) ,
Дж
(моль×К)
| Тпл, K |
| SrО | 590,5 | 559,3 | 55,44 | 45,0 | |
| Продолжение табл. 18.3 | |||||
| SrSO4 | 1443,5 | 1345,5 | 117,8 | 101,6 | |
| Sr3P2 | 693,9 | – | – | – | – |
| SrCO3 | 1224,3 | 1143,2 | 99,48 | 81,5 | – |
| SrSi | 188,1 | – | – | – | |
| SrSi2 | 188,1 | – | – | – | |
| Sr2Si | 380,8 | – | – | – | – |
| SrSiO3 | 1629,4 | 1544,1 | 96,3 | 88,4 | – |
| Sr2SiO4 | 2297,7 | 2182,4 | 153,4 | 134,2 | – |
Рис. 18.8.Диаграмма равновесного состояния системы SrO–Al2O3
Минералы и руды стронция. Содержание стронция в земной коре 3,4×10-2% (по массе), в свободном виде не встречается. Стронций образует около 40 минералов, из которых промышленные значения имеют целестин* SrSO4 и стронцианит** SrCO3. Стронций присутствует в качестве изоморфной примеси в различных магниевых, кальциевых (Sr, Ca)2 B14O23×8H2O и бариевых минералах, а также содержится в природных минерализованных видах (около 24% общих запасов стронция).
Часть стронция в океане концентрируется в железомар-
_________________________
* Целестин – Coelestin, Zolesbin - от латинского целестис – небесноголубой, плотность 3,9–4,0 г/см3, твердость 3–3,5, растворяется в Н2SO4.
** Стронцианит Strontianit – название по местности обнаружения ромбической сингонии, изотипен с арагонитом СаСО3, плотность 3,68–3,75, твердость 3,5 в кислотах легко растворяется
ганцевых конкрециях. На основании обобщения многочисленных данных исследований химического состава океанических железомарганцевых отложений выявлена положительная корреляция стронция и других элементов (Ni, Cu, Co, Vo, W, Ba) к марганцевым фазам конкреций, а Ti, V, Cr, Al, Pb, Y и Si – к железосодержащим фазам.
Технология выплавки ферросиликостронция. Стронций присутствует в природных минеральных образованиях в основном в виде целестина SrSO4. Целестиновый концентрат содержит около 86% SrSO4. При высокотемпературном взаимодействии сульфата SrSO4 c углеродом образуются сульфид SrS и СО (в Дж/моль):
SrSO4 + 4С = SrS + 4СО; ∆G  = 517371 – 700,95Т.
= 517371 – 700,95Т.
В присутствии SiO2 восстановление стронция до силицида протекает по реакции (в Дж/моль):
SrSO4 + 4С + SiO2 = SrSi + SO2 + 4СО;
∆G  = 993109 – 820,19Т.
= 993109 – 820,19Т.
Наряду с силицидной фазой при недостатке углерода в системе протекают реакции с образованием силикатов стронция (в Дж/моль):
SrSO4 +  SiO2 + С =
SiO2 + С =  (2SrО∙SiO2) + СО + SO2;
(2SrО∙SiO2) + СО + SO2;
∆G  = 127458 – 197,57Т.
= 127458 – 197,57Т.
Ферросиликоцирконий получали в дуговой электропечи мощностью 160 кВ∙А при напряжении 30 В и токе 1500 А. Шихта состояла из целестинового концентрата, кварцита, коксика и железной стружки. Полученный ферросиликостронций содержал 8-10% Sr, 48–59% Si, остальное – железо. Кратность шлака равнялась 1,5. В опытных кампаниях по выплавке ферросиликостронция в крупнолабораторной печи удельный расход электроэнергии был высоким, а полезное использование стронция низким. Совершенствование технологии выплавки ферросиликостронция приведет к снижению расхода электроэнергии.
Для получения комплексного сплава стронция с барием, а также прямого легирования стали и сплавов Sr и Ва, рационально использовать концентраты, содержащие карбонаты SrCO3 и ВаСО3. Концентрат* марки БСК-2 крупно-
___________________________
* Концентрат предлагает НПФ «Сосновинвест – Иркутск» (Электрометаллургия, 2004. - № 10)
стью до 10 мм имеет следующий химический состав, %:
| SrO | BaO | CaO | SiO2 | MgO | K2O | Na2O | FeO | CO2 |
| 5,5 | 16,0 | 21,5 | 24,8 | 0,9 | 3,0 | 1,5 | 4,0 | 18,0 |
|
из
5.00
|
Обсуждение в статье: Электрометаллургия ферросиликостронция |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

