 |
Главная |
Экзаменационные задания
|
из
5.00
|
1. B 24 № 39. Масса воды, которую надо добавить к 20 г раствора уксусной кислоты с массовой долей 70% для получения раствора уксусной кислоты с массовой долей 5% равна
1) 240 г
2) 250 г
3) 260 г
4) 280 г
Пояснение.
При разбавлении раствора масса самой уксусной кислоты не изменяется.


 , где х - масса добавленной воды
, где х - масса добавленной воды


2. B 24 № 181. Масса нитрата калия, которую следует растворить в 150 г раствора с массовой долей 10% для получения раствора с массовой долей 12%, равна (с точностью до десятых)
1) 3,0 г
2) 3,2 г
3) 3,4 г
4) 3,6 г
Пояснение.
Масса соли в этом процессе не изменяется, она только распределяется между раствором и твердой солью
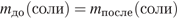
 , где х - масса растворяемого нитрата калия
, где х - масса растворяемого нитрата калия


ответ просят указать с точностью до десятых, поэтому

3. B 24 № 2362. К 110 г раствора с массовой долей хлорида магния 10% добавили 21 мл воды и 21 г этой же соли. Массовая доля соли в полученном растворе равна __________%. (Запишите число с точностью до целых.)
1) 14
2) 10
3) 21
4) 32
Пояснение.
ω=m(вещества)/m(раствора)
Найдем массу вещества m= 110*ω + 21=32 г
Найдем массу раствора m=m(начальное) + m(добавленное)=110 + 21 + 21=152 г
ω(конечная)=32*100/152=21%
4. B 24 № 2448. К 100 г раствора с массовой долей хлорида натрия 15% добавили 35 мл воды и 25 г этой же соли. Массовая доля соли в полученном растворе равна ___________%. (Запишите число с точностью до целых.)
1) 20
2) 13
3) 25
4) 12
Пояснение.
ω=m(вещества)/m(раствора)
Найдем массу вещества m= 100*ω + 25=40 г
Найдем массу раствора m =m(начальное) + m(добавленное)=100 + 35 + 25 = 160 г
ω(конечная)=40*100/160=25%
5. B 24 № 2577. Смешали 70 г раствора с массовой долей нитрата натрия 30% и 130 г раствора этой же соли с массовой долей 20%. Массовая доля соли в полученном растворе равна ___________%. (Запишите число с точностью до десятых.)
1) 23,5
2) 44
3) 31,5
4) 45,5
Пояснение.
ω=m(вещества)/m(раствора)
Найдем массу вещества m= 70*0,3 + 130*0,2=47 г
Найдем массу раствора m =m(начальное) + m(добавленное)=70 + 130 = 200 г
ω(конечная)=47*100/200=23,5%
6. B 24 № 2620. К 150 г раствора с массовой долей нитрата магния 10% добавили 15 г этой же соли и выпарили 45 мл воды. Массовая доля соли в полученном растворе равна ___________ %. (Запишите число с точностью до целых.)
1) 20
2) 24
3) 25
4) 15
Пояснение.
ω=m(вещества)/m(раствора)
Найдем массу вещества m= 150*ω + 15=30 г
Найдем массу раствора m =m(начальное) + m(добавленное)=150 + 15 -45 = 120 г
ω(конечная)=30*100/120=25%
7. B 24 № 2663. К 70 г раствора с массовой долей хлорида кальция 40% добавили 18 мл воды и 12 г этой же соли. Массовая доля соли в полученном растворе равна ____________%. (Запишите число с точностью до целых.)
1) 30
2) 15
3) 23
4) 40
Пояснение.
ω=m(вещества)/m(раствора)
Найдем массу вещества m= 70*ω + 12=40 г
Найдем массу раствора m =m(начальное) + m(добавленное)=70 + 18 + 12 = 100 г
ω(конечная)=40*100/100=40%
8. B 24 № 2706. Смешали 60 г раствора с массовой долей нитрата кальция 15% и 80 г раствора этой же соли с массовой долей 25%. Массовая доля соли в полученном растворе равна __________%. (Запишите число с точностью до десятых.)
1) 20,7
2) 41,4
3) 50,0
4) 100,0
Пояснение.
ω=m(вещества)/m(раствора)
Найдем массу вещества m= 60*0,15 + 80*0,25=29 г
Найдем массу раствора m =m(начальное) + m(добавленное)=60 + 80= 140 г
ω(конечная)=29*100/140=20,7%
9. B 24 № 3050. К 140 г раствора с массовой долей хлорида натрия 15% добавили 20 мл воды и 19 г этой же соли. Массовая доля соли в полученном растворе равна __________%. (Запишите число с точностью до целых.)
1) 54
2) 31
3) 44
4) 22
Пояснение.
ω=m(вещества)/m(раствора)
Найдем массу вещества m= 140*ω + 19=40 г
Найдем массу раствора m =m(начальное) + m(добавленное)=140 + 20 + 19 = 179 г
ω(конечная)=40*100/179=22%
10. B 24 № 3093. К 90 г раствора с массовой долей хлорида магния 10% добавили 40 мл воды и 21 г этой же соли. Массовая доля соли в полученном растворе равна ____________%. (Запишите число с точностью до целых.)
1) 42
2) 55
3) 30
4) 20
Пояснение.
ω=m(вещества)/m(раствора)
Найдем массу вещества m= 90*ω + 21=30 г
Найдем массу раствора m =m(начальное) + m(добавленное)=90 + 40 + 21 = 151 г
ω(конечная)=30*100/151=20%
11. B 24 № 3265. Смешали 80 г раствора с массовой долей нитрата натрия 25% и 20 г раствора этой же соли с массовой долей 40%. Массовая доля соли в полученном растворе равна __________%. (Запишите число с точностью до целых.)
1) 33
2) 28
3) 12
4) 36
Пояснение.
ω=m(вещества)/m(раствора)
Найдем массу вещества m= 80*0,25 + 20*0,4=28 г
Найдем массу раствора m =m(начальное) + m(добавленное)= 80 + 20 = 100 г
ω(конечная)=28*100/100=28%
12. B 24 № 3297. Масса нитрата калия, которую следует растворить в 150 г раствора с массовой долей этой соли 10% для получения раствора с массовой долей 12%, равна
1) 0,3 г
2) 2,0 г
3) 3,0 г
4) 3,4 г
Пояснение.
массовая доля = m(вещества)*100/m(суммарное)
Обозначив добавляемое количество нитрата калия за х, получим:
12=(150*0,1+х)*100/(150+х)
х=3,4 г
|
из
5.00
|
Обсуждение в статье: Экзаменационные задания |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

