 |
Главная |
Реакции боковых цепей в алкилбензолах
|
из
5.00
|
ЛЕКЦИЯ 15
Алкилбензолы
Получение алкилбензолов
Алкилирование.В результате этой реакции в бензольное кольцо вводятся алкильные группы с образованием гомологов из бензола. В качестве алкилирующих агентов можно использовать галогеналканы, алкены и спирты. Алкилирование по Ф-К осуществляется при действии на арены галогеналканов в присутствии кислот Льюиса в качестве катализаторов:

Рис. 15.1. Реакция алкилирования бензола галогеналканами
Катализатор – кислота Льюиса поляризует связь углерод-галоген, увеличивая электрофильность реагента:

Рис. 15.2. Схема активации электрофильного агента кислотой Льюиса
Реакция протекает мо механизму реакций электрофильного замещения:

Рис. 15.3. Схема реакции алкилирования бензола этилбромидом
Реакция алкилирования имеет ряд ограничений.
Во-первых, алкилирование по Ф-К обратимо, и наряду с прямой реакцией протекает и обратная реакция дезалкилирования (деалкилирования). Схема деалкилирования ароматических углеводородов показана на примере изопропилбензола:
- вначале протон присоединяется к молекуле изопропилбензола с образованием карб-катиона;
- затем карбкатион подвергается расщеплению по β-правилу и образует молекулу бензола и изопропил-ион. Этот карбкатион, встречаясь с новой молекулой изопропилбензола, образует карб-катион и выделяет пропилен.

Рис. 15.4. Схема реакции дезалкилирования изопропилбензола
Во-вторых, недостаток метода алкилирования по Фриделю-Крафтсу связан с изомеризацией алкилирующего агента в ходе реакции, в результате чего образуется смесь изомерных продуктов алкилирования.
Классическим примером является алкилирование бензола н-пропилхлоридом, где получается смесь н-пропил- и изопропилбензола, в которой изомеризованный продукт является доминирующим:

Рис. 15.5. Реакция изомеризации продуктов алкилирования бензола
В третьих; алкилирующие реагенты действуют менее избирательно, чем другие электрофилы, особенно при высокой температуре. Так, алкилирование толуола метилхлоридом при 0ºС приводит в основном к получению о- и н-ксилолов, а при повышенной температуре преимущественно образуется м-ксилол. При нагревании о- и н-ксилолы превращаются в м-изомер:

Рис. 15.6. Реакция алкилирования толуола метилхлоридом
???? В присутствии катализаторов кислотной природы удается осуществить диспропорционирование толуола до бензола и смеси орто-, пара- и мета-ксилолов, которую разделяют перегонкой.
Формилирование аренов по Гаттерману-Коху.Посредством этой реакции в ароматическое кольцо вводится альдегидная группа.
Реакция формилирования осуществляется смесью оксида углерода (II) и хлорводорода в присутствии хлорида алюминия. При взаимодействии хлорводорода и оксида углерода (II) образуется формилхлорид, из которого в комплексе с хлоридом алюминия генерируется электрофил [H-C=O]+:


Рис. 15.7. Формилирование аренов по Гаттерману-Коху
Ацилирование аренов по Фриделю-Крафтсу. Реакция ацилирования – важнейший метод синтеза ароматических кетонов путем замещения атома водорода на ацильную группу. В качестве ацилирующих реагентов чаще всего используются хлорангидриды или ангидриды кислот:
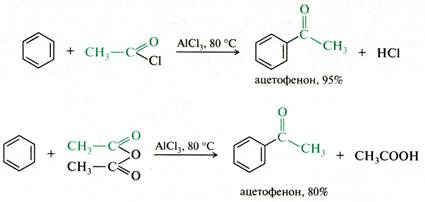
Рис. 15.7. Ацилирование бензола хлорангидридом и ангидридом кислоты
Алкилирование по Ф-К осуществляется с участием катализаторов – кислот Льюиса.
Реакцию проводят в малополярных органических растворителях: сероуглероде, нитробензоле, тетрахлорметане.
Образование электрофильного реагента протекает по следующей реакции:
- координация хлорангидрида с хлоридом алюминия с образованием комплекса с катализатором по карбонильному атому кислорода;
- ионизация комплекса с образованием ацил-катиона, который и является электрофильным агентом:

Рис. 15.8. Активация электрофильного реагента – хлорангидрида кислотой Льюиса
Для ангидрида карбоновой кислоты:

Рис. 15.9. Активация электрофильного реагента – ангидрида карбоновой кислоты кислотой Льюиса
В целом реакция ацилирования протекает по общему механизму электрофильного замещения в ароматическом ядре:

Рис. 15.10. Схема реакции ацилирования бензола хлорангидридом
Получающийся в результате реакции ароматический кетон образует комплекс с хлоридом алюминия. Для получения конечного продукта, комплекс разлагают хлороводородной кислотой со льдом.
Реакция ацилирования лишена тех недостатков, которые характерны для реакции алкилирования. Вводимая в кольцо карбонильная группа является электронакцептором, она дезактивирует кольцо, и последующего ацилирования не происходит. Поэтому ацилирование с последующим восстановлением карбонильной группы можно использовать для введения одной алкильной группы.
Кроме того, поскольку посредством реакции алкилирования невозможно ввести в кольцо алкильный заместитель с тремя и более атомами углерода с неразветвлённым углеродным скелетом, то ацилирование с последующим восстановлением позволяет решить эту задачу:

Рис. 15.11. Реакция ацилирования бензола пропионилхлоридом
Реакции боковых цепей в алкилбензолах
Наряду с реакциями замещения в ароматическом ядре для алкилбезолов характерны реакции, затрагивающие боковую цепь. Среди них наиболее важны реакции галогенирования и окисления.
|
из
5.00
|
Обсуждение в статье: Реакции боковых цепей в алкилбензолах |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

