 |
Главная |
Описание экспериментальной установки
|
из
5.00
|
Установка для изучения технологических параметров процессов реагентного осаждения представлена на рисунке 2. Через трансформатор 1, проводится регулирование напряжение, подаваемого на нагревательную плитку 2. На плитку устанавливается колба 3, в которую помещается раствор для осаждения. В раствор погружен термометр 4 для контроля за температурой осаждения. Раствор перемешивается с помощью мешалки 5. Мешалка приводится в движение двигателем 6. Частота оборотов мешалки изменяется при помощи лабораторного автотрансформатора 7. Раствор осаждающего реагента приливается из бюретки 8.
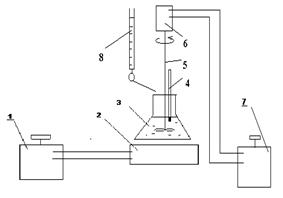
Рисунок 2 Экспериментальная установка для изучения технологических параметров процессов реагентного осаждения
Порядок выполнения работы.
- Приготовить 100 мл раствора сульфата меди с различной концентрацией 1, 5, 10, 20, 50, 100, 200, 250, 300, 350, 400, грамм соли на литр. Поместить раствор в колбу
Учитывать, что растворимость сульфата меди сильно зависит от температуры. Данные о растворимости представлены в таблице 2.
Таблица 2
Растворимость сульфата меди при различных температурах
| Растворимость, г/л | ||||||||||
| Температура, 0С |
- Рассчитать какой объем насыщенного раствора NaOH потребуется для осаждения всей меди из раствора в виде гидрооксида меди. Приготовить насыщенный раствор NaOH и залить его в бюретку. К раствору сульфата меди по каплям прибавлять из бюретки насыщенный раствор гидрооксида натрия. Включить мешалку, поддерживать температуру, указанную преподавателем.
- К раствору сульфата прилить не сразу весь объем щелочи, а некоторую его часть, по указанию преподавателя.
- После того как сформировался осадок, отфильтровать пульпу через вакуумный фильтр. Оставшийся в колбе осадок смыть на фильтр маточным раствором.
- Высушить, взвесить осадок и сдать его для анализа на содержание меди. Полученный результат занести в таблицу 3.
- Повторить опыт при различном расходе осаждающего реагента (раствора щелочи), различной концентрации NaOH в осаждающем растворе, различной температуре, при добавке примесных солей, влияющих на ионную силу раствора и степень извлечения меди в осадок, при различной исходной концентрации сульфата меди в растворе. Результаты опытов записывать в таблицу 3.
- Повторить опыт используя нитрат, хлорид и ацетат меди
Таблица 3
Результаты опытов по изучению технологических показателей процесса реагентного осаждения меди из раствора сульфата меди.
| С Н2SO4, % | Объем раствора NaOH | Масса | Т, 0С | Активность | m | ПР | Степень извлечения Cu в осадок | ||||
| Стехиом. | Факт. | осадка | Cu в осадке | Cu2+ | ОН- | факт. | теор. | ||||
4. Обработка экспериментальных данных, содержание отчета
- Рассчитать согласно стехиометрии реакции расход гидрооксида натрия на осаждение ионов меди из раствора сульфата меди.
CuSO4 + 2 NaOH = Cu(OH)2 + Na2SO4
NaOH = 2 * MCuSO4 * MrNaOH / MrCuSO4
- Рассчитать объем раствора щелочи по формуле:
V NaOH = NaOH / CNaOH, (9)
где: V NaOH - объем раствора щелочи
CNaOH - концентрация раствора щелочи (задается преподавателем или принимается как для насыщенного раствора при данной температуре – 1000-1100 грамм / литр)
- Рассчитать фактическую степень извлечения меди в осадок по формуле:
Хфакт = Мосадка * [Cu, %]осадка * MrCuSO4 / МCuSO4 * ArCu (10)
- Рассчитать концентрацию ионов меди в маточном растворе как корень квадратный из произведения растворимости. ПР Cu(OH)2 = 2,2*10-20
- Рассчитать теоретическую степень извлечения меди, без учета ионной силы раствора, как описано в примере 3.
- Найти отношение объема фактически прилитого раствора щелочи к стехиометрическому объему.
- Построить график зависимости фактической степени извлечения меди в осадок от, найденного выше, отношения для различных температур, исходных концентраций сульфата меди и щелочи в осадителе, и различных исходных солей меди – нитрата, хлорида, ацетата и т.д.
- Используя математический пакет корреляционно-регрессионного анализа построить математическую модель процесса реагентного осаждения ионов меди как зависимость вида Х CuSO4 = f (Vфакт / Vстехиометр, С Н2SO4, температура, CNaOH)
- Дополнительно рассчитайте ионную силу раствора, коэффициенты активности Cu2+ , ОН- и ПР с учетом коэффициентов активности по формулам 6, 7, 8 и данным таблицы 1. С учетом изменившегося ПР рассчитать теоретическую степень извлечения меди в осадок. Расчет вести исходя из стехиометрического расхода щелочи на связывание ионов меди.
- Сделать выводы по проведенной работе и предложить технологические параметры процесса осаждения меди из раствора
Контрольные вопросы:
- Опишите общую схему процессов осаждения – выщелачивания
- Объясните природу процессов, сопровождающих явления растворения – осаждения
- Как описывается скорость процессов растворения – осаждения ?
- Что такое произведение растворимости (ПР) ? Как выводится формула для расчета ПР ?
- Как рассчитать концентрацию насыщенного раствора соли, зная произведение растворимости ?
- Как опытным путем определить ПР ?
- Как рассчитать теоретическое значение степени извлечения иона в осадок, зная ПР ?
- Как рассчитать концентрацию насыщенного раствора соли, зная ПР ?
- Что такое ионная сила раствора ? Закон Льюиса ?
- Закон Дебая-Хюккеля ?
- Что такое цементация ?
- Какие были сделаны выводы по работе и предложены технологические параметры процесса осаждения ?
|
из
5.00
|
Обсуждение в статье: Описание экспериментальной установки |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

