 |
Главная |
Примеры лабораторных опытов при формировании первоначальных химических понятий
|
из
5.00
|
Опыт 1. Изучение физических свойств веществ.
Оборудование и реактивы: пробирки (6 шт.), стеклянная палочка; образцы веществ: медь (проволока), сера, дистиллированная вода, нашатырный спирт, поваренная соль, мел. Варианты: поваренная соль и алюминий; вода и железо; медь и сера; уксус и растительное масло.
План изучения свойств вещества:
а) Агрегатное состояние вещества при комнатной температуре.
б) Цвет, блеск.
в) Запах.
г) Растворимость в воде.
д) Относительная плотность.
Наблюдения занесите в таблицу:
ФИЗИЧЕСКИЕ СВОЙСТВА ВЕЩЕСТВ
| Вещество | Агрегатное состояние | Цвет | Запах | Растворимость в воде |
| Медь | ||||
| Сера | ||||
| Вода | ----- | |||
| Нашатырный спирт | ----- | |||
| Поваренная соль | ||||
| Мел |
Опыт 2. Сравнение физических свойств веществ.
Оборудование и реактивы: пробирки (4 шт.), стеклянная палочка; образцы веществ: дистиллированная вода, нашатырный спирт, поваренная соль, мел.
Результаты занесите в таблицу:
СРАВНЕНИЕ ФИЗИЧЕСКИХ СВОЙСТВ ВЕЩЕСТВ
| Свойства | Мел | Поваренная соль | Вода | Нашатырный спирт | |
| Сходство | Агрегатное состояние | ||||
| Цвет | |||||
| Запах | |||||
| Растворимость в воде | --- | ||||
| Различия | Агрегатное состояние | ||||
| Цвет | |||||
| Запах | |||||
| Растворимость в воде | --- |
Опыт 3. Разделение смеси веществ:
а) Дана смесь речного песка и древесных опилок. Разделите ее. Какие свойства песка и древесины вы используете для их разделения?
б) Дана смесь железных опилок и порошка древесного угля. Выделите из смеси железо двумя способами.
в) Имеется смесь поваренной соли и речного песка. Выделите из нее песок.
г) Из смеси песка и медного купороса выделите медный купорос.
Опыт 4. Физические и химические явления.
а) Плавление парафина.
б) Прокаливание медной проволоки.
в) Взаимодействие соляной кислоты с мрамором.
г) Взаимодействие соды с уксусной кислотой.
д) Растворение поваренной соли в воде и выпаривание раствора.
Тема 9. Периодический закон, Периодическая система химических элементов, строение атома и строение вещества в школьном курсе химии.
Изучив тему, вы должны
ЗНАТЬ:
· образовательные, воспитывающие и развивающие функции темы;
· историю определения места темы в школьном курсе химии и ее структуру;
· методические подходы к изучению темы;
· систему опорных знаний и подготовку учащихся к пониманию сущности периодичности;
· объем сведений по строению атома и химической связи;
· структуру системы теоретических знаний о строении вещества, последовательность развития понятий.
УМЕТЬ:
· использовать комплекс наглядных средств при изучении темы;
· устанавливать и показывать причинно-следственные связи между строением и свойствами веществ, выявлять на их основе учебные проблемы и использовать проблемное обучение;
· формировать умения школьников пользоваться Периодической системой;
· обучать школьников научному прогнозированию на материале темы;
· осуществлять контроль результатов обучения по теме;
· планировать, моделировать и проводить уроки по теме в школе.
Задания для подготовки к занятию (входной контроль):
1) Каковы существенные особенности содержательного наполнения темы?
2) Обоснуйте место изучения ПЗ в школьном курсе химии.
3) Какие опорные знания необходимы для изучения ПЗ, ПСХЭ, где и когда они вводятся?
4) Охарактеризуйте методические подходы к изучению ПЗ и строения атома. Каковы их преимущества и недостатки?
5) Раскройте образовательный аспект темы.
6) Воспитывающая и развивающая функции изучения темы.
7) Приведите примеры разных вариантов средств наглядности при изучении теории строения атома, химической связи и строения вещества.
8) Какие новые стороны понятий о веществе, химической реакции, химическом элементе раскрываются в теме ПЗ и ПСХЭ?
9) Каково место и значение обобщения знаний учащихся в процессе изучения химической связи и структуры вещества?
10) Какие опорные знания необходимы учащимся для усвоения понятия о периодичности?
11) Какие опорные понятия необходимы для изучения понятия степени окисления? Обоснуйте место введения этого понятия в курсе химии. Какие сведения из курса физики используются для этого?
12) Какие опорные знания необходимы для понимания природы ковалентной связи?
13) Какие модели могут быть использованы для понимания химической связи и строения кристаллических решеток?
14) Тема бедна экспериментом. Попытайтесь подобрать к ней опыты.
Литература:
1. Чернобельская Г.М. Методика обучения химии в средней школе.- М.: Владос, 2000, с. 220-233.
Подготовка сообщений:
1) "Обзор дополнительной методической литературы по теме"
2) "Варианты массовых внеклассных мероприятий по теме"
Задания для самостоятельного выполнения:
1. Сделайте методический анализ темы.
2. Изучите химическую, методическую, научно-популярную литературу по теме.
3. Изучите имеющиеся средства обучения по теме. Предложите варианты их применения.
4. Составьте вопросы-задания для учащихся при работе с карточками химических элементов.
5. Составьте план характеристики элемента на основе его положения в ПС.
6. Разработайте алгоритм составления электронной конфигурации атома.
7. Разработайте тематику докладов учащихся, посвященных ПЗ. Где и когда они могут быть сделаны? Подберите литературу и иные источники информации для них.
8. Проанализируйте содержание средств наглядности, имеющихся в кабинете по данной теме (карточки химических элементов, школьные таблицы). Умейте озвучивать изображения, комментировать содержание.
9. Составьте блиц-опрос на знания закономерностей ПС.
10. Составьте блиц-опрос на знания электронных конфигураций атомов.
11. Составьте не менее 10 тестовых заданий на знания строения атома.
12. Подберите и придумайте познавательные задания в игровой форме по теме.
13. Составьте химический диктант по одному из вопросов темы.
14. Составьте четыре варианта заданий для проведения 20-минутной самостоятельной работы при изучении химической связи.
15. Раскройте систему учебных проблем (предложите формулировки учебных проблем), решаемых на материале темы ПЗ и ПСХЭ.
16. Разработайте систему заданий для школьников по работе с учебником.
17. Предложите различные варианты определения степени окисления в соединениях.
18. Составьте серию познавательных заданий для школьников: а) на объяснение свойств веществ; б) на прогнозирование свойств соединений.
19. Пользуясь программой и учебником, проанализируйте предложенный химический эксперимент в данной теме. Как его можно расширить? Приведите примеры и обоснуйте их (Приложение 1).
20. На нескольких примерах раскройте взаимосвязь состава, строения и свойств веществ.
21. Составьте план-конспект урока на тему "Типы кристаллических решеток". Приведите пример объяснения учителя в сочетании со средствами наглядности.
22. Разработайте конспект урока по обобщению знаний школьников о ПЗ, химической связи и структуре вещества.
23. Создайте фрагменты презентаций, содержащих динамические эффекты: образование химической связи, превращение нейтрального атома в ион, определение типа химической связи по разнице в электроотрицательностях и пр.
24. Предложите варианты проведения массовых внеклассных мероприятий с учащимися по творчеству Д.И.Менделеева и Периодическому закону.
Приложение 1
Химический эксперимент по теме "Периодический закон и Периодическая система химических элементов Д.И. Менделеева"
Опыты ставят своей целью исследование кислотно-основных свойств гидроксидов элементов и установление закономерностей в изменении свойств высших гидроксидов в периоде и группе.
Опыт 1. Кислотно-основные свойства гидроксидов элементов 3-го периода
а) Свойства гидроксида магния
Получите гидроксид магния реакцией обмена, используя имеющиеся реактивы. Отметьте цвет осадка. Разделите осадок на две части. К одной части прилейте соляную или серную кислоту, к другой части осадка - раствор щелочи. В какой пробирке осадок растворился? Объясните наблюдаемое. Составьте уравнения протекающих реакций. Сделайте вывод, какие свойства (основные, кислотные или амфотерные) проявляет гидроксид магния.
б) Свойства гидроксида алюминия
Получите гидроксид алюминия реакцией обмена, используя имеющиеся на столе реактивы (к раствору соли алюминия добавляйте по каплям раствор щелочи до образования осадка). Отметьте цвет осадка. Разделите осадок на две части. К одной части прилейте соляную или серную кислоту, к другой части осадка - раствор щелочи. Объясните наблюдаемое. Составьте уравнения реакций. Сделайте вывод, какие свойства (основные, амфотерные или кислотные) проявляет гидроксид алюминия. Объясните, почему при получении гидроксида алюминия реакцией обмена раствор щелочи следует приливать к соли, а не наоборот; почему раствор щелочи следует приливать по каплям, избегая избытка.
в) Свойства серной кислоты - гидроксида серы(VI)
Налейте в пробирку 1-2 мл раствора серной кислоты. Добавьте каплю лакмуса. Какой цвет он приобрел? Затем к кислоте по каплям при перемешивании добавляйте раствор щелочи, пока окраска лакмуса не изменится на фиолетовую. Напишите уравнение реакции между кислотой и щелочью. Как называется эта реакция? Сделайте вывод о свойствах серной кислоты.
Запишите формулы изученных гидроксидов в горизонтальный ряд и сделайте вывод, отражающий характер изменения свойств гидроксидов элементов 3-го периода слева направо.
Опыт 2. Свойства гидроксидов элементов главной подгруппы II группы
а) Свойства гидроксида бериллия
Все соединения бериллия токсичны, поэтому соль бериллия целесообразно заменить на соль цинка.
Получите гидроксид цинка реакцией обмена (аналогично получению гидроксида алюминия в опыте 1 б). Отметьте цвет осадка. Разделите осадок на две части. К одной части прилейте соляную или серную кислоту, к другой части осадка - раствор щелочи. Объясните наблюдаемое. Составьте уравнения реакций. Сделайте вывод, какие свойства (основные, амфотерные или кислотные) проявляет гидроксид цинка (бериллия).
б) Свойства гидроксида магния
Воспользуйтесь данными опыта 1 а).
в) Свойства гидроксида кальция
Налейте в пробирку 1-2 мл раствора хлорида или нитрата магния. Добавьте раствор гидроксида кальция (известковую воду). Что наблюдаете? Это доказывает, что гидроксид кальция более сильной основание, чем гидроксид магния. Напишите уравнение реакции.
Расположите формулы изученных гидроксидов в вертикальный ряд (сверху вниз) и сделайте вывод, отражающий характер изменения свойств гидроксидов элементов главной подгруппы II группы по мере возрастания атомных масс.
Тема 10. Методика изучения растворов и основ электролитической диссоциации как одной из теоретических концепций.
Изучив тему, вы должны
ЗНАТЬ:
· место и значение темы в курсе химии;
· систему опорных понятий при изучении электролитической диссоциации;
· взаимосвязь важнейших понятий темы, ее построение;
· методические особенности химического эксперимента по теме.
УМЕТЬ:
· разрабатывать поурочное планирование темы для разных альтернативных и углубленного курсов химии;
· владеть техникой и методикой химического эксперимента по теме;
· применять учебное оборудование, средства наглядности по теме;
· планировать, моделировать и проводить уроки по теме;
· подготавливать и проводить практические занятия разных видов по теме;
· контролировать и оценивать результаты обучения школьников.
Задания для подготовки к занятию (входной контроль):
1) Место и значение темы "Растворы. Электролитическая диссоциация" в школьном курсе химии.
2) Содержание темы: базовые понятия, взаимосвязь между ними.
3) Методические подходы к изучению процессов диссоциации, их достоинства и недостатки.
4) Необходимые теоретические знания школьников, приступающих к изучению темы.
5) Методика изучения основ теории электролитической диссоциации.
6) Развитие и обобщение знаний учащихся о кислотах, основаниях и солях на основе теории электролитов.
7) Химический эксперимент в теме, его разновидности, техника и методика.
8) Процессы гидролиза солей как объективно сложные в курсе химии.
Литература:
1. Чернобельская Г.М. Методика обучения химии в средней школе.- М.: Владос, 2000, с. 233-239.
Задания для самостоятельного выполнения:
1. Осуществите методический анализ темы.
2. Изучите методическую литературу по теме.
3. Проанализируйте программу и учебник, определите требования к изучению темы.
4. Разработайте поурочное планирование темы для разных альтернативных и углубленного курсов химии.
5. Познакомьтесь с определениями основных понятий. Сравните определения кислот, оснований и солей с разных теоретических позиций.
6. Озвучьте рисунки школьного учебника и таблицы, имеющиеся в кабинете, посвященные механизмам электролитической диссоциации.
7. Подготовьте вопросы для устного фронтального опроса учащихся по теме "Электролиты и неэлектролиты".
8. Продумайте варианты домашних заданий для школьников, направленных на повторение базовых понятий перед изучением ТЭД.
9. Ознакомьтесь с опорными конспектами по теме, умейте их озвучивать.
10. Составьте два варианта заданий для проведения контрольной работы по теме, обоснуйте их.
11. Пользуясь программой и учебниками, отберите все сведения о растворах, которые учащиеся получают в средней школе.
12. Составьте комплекты заданий репродуктивного, продуктивного и творческого уровней для закрепления знаний по теме.
13. Проанализируйте типы экспериментальных задач по теме, представленные в школьном учебнике. Разработайте четыре варианта экспериментальных задач по теме для проведения практической работы.
14. Освойте технику и методику работы с учебным оборудованием, а также технику химического эксперимента по теме.
15. Проанализируйте технику опытов, свидетельствующих о том, что растворение - сложный физико-химический процесс (Приложение 1). Предложите методику их включения в урок.
Экспериментальная часть:
Опыт 1. Испытание веществ и их растворов на электропроводность.
Для проведения опыта используются как самодельные, так и заводские приборы (Рис. 1). Чаще всего они представляют собой лампочки с разомкнутой цепью. При замыкании цепи проводником I рода (металлическим) или II рода (раствором электролита) лампочка загорается; либо устройство, включенное в цепь, показывает прохождение электрического тока.
а)  б)
б)  в)
в) 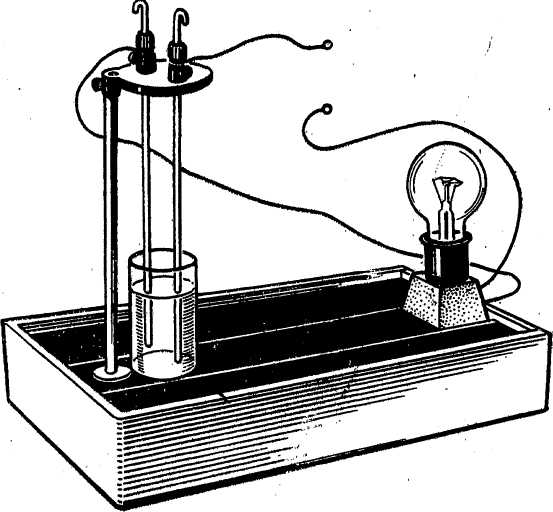
Рис. 1. Приборы для испытания электрической проводимости веществ: а), б) - самодельные приборы; в) - прибор Черняка.
Как правило, перед исследованием веществ и их растворов на электропроводность убеждаются, что прибор действует. Для этого при выключенном штепселе замыкают место разрыва цепи кусочком металла (зачищенной металлической частью держателя для пробирок, не касаясь руками при этом металлической части!). Включают прибор в сеть. Убеждаются, что лампочка горит.
С помощью прибора исследуют на электропроводность вещества различных классов и их растворы.
Для испытания целесообразно взять: гидроксид натрия, хлорид натрия, глюкозу, уксусную кислоту, воду.
Последовательность работы с веществами.
Сначала рассматривают состояние анализируемых веществ при обычных условиях, обсуждают тип связи у этих веществ. Наблюдения, соображения оформляют в виде таблицы (Табл. 1). Далее испытывают электропроводность взятых веществ. Действия с веществами, показания прибора во время испытания, выводы (имеют ли вещества с данным типом связи в безводном состоянии подвижно заряженные частицы) на основе наблюдений записывают в таблицу.
Затем приливают воду, получают растворы. Испытывают электропроводность водных растворов веществ. Результаты и выводы (каким типом связи должно обладать вещество, чтобы раствор его имел подвижные ионы; какой процесс должен произойти с узлом кристалла этого вещества, чтобы подвижные ионы возникли; какова роль воды в этом) оформляют в таблице.
Таблица 1
Испытание электропроводности веществ
| Формулы испытуемых веществ | NаОН | NaCI | С6Н12О6 | СН3СООН | Н2О |
| Агрегатное состояние веществ | |||||
| Тип связи в соединениях | |||||
| Показания прибора | |||||
| Вывод 1. | |||||
| Добавление воды | |||||
| Показания прибора | |||||
| Вывод 2. |
Техника опыта. До начала эксперимента подбирают 6 сухих стаканов и один прибор. Стаканы этикетируют. Насыпают и наливают вещества в таком количестве, чтобы было прикрыто дно стакана. Воды наливают больше половины стакана. После каждого испытания, вынув штепсель из розетки, очищают разомкнутые концы электродов (проводов) от сухих веществ тряпочкой или бумагой. После каждого испытания жидкости или растворов, вынув штепсель из розетки, промывают дистиллированной водой в 6-м стакане.
Для приготовления растворов приливают 10 мл дистиллированной воды (из последнего стакана) в каждый стакан с веществом.
По окончании опыта каждое вещество сливают в склянку с той же этикеткой, стоящей под тягой. Разомкнутые концы приборов как следует осушают и очищают.
Опыт 2. Зависимость электропроводности уксусной кислоты от концентрации.
Для опыта используют прибор - лампочку с разомкнутой цепью.
Техника опыта. На дно химического стакана наливают немного крепкого раствора уксусной кислоты (ледяной). Испытывают жидкость на электропроводность. Фиксируют отсутствие, либо слабый накал лампочки. Разбавляют жидкость дистиллированной водой. Снова испытывают на электропроводность. Наблюдают усиление свечения нити накаливания.
Опыт 3. Опыт по различной силе электролитов.
Для опыта используют прибор - лампочку с разомкнутой цепью.
Техника опыта. Готовят растворы соляной и уксусной кислот одинаковой молярной концентрации (1М, либо 0,1М, либо 0,01М). Наливают в химические стаканы одинакового диаметра примерно равные объемы кислот. Испытывают растворы на электрическую проводимость. О силе электролитов судят по величине накала лампочки.
Опыт 4. Движение ионов при прохождении через раствор постоянного электрического тока.
Опыт проводят с использованием либо самодельного прибора, либо прибора Черняка (Рис. 2).
Техника опыта. На стеклянную пластинку (крышку прибора Черняка) кладут лист фильтровальной бумаги. Бумагу предварительно смачивают раствором электролита с индикатором. Для этого заранее в стакане смешивают 10% раствор хлорида натрия или сульфата натрия с метилоранжем (1) или раствор хлорида натрия с фенолфталеином(2).
Первая смесь используется для обнаружения направленного движения катионов водорода, вторая – для обнаружения движения гидроксид-ионов.
В стакан опускают свернутый рулончиком лист фильтровальной бумаги, увлажняют, придерживая пинцетом, один конец, затем второй.
На противоположные концы бумаги накладывают и плотно прижимают электроды (медные или алюминиевые; можно использовать зажимы «крокодильчики»). Электроды подсоединяют к источнику постоянного тока.
Между электродами, параллельно бумаге, туго натягивают пинцетом толстую нитку, смоченную в фарфоровой чашке соляной кислотой(1) или щелочью(2). Нитку располагают посередине, на равномерном расстоянии от электродов.
Наблюдают в отсутствие тока равномерную диффузию частиц вправо и влево от нитки (равномерное красное окрашивание (1), малиновое (2). Провода включают в сеть постоянного тока. Наблюдают некоторое время. Диффузия становится односторонней.
а)  б)
б) 
Рис. 2. Приборы для демонстрации движения ионов: а) самодельный; б) прибор Черняка.
Опыт 5. Выделение тепла при растворении вещества (с термоскопом)
Описание прибора: Термоскоп состоит из манометрической трубки с красителем и герметично соединенной с ней сухой пробирки. Манометрическая трубка закреплена в лапке штатива. Уровень красителя отмечен резиновым кольцом. Если температура испытуемой среды равна температуре воздуха в пробирке, уровень красителя не меняется. Если температура среды меньше температуры воздуха в пробирке, воздух сжимается, и уровень красителя во внешнем колене уменьшается. Если температура анализируемой среды больше температуры воздуха в пробирке, воздух расширяется, и уровень красителя во внешнем колене манометрической трубки увеличивается.
Техника опыта. Воду объемом 10 мл наливают в узкий химический стакан. 10 мл концентрированной серной кислоты отмеривают мерной пробиркой. Погружают пробирку термоскопа в воду, отмечают уровень красителя. Затем в воду тонкой струйкой, быстро перемешивая, приливают кислоту. Отмечают показания термоскопа во внешнем и внутреннем коленах. После работы все сливают в склянки под тягой.
Опыт 6. Поглощение тепла при растворении (с нитратом аммония)
Оборудование и реактивы. Стакан на 500 мл с палочкой. Демонстрационный термометр. Пробирка. Фанерная дощечка (стеклянная пластинка, металлическая пластинка). Нитрат аммония (кристаллический). Дистиллированная вода.
Техника опыта. Под дно стакана помещают пластинку, заблаговременно смоченную водой. В стакан почти до дна опускают укрепленный в штативе термометр. Отвешивают 120 г нитрата аммония и помещают в стакан так, чтобы шарик термометра был закрыт. Готовят пробирку с небольшим количеством дистиллированной воды (лучше холодной). Затем в стакан вливают 200 мл воды и перемешивают смесь пробиркой с водой. При растворении нитрата аммония в воде температура опускается до –20 0С и ниже. Стакан снаружи покрывается инеем. Смоченная водой пластинка примерзает ко дну стакана, а вода в пробирке замерзает.
Для этого опыта можно брать и другие вещества. Тепловой эффект их растворения смотрите в таблицах:
ПРИМЕРЫ ОХЛАЖДАЮЩИХ СМЕСЕЙ
| Соль | Граммов соли на 100 г воды | Понижение температуры,градусы | Соль | Граммов соли на 100 г воды | Понижение температуры,градусы |
| NaCI | NaNO3 | ||||
| MgSO4 .7H2O | Na2S2O3 .5H2O | ||||
| Na2CO3 .10H2O | KI | 22,5 | |||
| KNO3 | CaCI2 .6H2O | ||||
| NaC2H3O2 .3H2O | NH4SCN | ||||
| NH4CI | KSCN | ||||
| KCI | NH4NO3 |
ОХЛАЖДАЮЩИЕ СМЕСИ
| Соли | Массовые части на 100 г снега | Температура смеси (0С) |
| Хлорид натрия | -21 | |
| Хлорид аммония | -30 | |
| Нитрат натрия | -30 | |
| Хлорид кальция CaCl2.6H2O | -55 |
Приложение 1
Примеры демонстрационных опытов по теме "Растворы"
Опыт 1. Изменение объемов при растворении жидкостей
Оборудование: мерные цилиндры (3 шт.), пробка, карандаш по стеклу, маркер или резиновые кольца; склянка для сбора раствора.
Реактивы: возможны следующие варианты: а) ацетон и вода; б) этиловый спирт и глицерин; в) этиловый спирт и вода; г) глицерин и вода; д) уксусная кислота и вода.
Техника опыта: На одном из мерных цилиндров нанесите метки, соответствующие объемам сливаемых жидкостей (см. Таблицу). Двумя другими цилиндрами отмерьте необходимое количество веществ, слейте оба вещества в помеченный цилиндр, закройте его пробкой и переверните несколько раз для того, чтобы жидкости перемешались. Отметьте суммарный объем полученного раствора. Вылейте раствор в заранее приготовленную склянку. Помните, что растворение сопровождается изменением температуры. Поэтому измерять суммарный объем нужно только после того, как раствор примет комнатную температуру.
КОЛИЧЕСТВЕННЫЕ ОТНОШЕНИЯ ВЕЩЕСТВ В ХОДЕ ОПЫТА
| Примеры смесей | Объем полученного раствора, мл |
| 5 мл ацетона и 5 мл воды | 8 - 9 |
| 5 мл спирта и 5 мл глицерина | 8 - 9 |
| 50 мл спирта и 50 мл воды | 97 - 98 |
| 45 мл глицерина и 43 мл воды | |
| 60 мл уксусной кислоты и 18 мл воды |
Примечание. Увеличение объема жидкости можно наблюдать при смешивании 50 мл нитрометана и 50 мл этилового спирта.
Опыт 2. Смешивание пшена и гороха
Оборудование и реактивы: цилиндр, банка с крышкой; пшено, горох.
Техника опыта: В цилиндр, разделенный метками (50 и 50 мл), насыпьте до первой метки пшено, а затем до второй метки - горох.Поскольку перемешивать в цилиндре неудобно, пересыпьте смесь в банку с крышкой и тщательно перемешайте. Полученную смесь пшена и гороха снова пересыпьте в цилиндр. Зафиксируйте заметное уменьшение общего объема смеси.
Тема 11. Методика изучения основных закономерностей химических реакций
Изучив тему, вы должны
ЗНАТЬ:
· структуру содержания понятия "химическая реакция", взаимосвязь ее компонентов;
· качественные и количественные характеристики химических реакций;
· связь понятия "химическая реакция" с теоретическими темами и другими понятиями школьного курса химии;
· объем сведений о химической кинетике, термодинамике, химическом равновесии в школьных программах и учебниках;
· основные типы расчетных задач по теме.
УМЕТЬ:
· привлекать средства наглядности при изучении основных закономерностей химических реакций;
· составлять комплекты расчетных химических задач по теме;
· планировать и проводить химический эксперимент по теме;
· осуществлять контроль результатов обучения по теме.
Задания для подготовки к занятию (входной контроль):
Химическая кинетика.
1) Выясните объем сведений по теме «Скорость химической реакции. Химическое равновесие» в учебнике О.С.Габриеляна.
2) Ознакомьтесь с опорным конспектом по скорости химических реакций и зависимости ее от различных факторов (Приложение 1). Оформите конспект у себя в тетради. Умейте его озвучивать. Ответьте на вопрос (устно): какие понятия раскрываются на качественном уровне, какие - с привлечением количественных характеристик. На какие закономерности будут решаться расчетные задачи?
3) Ознакомьтесь (перепишите в тетрадь, решите) с комплектом из трех задач для усвоения определения средней скорости химической реакции, умейте его обосновывать (Приложение 3).
4) Придумайте подобный комплект из прямой и взаимообратных задач. Обратите внимание, что при составлении этих задач не используют уравнения конкретных реакций. Тем самым становится возможным свободное варьирование числовыми данными. Аналогичное задание предлагают ученикам, проверяя, усвоили ли они данное понятие.
5) Ознакомьтесь с табличной формой задач на среднюю скорость реакции для устного решения (Приложение 3).
6) Представьте текст следующей задачи (из того же школьного задачника) в виде таблицы. Решите ее устно.
Задача. Химическая реакция протекает в растворе согласно уравнению А + В = С. Исходные концентрации: А - 0,80 моль/л, В - 1,00 моль/л. Спустя 20 мин концентрация А снизилась до 0,78 моль/л. Какова стала концентрация В? С какой средней скоростью протекала за этот промежуток времени реакция, если о скорости реакции судить по убыванию концентрации вещества А, вещества В?
7) Вспомните зависимость скорости реакции от концентрации. Ознакомьтесь с задачами на закон действующих масс (Приложение 3), обоснуйте принцип их составления. Решите задачи.
8) Составьте свой набор задач на закон действующих масс, варьируя кинетические уравнения и условия.
9) Вспомните влияние температуры на скорость химической реакции. Ознакомьтесь с серией расчетных задач (Приложение 3). Решите их.
10) Умейте раскрывать зависимость скорости химической реакции от площади поверхности соприкосновения. Ознакомьтесь с текстом расчетной задачи (Приложение 3).
11) Умейте раскрывать влияние катализатора на скорость химической реакции. Познакомьтесь с возможной изобразительной наглядностью (рисунки, графики), тестами для проверки знаний по этому вопросу.
12) Выясните технику опытов по влиянию различных факторов на скорость химической реакции.
Обратимые химические реакции. Химическое равновесие.
1) Вспомните определение обратимых реакций (кинетическое), умейте приводить примеры. Умейте строить график изменения скоростей прямого и обратного процессов.
2) Вспомните, что такое смещение равновесия и какие факторы его вызывают. Умейте формулировать и объяснять принцип Ле-Шателье.
3) Ознакомьтесь с опорным конспектом по теме (Приложение 2), умейте его воспроизводить и озвучивать.
4) Выясните технику опытов по смещению химического равновесия.
Литература:
1. Чернобельская Г.М. Методика обучения химии в средней школе.- М.: Владос, 2000, с. 272-281.
2. Турлакова Е.В. Использование схем-конспектов при изучении закономерностей химических реакций // Химия в школе, 1997, №1, С. 26-29.
Задания для самостоятельного выполнения:
1. Озвучьте опорный конспект по скорости реакции и зависимости ее от различных факторов.
2. Озвучьте опорный конспект по химическому равновесию и способам его смещения.
3. Прокомментируйте и обоснуйте подбор задач на скорость химической реакции и зависимость ее от разных факторов.
4. Познакомьтесь с демонстрационными таблицами по теме, умейте их озвучивать. Предложите варианты их использования на уроке.
5. Решите серию задач но скорость химической реакции и зависимость ее от разных факторов; выполните серию упражнений по химическому равновесию и способам его смещения.
Экспериментальная часть:
Опыт 1. Зависимость скорости химических реакций от различных условий
Для демонстрации опытов используются как заводские приборы (Рис. 1), так и самодельные (Рис. 2). Принцип их работы одинаков.
а)  б)
б) 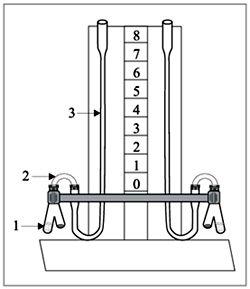
Рис. 1. Заводские приборы для демонстрации зависимости скорости химической реакции от различных условий: а) с демонстрационными пробирками: 1 - панель-подставка; 2 - пружинящие хомутики; 3 - пробирки; 4 - стеклянные трубки; 6 - резиновые трубки; 7 - манометрические трубки; 8 - шкала; б) с сосудами Ландольта: 1 - сосуд Ландольта; 2 - резиновая трубка; 3 - манометрическая трубка.

Рис. 2. Самодельный прибор для демонстрации зависимости скорости реакции от различных факторов (см. Описание установки).
Описание установки (Рис. 2):
Установка состоит из двух штативов, в которых укреплены водяные манометры (1). Водяной манометр образуют две стандартные стеклянные трубки из школьного набора, соединенные внизу кусочком резиновой трубки. Отростки манометра крепятся в лапках в верхней своей части, чтобы большая часть манометрической трубки была свободна для наблюдения. Отростки параллельны друг другу.
В манометры налита вода, подкрашенная любым красителем, хорошо видным издали, например, фуксином. Первоначальный уровень воды в обеих трубках манометра одинаков. Он отмечен на двух трубках манометра (2, 3) узкими кусочками бумаги или резиновыми кольцами, окрашенными ярко, контрастно к красителю. Внешние колена(4, 5) одного и второго манометров с помощью резиновых трубок соединены со стеклянными трубками, вставленными в пробки, герметично закрывающие реакционные пробирки (6, 7). (Кольца или кусочки бумаги отмечают уровень воды, до которого она поднимается, когда пустые пробирки закрываются герметично пробками).
Внутренние колена (8, 9) манометров через резиновые трубки соединены со стеклянными трубками, опущенными в химические стаканы, укрепленные на сетках. Стеклянные стаканы служат предохранительными склянками. В них выбрасывается краситель, когда экспериментатор вовремя не прекратит наблюдения, не снимет реакционные пробирки с пробок.
Наполнение манометров водой с красителем.
Манометры поднимают концами (10, 11) вверх. В одно из отверстий наливают подкрашенную воду. Встряхиванием трубок добиваются приблизительного равенства положения красителя в манометре. Манометрическую трубку зажимают в лапках штатива. При надевании пробирки с воздухом часть красителя перегоняется во внутреннее колено(8, 9).
Работа с установкой
С установкой работают двое – учитель и ученик – ассистент (демонстрационный вариант эксперимента) или два ученика (лабораторный вариант).
Работа экспериментаторов должна быть синхронной. Они должны наливать или насыпать одинаковое количество веществ, одновременно приводить в соприкосновение вещества, одновременно закрывать реакционные пробирки пробками и вести наблюдения за перемещением красителя во внутренних трубках манометров. Когда по положению красителя становится возможным сделать однозначный вывод, экспериментаторы открывают пробки, выливают содержимое и готовят их к новым опытам. На установке проводят следующие опыты:
1) Зависимость скорости реакции от природы веществ. К 5 мл HCl 1н и 5 мл СН3СООН 1н добавляют кусочки магния длиной в 0,5см.
2) Зависимость от концентрации веществ. К 5 мл HCl 1:4 и 5 мл HСl 1:10 одновременно добавляют 4 кусочка цинка одинакового размера.
3) Зависимость от температуры. К 5 мл HCl 1:4, до опыта подогретой в реакционной пробирке до 400С, и к 5 мл HCl 1:4, не подогретой, одновременно добавляют 4 кусочка цинка одинакового размера.
4) Зависимость от поверхности веществ. К 5 мл HCl 1:5 в одной пробирке добавляют 1 кусочек магния, одновременно в другой пробирке к 5 мл HCl 1:5 присыпают равное по весу количество порошка магния. (Грученко Г.И.)
|
из
5.00
|
Обсуждение в статье: Примеры лабораторных опытов при формировании первоначальных химических понятий |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

