 |
Главная |
Опыт 1. Определение рН воды
|
из
5.00
|
Для измерения рН можно использовать универсальную индикаторную бумагу, а для более точного измерения используется потенциометрический метод, лежащий в основе работы рН-метров. Измеряется электродвижущая сила между стеклянным электродом (индикатором Н+ ионов) и электродом сравнения. Известно, что значение потенциала стеклянной мембраны изменяется обратимо по отношению к активности водородных ионов. Электродвижущая сила, измеренная с помощью рН-метра, регистрируется в единицах рН.
Материалы и оборудование
Универсальная индикаторная бумага или рН-метр
Стаканы на 50 или 100 мл
Пипетки на 1 мл
Проба воды
1М раствор NaOH
1M раствор H2SO4 или HCl
Методика
1. Налейте воду в стакан и опустите в исследуемую воду кусочек универсальной индикаторной бумаги и сравните ее цвет с цветной шкалой. Определите значение рН.
2. Ополосните зонд рН-метра дистиллированной водой, опустите его в стакан с пробой исследуемой воды и снимите показания рН. Вновь ополосните зонд дистиллированной водой перед тем, как поместить его на хранение в буферный раствор.
3. Повторите опыт с модельными пробами воды, имитирующими пробы воды из различных источников. Для этого в стакан с исследуемой водой добавьте несколько капель 1М раствора H2SO4 или HCl, перемешайте и измерьте рН смоделированной воды на рН-метре.
4. В стакан с водой добавьте несколько капель 1М раствора NaOH, перемешайте и измерьте рН второй смоделированной воды.
5. Запишите результаты всех трех измерений и сделайте вывод о пригодности данных водных сред для жизнедеятельности живых организмов.
Опыт 2.Определение содержания хлоридов в природных водах методом осаждения (приблизительная оценка солености)
Содержание растворенных солей в водах открытого океана составляет 3,5%, из которых 2,7%, приходится на долю поваренной соли – NaCl. Поэтому соленость вод приблизительно можно оценить, определяя в них содержание хлоридов методом осаждения, используя осаждение хлоридов в виде нерастворимого хлорида серебра – AgCl по реакции:
NaCl + AgNO3 → AgCl↓ + NaNO3
белый осадок
Анализ проводится титриметрически. Титриметрический метод анализа основан на точном измерении количества реактива, израсходованного на реакцию с определяемым веществом. Титрование - прибавление титрованного раствора к анализируемому для определения точного эквивалентного его количества. Титрованный раствор – раствор, концентрация которого точно известна. Момент титрования, когда количество добавленного титрованного раствора эквивалентно количеству определяемого вещества, называется точкой эквивалентности.
Методы осаждения основаны на реакциях образования малорастворимых соединений.
Материалы и оборудование
Проба исследуемой воды
Пипетка объемом 5 или 10 см3
Бюретка
Дистиллированная вода в бутыли
3 конические колбы
Белая кафельная плитка
Калийхроматный индикатор – 2 %-ный раствор K2CrO4
0,05н раствор нитрата серебра – AgNO3
Методика
1. Налейте 1-2 см3 исследуемой воды в коническую колбу и добавьте 2 капли калийхроматного индикатора и 10 см3 дистиллированной воды, все хорошо потрясите.
2. Из бюретки оттитруйте раствором нитрата серебра, постоянно встряхивая коническую колбу.
3. В конечной точке титрования осадок хлорида серебра окрашивается в красный цвет из-за образования хромата серебра красного цвета по реакции:
K2CrO4 + 2AgNO3 → Ag2CrO4↓ + 2KNO3
красный осадок
4. Дважды повторите титрование с таким же объемом исследуемой воды. Подсчитайте среднее количество израсходованного нитрата серебра.
5. Рассчитайте содержание хлоридов (%) в анализируемой воде по формуле:

где  – концентрация,
– концентрация,  – объем нитрата серебра, мл;
– объем нитрата серебра, мл;
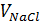 – объем анализируемой воды, мл;
– объем анализируемой воды, мл;
58,5 – молекулярная масса NaCl.
6. Сделайте вывод, исходя из содержания солей, к какому типу вод относится исследованная вода, какие живые организмы могут жить в данной водной среде, можно ли использовать ее для хозяйственно-питьевого, культурно-бытового и других видов водопотребления.
|
из
5.00
|
Обсуждение в статье: Опыт 1. Определение рН воды |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

