 |
Главная |
В каждой окислительно-восстановительной реакции проставить степени окисления и записать полуреакции
|
из
5.00
|
Написать названия соединений в химических реакциях.
Для реакций, в которых происходит гидролиз какого-либо продукта, написать уравнение гидролиза.
Приложение
В IV группу входят углерод  , кремний
, кремний  , германий
, германий  , олово
, олово  и свинец
и свинец 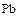 . Электронная конфигурация невозбужденных атомов элементов
. Электронная конфигурация невозбужденных атомов элементов 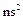
 (валентные электроны), причем на р-орбиталях находится 2 неспаренных электрона (правило Гунда):
(валентные электроны), причем на р-орбиталях находится 2 неспаренных электрона (правило Гунда):
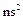

 
| 
| 
|
В своих соединениях элементы IV-A- группы, имеют, как правило, две степени окисления: (+II) или (+IV). Устойчивость соединений со степенью окисления (+II) увеличивается от С к Рb, что подтверждается в частности изменением энергии Гиббса:
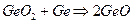
 41 кДж
41 кДж

 6 кДж
6 кДж
 ,
, 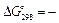 185 кДж
185 кДж
Из значений  следует, что соединения
следует, что соединения  (II) должны быть сильными восстановителями, а соединения
(II) должны быть сильными восстановителями, а соединения 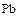 (IV) - сильными окислителями (
(IV) - сильными окислителями (  ,
,  ).
).
Элементы IV - А - группы в степени окисления (+IV) образуют слабые кислоты (  ,
,  ,
, 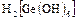 ,
,  ,
, 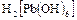 ), а со степенью окисления (+II) – малорастворимые основания составов
), а со степенью окисления (+II) – малорастворимые основания составов  ,
, 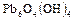 , которые проявляют амфотерные свойства. Устойчивость гидридов резко падает от метана
, которые проявляют амфотерные свойства. Устойчивость гидридов резко падает от метана  (
(  51 кДж/моль) к плюмбату
51 кДж/моль) к плюмбату  . Уже моносилан
. Уже моносилан  является эндотермическим соединением (
является эндотермическим соединением (  57кДж/моль).
57кДж/моль).
Гидролиз всех тетрагалогенов термодинамически возможен:
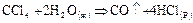
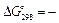 380 кДж
380 кДж

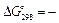 278 кДж
278 кДж
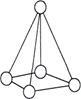 Углерод, кремний и германий имеют несколько аллотропных модификаций, одной из которых является модификация с атомной кристаллической решеткой алмаза.
Углерод, кремний и германий имеют несколько аллотропных модификаций, одной из которых является модификация с атомной кристаллической решеткой алмаза.
Алмаз - метастабильная модификация углерода. В его кристаллах каждый атом углерода окружен 4 такими же атомами, располагающимися в вершинах правильного тетраэдра.
 Графит - стабильная аллотропная модификация углерода со слоистой структурой, состоящая из шестичленных бесконечных колец.
Графит - стабильная аллотропная модификация углерода со слоистой структурой, состоящая из шестичленных бесконечных колец.
Кристаллическую решётку графита можно считать переходной между молекулярной и металлической решетками.
Кристаллическая решётка третьей аллотропной модификации углерода - карбина состоит из линейных цепей. Расстояние между ними меньше, чем между слоями графита, за счет более сильного межмолекулярного взаимодействия. Карбин образует кристаллы белого цвета. У углерода допускают существование еще двух малоизученных модификации металлического углерода (углерод (III) и углерода  ). Химическая активность возрастает от углерода (графит) к германию, а среди аллотропных модификаций углерода наименее химически активен алмаз. При пропускании, водяного пара через сильно нагретые
). Химическая активность возрастает от углерода (графит) к германию, а среди аллотропных модификаций углерода наименее химически активен алмаз. При пропускании, водяного пара через сильно нагретые  ,
,  или
или  можно наблюдать реакции:
можно наблюдать реакции:


В кислороде при высоких температурах  ,
,  ,
,  сгорают с образованием оксидов
сгорают с образованием оксидов  ,
,  ,
, 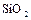 и
и  .
.
С водородом  ,
,  ,
,  непосредственно не взаимодействуют, а с
непосредственно не взаимодействуют, а с  вступает в реакцию только
вступает в реакцию только  с образованием при t выше 1300 °С белого вещества состава тетранитрида трикремния
с образованием при t выше 1300 °С белого вещества состава тетранитрида трикремния  . Кремний, в отличие от
. Кремний, в отличие от  , может взаимодействовать с углеродом при температуре около
, может взаимодействовать с углеродом при температуре около  с образованием карбида кремния
с образованием карбида кремния  -химически инертного вещества, по твердости уступающего только алмазу.
-химически инертного вещества, по твердости уступающего только алмазу.
На углерод и кремний азотная, серная, хлорная и галогенводородные кислоты в обычных условиях не действуют.
В присутствии порошка меди кремний взаимодействует с безводным  :
:

Эта реакция используется для промышленного получения трихлорсилана.
Аморфный углерод  (активированный или древесный уголь) более химически активен. Азотная кислота
(активированный или древесный уголь) более химически активен. Азотная кислота  окисляет его до
окисляет его до  :
:

В  германий подвергается пассивированию, но при нагревании медленно взаимодействует по реакции:
германий подвергается пассивированию, но при нагревании медленно взаимодействует по реакции:

Он взаимодействует с растворами 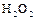 и
и  :
:


Расплавы и водные растворы 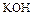 и
и 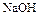 взаимодействуют только с
взаимодействуют только с  и
и  :
:


Углерод вступает в реакции с галогенами при нагревании. Со фтором углерод образует продукты состава  , где n ≥ 1 (
, где n ≥ 1 ( 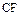 ,
, 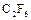 ,
,  и т.д.), а с другими галогенами «n» уменьшается до n=4, например
и т.д.), а с другими галогенами «n» уменьшается до n=4, например  ,
,  .
.
Известно несколько оксидов углерода (  ,
,  ,
,  ) и по 2 оксида
) и по 2 оксида  и
и  (
(  ,
,  ,
, 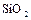 ,
,  ). Восстановительные свойства
). Восстановительные свойства  при повышенной температуре сильнее, чем у водорода в реакции:
при повышенной температуре сильнее, чем у водорода в реакции:

 - восстановитель
- восстановитель
 - окислитель
- окислитель
 участвует в реакции присоединения:
участвует в реакции присоединения:
 - формиат калия
- формиат калия
0,5 мПа
С металлами  образует комплексные соединения карбониды:
образует комплексные соединения карбониды:

Для синтеза  применяют главным образом следующие реакциии:
применяют главным образом следующие реакциии:
 - в промышленности
- в промышленности
 t
t
|

t

 Диоксид углерода -
Диоксид углерода -  - газ без цвета и запаха, тяжелее воздуха. Твердый
- газ без цвета и запаха, тяжелее воздуха. Твердый  возгоняется без плавления при 78°C. В жидком состоянии он может находиться только под давлением. Молекула
возгоняется без плавления при 78°C. В жидком состоянии он может находиться только под давлением. Молекула  линейная, длина связи
линейная, длина связи  -
-  равна 116 пм:
равна 116 пм:
В воде  растворяется: 1 л воды при 25°С и 0,1 мПа поглощает 0,76 л
растворяется: 1 л воды при 25°С и 0,1 мПа поглощает 0,76 л  . Только 1%
. Только 1%  взаимодействует с водой, образуя угольную кислоту:
взаимодействует с водой, образуя угольную кислоту:

Диоксид углерода превращает водные растворы щелочных и щелочноземельных металлов и магния в гидрокарбонаты при избытке  :
:

Гидроксиды и оксиды этих же элементов поглощают  из воздуха:
из воздуха:

Диоксид углерода и водорода взаимодействуют (  ,
,  ) в присутствии катализатора (смесь
) в присутствии катализатора (смесь  и
и 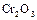 ) с образованием метанола:
) с образованием метанола:
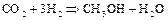
 получают в промышленности при разложении известняка:
получают в промышленности при разложении известняка:

В лаборатории его получают по реакции:

В свободном виде мономерные кислородные кислоты углерода, кремния и германия (  ,
,  ,
,  ) не получены.
) не получены.
Карбонаты под действием кислот выделяют  :
:

Протолиз  в водном растворе протекает в основном до образования гидрокарбонатных анионов.
в водном растворе протекает в основном до образования гидрокарбонатных анионов.
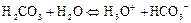
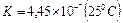
Анионная кислота  является еще более слабой:
является еще более слабой:


Кремниевые и германиевые кислоты слабее угольной, они выпадают в осадок при пропускании  через их водный раствор.
через их водный раствор.
|
из
5.00
|
Обсуждение в статье: В каждой окислительно-восстановительной реакции проставить степени окисления и записать полуреакции |
|
Обсуждений еще не было, будьте первым... ↓↓↓ |

Почему 1285321 студент выбрали МегаОбучалку...
Система поиска информации
Мобильная версия сайта
Удобная навигация
Нет шокирующей рекламы

